Genome Biology|安徽农业大学团队揭示猕猴桃抗溃疡病分子新机制
- 2026-04-18 07:57:30
点击“蓝字” 关注我们
猕猴桃(Actinidiassp.)因高维生素C含量、均衡的矿物质营养组成、膳食纤维及其他有益代谢产物,在全球广受欢迎。然而其面临的最大挑战是由丁香假单胞菌猕猴桃致病变种(Pseudomonassyringaepv. actinidiae, Psa)引发的溃疡病。利用野生近缘种是提升抗病性的关键,毛花猕猴桃对Psa具有显著抗性,目前仅有少量毛花猕猴桃基因组组装数据,限制了其遗传变异的解析与利用。
2026年4月9日,安徽农业大学刘永胜团队在Genomebiology发表了题为“Allelic structural variation at the NLR25-1 locus enhances defense against Pseudomonas syringae in kiwifruit”的研究论文,研究完成了12份猕猴桃的基因组组装,结合已发表的12个基因组,构建了无参考偏差的图形泛基因组。该数据集揭示了广泛的基因组变异,鉴定出一个具有等位基因特异性表达的野生等位基因AeNLR25-1,该基因可增强栽培猕猴桃的Psa抗性。


材料方法
基因组组装:11份野生毛花猕猴桃(覆盖自然分布区),1份毛花猕猴桃‘White’与中华猕猴桃中华变种‘H0809’的种间杂交F₁个体‘HH-1’;
泛基因组构建:结合已发表的3份毛花猕猴桃和9份中华猕猴桃;
转录组测序:16 份种质(毛花猕猴桃和中华猕猴桃中华变种各8份)的叶片,毛花猕猴桃×中华猕猴桃中华变种F₁杂种‘HH-1’叶片经Psa接种后0、12、72小时,3个生物学重复;
其他:qRT-PCR、CRISPR敲除、过表达验证、双荧光素酶实验、酵母单杂交、EMSA、Psa接种、生理指标检测等。

研究结果
1.完成12份猕猴桃材料高质量基因组组装,揭示种间基因组差异
为捕获基因组变异,研究选取11份野生毛花猕猴桃及毛花猕猴桃与中华猕猴桃杂交种进行基因组组装;最终获得24个高质量单倍型基因组,组装大小581.2-630.7 Mb,Contig N50为5-21 Mb,BUSCO完整性平均为98.62%,LAI均超过18.94,达到“参考级”标准。
随后用EDTA工具包注释转座元件(TE),发现毛花猕猴桃基因组平均比中华猕猴桃中华变种大约12.5 Mb,其TE含量略高,基因组大小增加主要源于TE片段扩增,同时结合多种方法在24个组装基因组中预测到42,742-48,555个基因。
2.猕猴桃种间泛基因组构建及结构变异解析
研究首先基于15份毛花猕猴桃的28个单倍型构建其泛基因组,获得54,770个饱和基因家族并划分为核心、软核心、非必需和特有四类;在此基础上整合18个中华猕猴桃单倍型,构建出跨物种泛基因组,46个单倍型共形成56,572个饱和基因家族,其中核心基因参与基础生命过程,可变基因富集于免疫应答、次生代谢等抗逆通路,是物种间抗病性差异的重要遗传基础。
随后采用PGGB流程构建无参考偏差的图形泛基因组,该基因组大小2.24 Gb,为MDHAPA基因组的3.6倍,共鉴定出超3100万个SNP、1300多万个小片段InDel及62万余个结构变异SV,为抗病基因挖掘提供了丰富资源;其中SV多小于2 Kb,总序列量达1.5 Gb,48.05%的SV由转座子插入驱动,同时筛选出269,784个种间高度分化SV,是毛花猕猴桃与中华猕猴桃遗传分化和性状差异的核心因子。
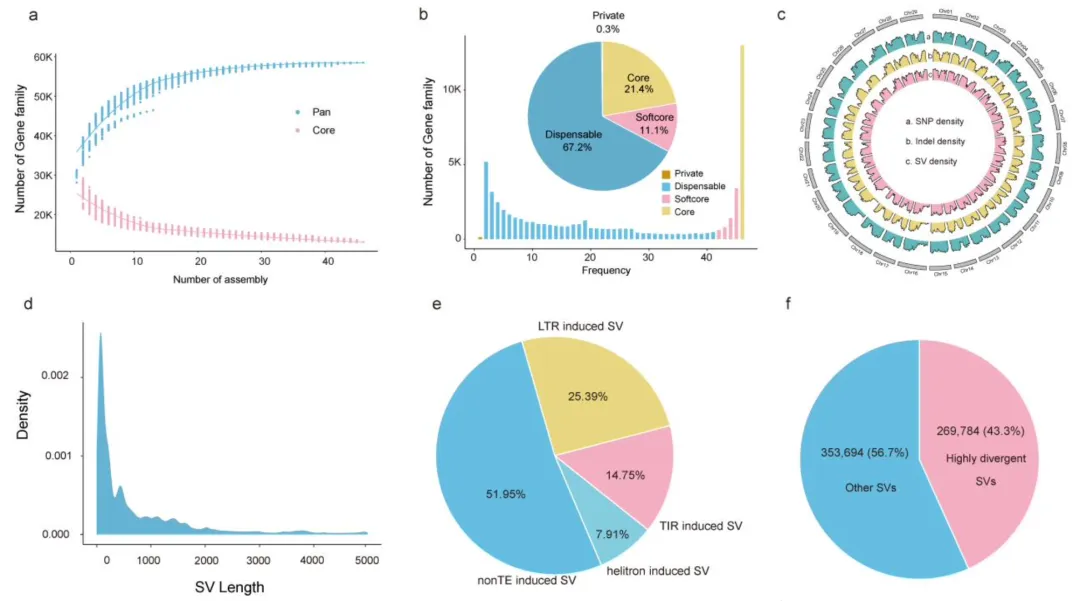
图1 毛花猕猴桃与中华猕猴桃栽培类种种间泛基因组的构建与分析
3.泛NLR组构建明确免疫基因家族的种间差异
NLR基因作为植物抗病核心免疫受体,本研究首次构建了猕猴桃泛NLR组,全基因组共鉴定出7,692个NLR基因,不同材料中该基因数量介于130-210个之间,差异显著;研究将其划分为TN、CN、NL、CNL、NB、TNL 6类,其中毛花猕猴桃的TNL型NLR基因数量显著多于中华猕猴桃;同时划分出99个非冗余NLR直系同源群,核心、软核心及可变类群分别占比9.1%、26.3%和64.6%,并发现9个仅存在于毛花猕猴桃、在中华猕猴桃中完全缺失的NLR直系同源群,这些是野生猕猴桃抗病的潜在关键基因;此外,448个种间高度分化结构变异(SV)与69个NLR基因相关,直接关联两个物种间的抗病性差异。
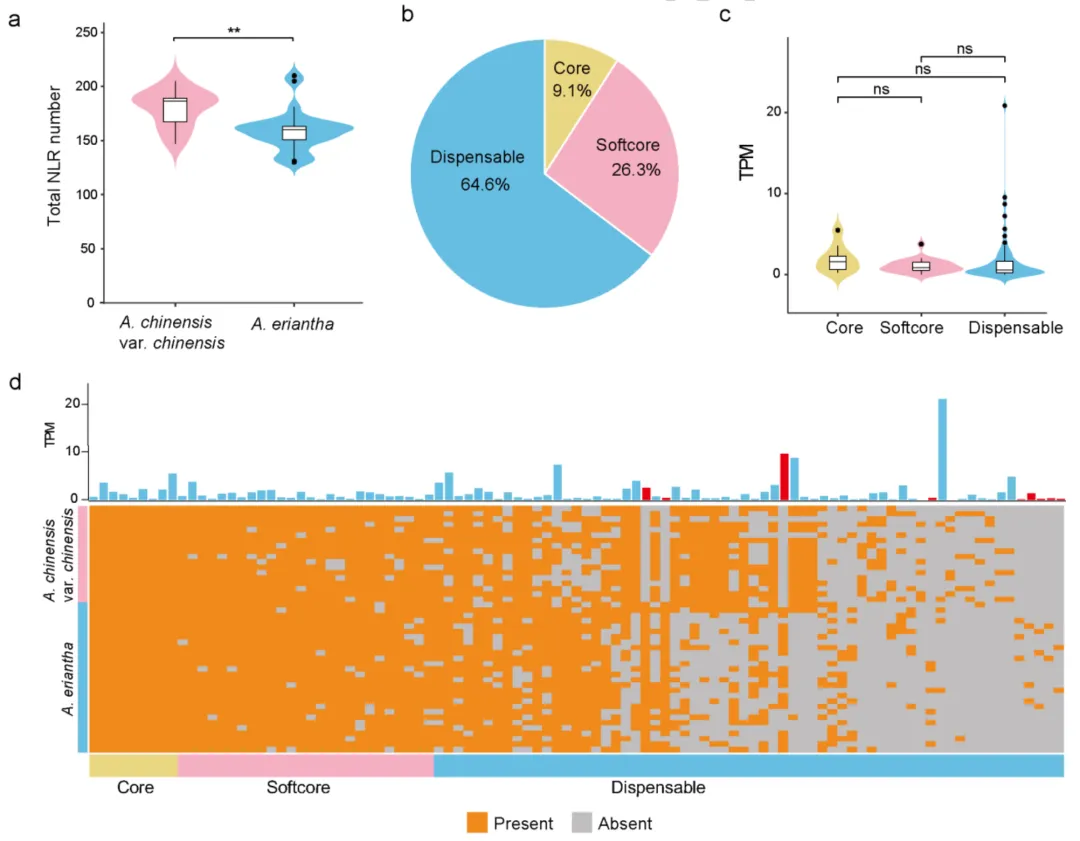
图2 毛花猕猴桃与中华猕猴桃泛基因组水平的泛NLR 组解析
4.中华猕猴桃中华变种与毛花猕猴桃的Psa抗性差异及种间F₁杂交种中NLR25-1等位基因特异性表达的物种特异性结构变异
本研究针对中华猕猴桃普遍感溃疡病(Psa)、毛花猕猴桃高抗Psa的表型差异,以抗病毛花猕猴桃‘White’与感病中华猕猴桃‘H0809’杂交获得F₁代‘HH-1’,接种鉴定显示父本严重感病、母本近免疫,杂种呈中间抗性,且群体验证毛花猕猴桃种质均高抗、中华猕猴桃多感病。
对‘HH-1’进行Psa诱导转录组分析,鉴定出大量差异表达基因与等位基因,并筛选到多个时间点的等位基因特异性表达基因(ASEGs),其中偏向毛花单倍型的抗病基因上调数量显著多于中华来源;进一步锁定位于种间特异结构变异区的NLR25-1,该基因在杂种中强烈偏向表达毛花型AeNLR25-1,中华型AcNLR25-1 几乎不表达,二者编码区存在34个SNP并导致20个氨基酸替换。
机制解析发现,NLR25-1 启动子区存在保守种间结构变异,毛花猕猴桃在该位点上游含有约3.5kb的特异插入片段AeSV并携带6个转座元件,中华猕猴桃则被短片段AcSV替代且仅含1个转座元件,该启动子结构差异是其等位基因特异性表达的核心原因。
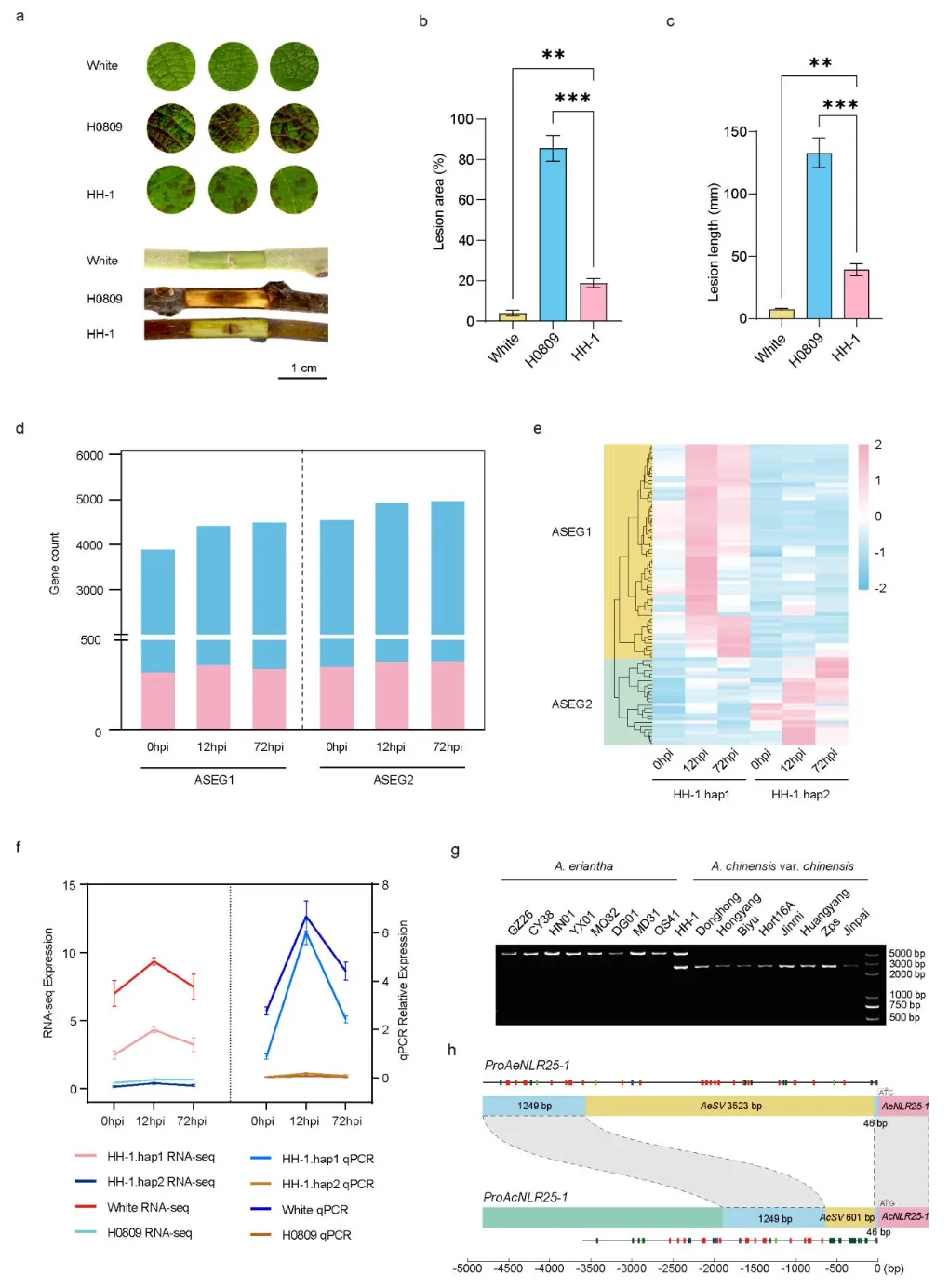
图3 启动子区SV导致毛花猕猴桃与中华猕猴桃F₁杂种中NLR25-1 位点的等位基因特异性表达
5.多维度验证NLR25-1 抗病功能
为解析NLR25-1 的生物学功能,研究通过CRISPR-Cas9技术获得‘HH-1’的3 个NLR25-1敲除突变体,Psa接种后,突变体叶盘病斑、菌体生长量均显著高于野生型(WT),盆栽苗症状更严重;生理及分子检测显示,突变体免疫应答弱、细胞损伤重、防御酶活性低,水杨酸通路防御基因表达上调幅度远低于WT,证实NLR25-1 在抗Psa中起关键作用。
随后,以‘H0809’为受体获得3个AeNLR25-1 过表达株系,接种后过表达株系病斑更小、菌体生长更少,免疫应答及防御能力显著强于WT,进一步验证其抗Psa功能。
此外,构建‘HH-1’与‘H0809’的BCF₁回交群体,120个后代分型为杂合子(AeNLR25-1/AcNLR25-1)和纯合子(AcNLR25-1/AcNLR25-1),表型显示杂合子病斑更小、抗性更强,进一步支持AeNLR25-1 偏好表达的免疫功能,综上明确AeNLR25-1 是调控猕猴桃抗Psa的关键基因。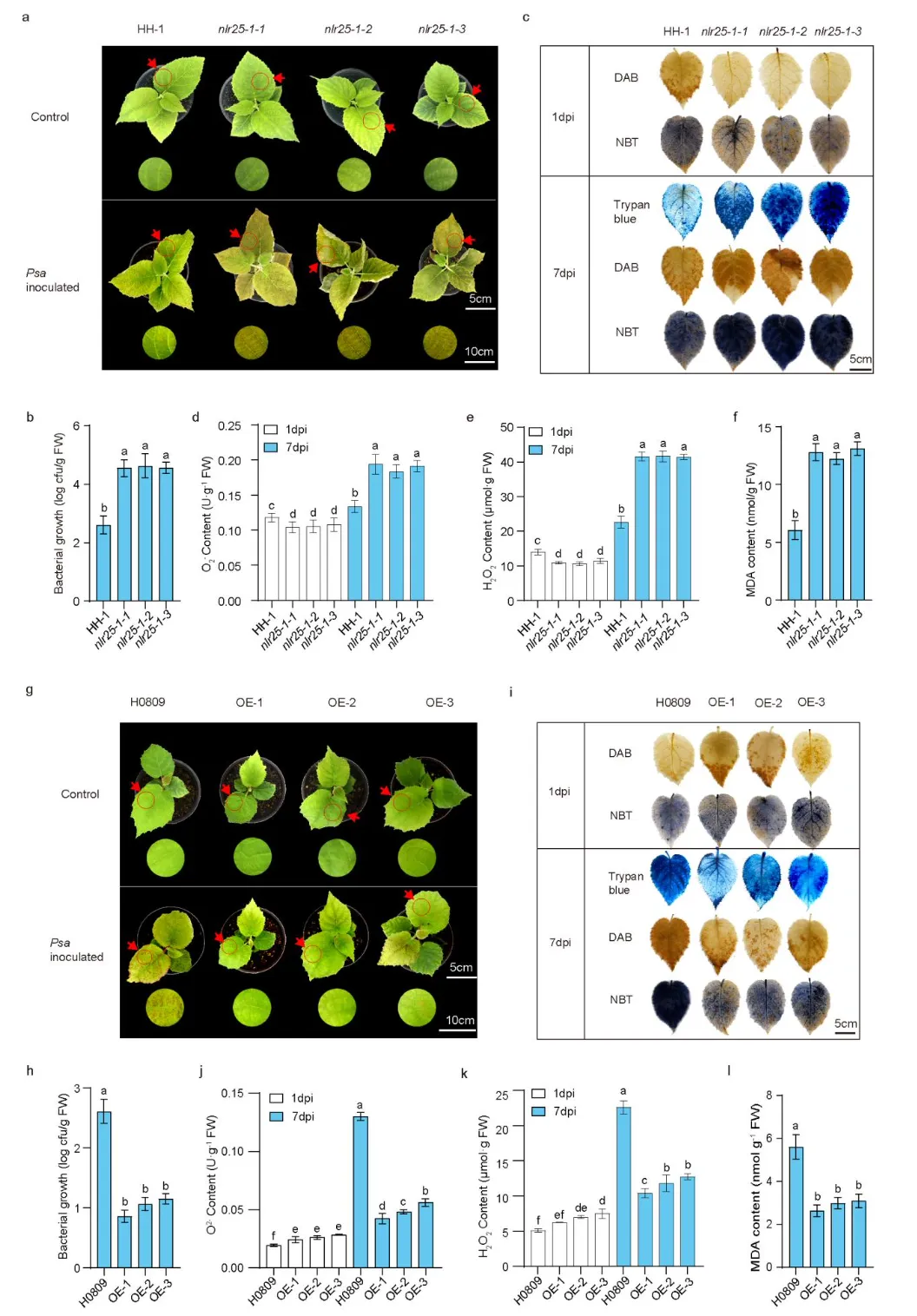
图4基于敲除突变体与过表达转基因株系解析NLR25-1在响应猕猴桃溃疡病菌(Psa)侵染中的功能
6. AeWRKY75与AcWRKY75特异性结合AeSV并激活AeNLR25-1 转录及免疫应答
为探究结构变异对两种等位启动子活性的影响,研究通过GUS染色证实ProAeNLR25-1 启动子活性显著高于ProAcNLR25-1,与前期表达结果一致。转录组分析显示,Psa接种12小时大量转录因子上调且WRKY家族富集,经筛选与双荧光素酶验证,确定AeWRKY75可激活AeNLR25-1 启动子。
进一步克隆其等位基因AcWRKY75,发现二者均受Psa诱导表达,且均可通过结合AeSV区域的AeW-box顺式元件激活AeNLR25-1启动子,而AcNLR25-1 启动子因缺少该元件无法被激活。
随后获得WRKY75敲除突变体,分子检测表明突变体中AeNLR25-1 的本底表达与诱导上调幅度均显著低于野生型;表型及生理生化实验显示,突变体病斑更大、菌体增殖更快,免疫应答、抗氧化酶活性与防御基因诱导均显著弱于野生型,最终证实WRKY75通过特异性激活AeNLR25-1 表达,在猕猴桃抗Psa过程中发挥关键调控作用。
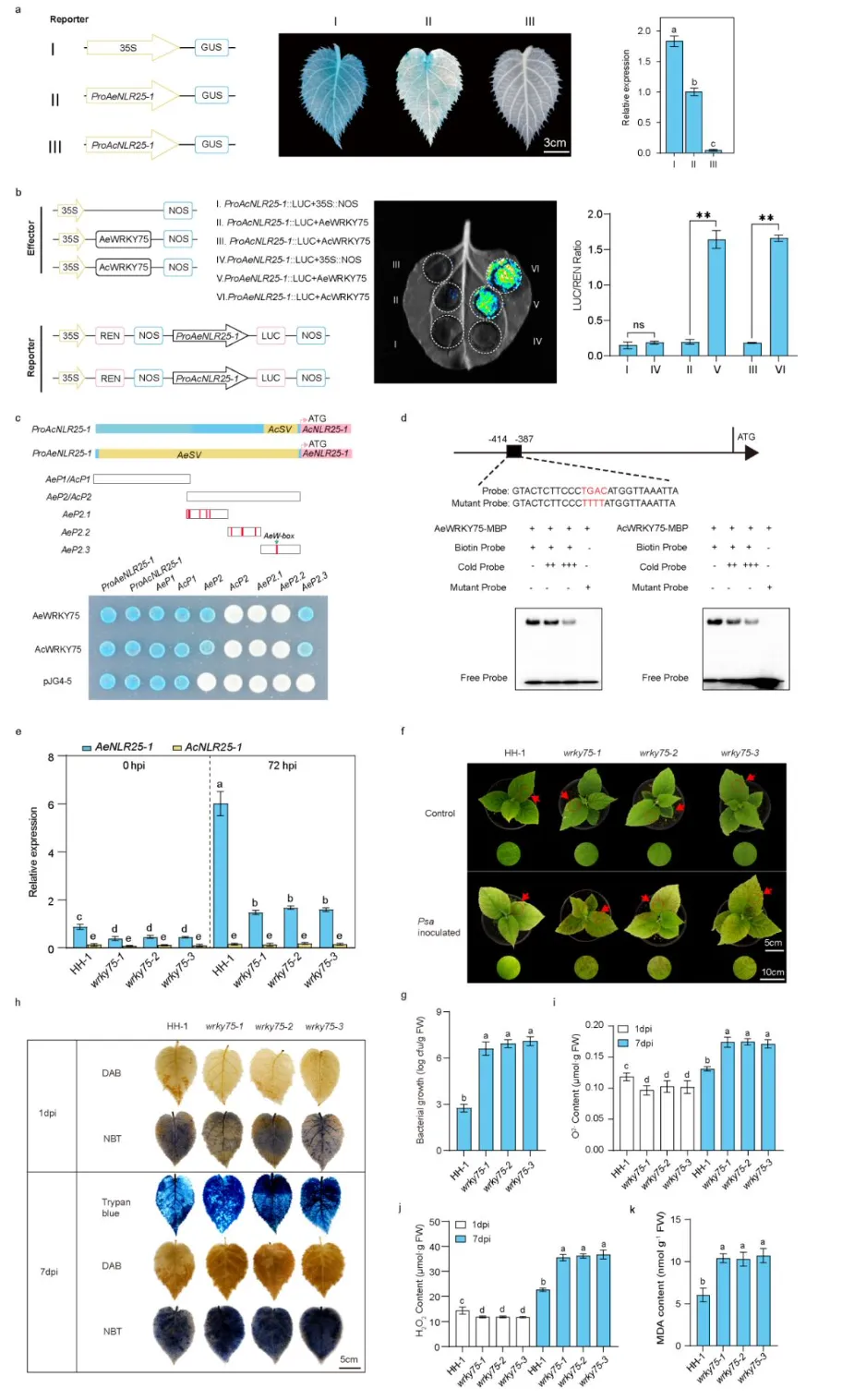
图5 AeWRKY75/AcWRKY75可特异性结合并激活AeNLR25-1 启动子,进而赋予猕猴桃对猕猴桃溃疡病菌(Psa)的抗性

小结
本研究通过构建毛花猕猴桃与中华猕猴桃的种间泛基因组,系统解析了猕猴桃基因组变异与抗病性的关联机制,明确转座子驱动的启动子结构变异使野生毛花猕猴桃的AeNLR25-1 呈现等位特异性高表达,该基因可被AeWRKY75/AcWRKY75特异性结合激活,进而启动免疫通路、显著提升猕猴桃对Psa溃疡病的抗性,研究不仅阐明了野生猕猴桃抗病的分子机理,更为挖掘优异野生等位基因、加速猕猴桃遗传改良提供了重要理论框架。
参考文献
Wu Y, Wang Y, Lin Y, et al. Allelic structural variation at the NLR25-1 locus enhances defense against Pseudomonassyringae in kiwifruit. Genome Biol. 2026 Apr 9.
往期回顾

