江西农业大学黄路生院士团队最新Science:构建全球首个“全家桶式”猪单细胞时空图
- 2026-05-19 20:51:46
2026年3月10日,江西农业大学黄路生团队在Science在线发表题为“Family single-cell atlases reveal pig pregnancy and fetal growth restriction critical cell types”的研究论文。该研究构建了全球首个“全家桶式”(All-from-one)猪单细胞时空图谱。该研究利用单细胞转录组测序(scRNA-seq)与单细胞核转录组测序(snRNA-seq)技术,对一头怀孕母猪(F1M1)及其雄性胎儿(F1S1)的405个样本进行了深度分析。图谱涵盖了胎儿115个组织位点和母体119个组织位点,总计包含256万个细胞。这一规模宏大的数据不仅绘制了生命全景,更在细胞分辨率下精确解析了妊娠期的复杂生理重塑。
一、研究背景
单细胞图谱的局限:现有单细胞图谱多整合自不同个体,受遗传、年龄、环境等因素干扰,难以实现对细胞类型、转录因子等的精准比较。
妊娠研究的技术瓶颈:人类妊娠期母体与胎儿组织难以获取,且小鼠等模型在心脏生理(如心率)上与人类差异大,限制了机制研究。
FGR的临床重要性:FGR影响5-10%的人类妊娠,是围产期死亡和疾病的重要原因,但其细胞与分子机制尚不明确。
猪作为理想模型:猪在解剖、生理、基因组等方面与人类高度相似,且FGR发生率更高(15-20%),为研究妊娠适应与发育异常提供了独特优势。
二、研究方法
“all-from-one”实验设计:从一头怀孕母猪(115个组织)及其胎猪(119个组织)中同时采集样本,控制遗传与环境变量。
多组学技术整合:单细胞/单核RNA测序(scRNA-seq/snRNA-seq):覆盖256万个细胞。代谢组学、体外细胞系、类器官(滋养层、肌肉)、基因编辑猪、大鼠模型等。
多阶段心脏分析:比较非孕、晚孕、产后母猪的心脏组织,识别妊娠特异性细胞亚型。
FGR研究策略:利用同窝正常体重(NW)与生长受限(GR)胎猪,结合转录组、代谢组、功能实验(如L-亮氨酸补充)解析机制。
三、研究结果
构建全身单细胞图谱:识别出76种主要细胞类型,412种内皮细胞亚型。发现内皮细胞在免疫调控、代谢等功能上存在组织与发育阶段特异性,尤其脑与外周差异显著。
妊娠期心脏适应性重塑:发现妊娠特异性心脏毛细血管内皮亚型(Cap2),其在妊娠期富集,表达脂肪酸转运基因,产后恢复。Cap2通过促进脂肪酸利用、抑制葡萄糖代谢,支持妊娠期心肌能量需求。
FGR的关键机制:FGR胎猪的滋养层细胞中氨基酸转运蛋白(SLC1A5、SLC38A2)表达下调,导致L-亮氨酸转运不足。胎猪肌肉中特定II型肌纤维亚型(type IIC1)比例下降,影响肌肉发育与体重增长。L-亮氨酸补充实验(猪、大鼠、人源类器官)证实其可部分恢复肌纤维发育与体重。
跨物种保守性:猪与人心脏Cap2亚型、滋养层细胞、肌纤维亚型等在基因表达与功能上高度保守。
四、研究结论
“all-from-one”策略的有效性:成功构建了首个同一个体全身单细胞图谱,为研究细胞身份、转录因子调控等提供了“纯净”背景。妊娠心脏适应的细胞基础:揭示了Cap2内皮细胞在妊娠期心脏代谢重塑中的关键作用。FGR的机制链:明确了“滋养层氨基酸转运障碍 → L-亮氨酸缺乏 → 特定肌纤维发育受损 → 胎儿体重下降”的因果路径。跨物种保守性:猪模型在心脏、胎盘、肌肉等组织层面与人类高度一致,支持其作为人类妊娠与发育研究的理想模型。
技术推广与标准化:该“all-from-one”策略可推广至其他物种或疾病模型,为构建高质量参考图谱提供范式。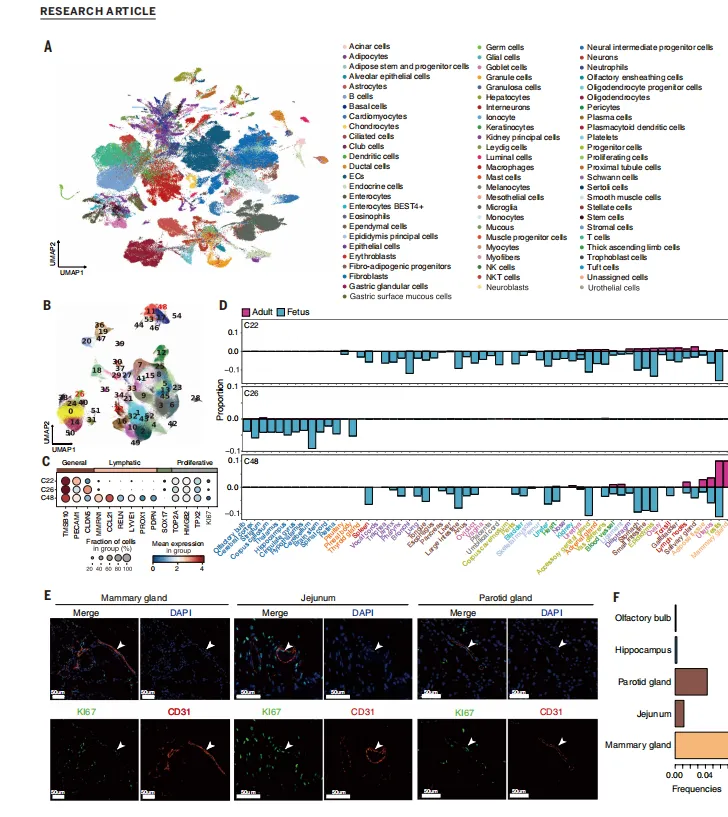 图 2. “一体化”单细胞图谱的构建以及胎儿和成年猪全身器官中内皮细胞(EC)全景的特征描述。
图 2. “一体化”单细胞图谱的构建以及胎儿和成年猪全身器官中内皮细胞(EC)全景的特征描述。
五、未来研究前景
人类妊娠疾病机制研究:利用猪模型进一步探究妊娠期高血压、心肌病等疾病的细胞机制。
FGR早期诊断与干预:基于氨基酸转运通路开发生物标志物或营养干预策略,优化L-亮氨酸补充时机与剂量。
细胞类型特异性转录因子功能研究:如IRX6在微胶质细胞中的作用,可深入探索其在神经发育与疾病中的功能。
跨物种比较与转化医学:利用该图谱与人类、小鼠等数据整合,构建跨物种细胞调控网络,推动猪在异种移植、药物评估等领域的应用。
技术推广与标准化:该“all-from-one”策略可推广至其他物种或疾病模型,为构建高质量参考图谱提供范式。
微信加群
公众号汇集了上万名医学和生命科学研究人员。我们组建了多个专业的科研交流群。分享最新最前沿的医学生命科学科研思路及其原文、科研统计交流,同时对于需要申报基金课题的PI和中高级职称人员,我们整理了相关的国自然基金课题申报资料和既往中标标书,可联系工作人员获取。温馨提示:进群可长按下面二维码,添加小编,备注“加群”,之后再邀请进专业群,非诚勿扰。

