《食品科学》:华南农业大学岳淑丽副教授、广东省农业科学院胡斌高级畜牧师等:基于脂质组学和风味组学分析肌内脂肪对杜花猪肉的影响
- 2026-04-17 16:33:58

01
IMF含量差异分析
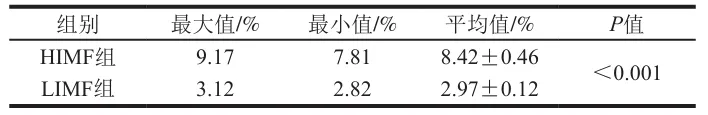
基于165 个样本IMF含量测定结果,获得了165 个连续分布的原始数据。对165 个IMF数据进行正态性检验,确认数据符合正态分布。基于该数据分布特征设定分组阈值,高肌内脂肪(HIMF)组:IMF含量≥均值+1 倍标准差。低肌内脂肪(LIMF)组:IMF含量≤均值-1 倍标准差。初步筛选后,HIMF组符合阈值的样本共20 个,LIMF组符合阈值的样本共19 个。按“组内标准差最小化”原则从两组中各选取6 个样本。统计分析显示,两组间T检验得到的P值小于0.001,差异高度显著(表1)。

02
脂质组成分析
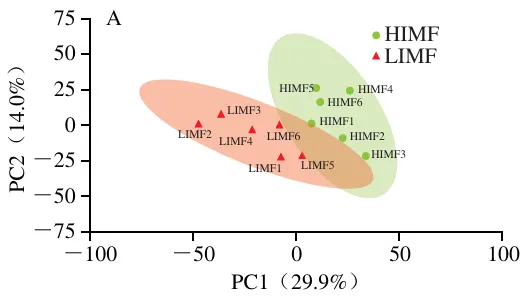
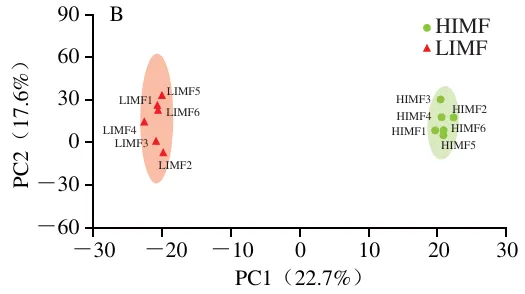
采用均值中心化的无监督PCA模型对HIMF组和LIMF组进行质控分析。结果表明,两组的脂质提取物在数据集中被PC1(29.9%)和PC1(14.0%)明显区分(图1A)。OPLS-DA作为一种集成监督模式识别的多元统计分析方法,旨在消除背景噪声和组内误差干扰的影响,最大化组间差异。OPLS-DA模型( RX2=0.834,RY2=0.862,Q2=0.488)显示,两组间的分离状况良好,表明该模型具有较好的诠释和预测能力,实验数据具有良好的重复性(图1B)。
 |  |

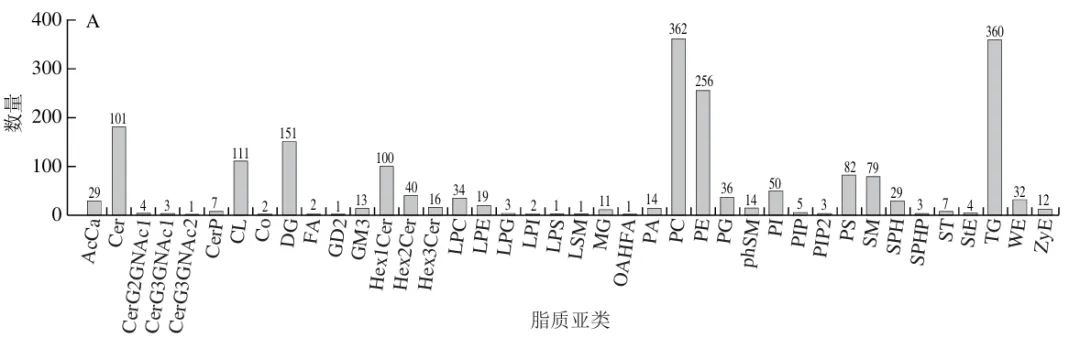
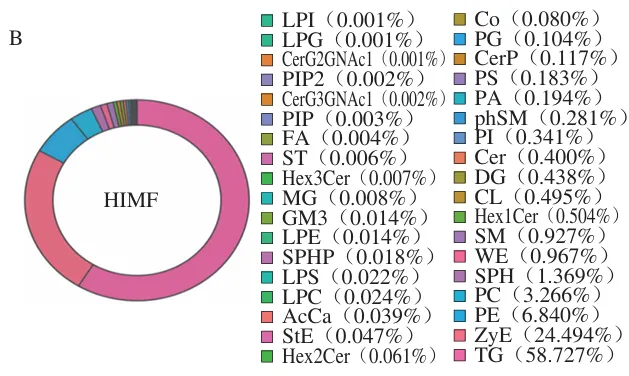
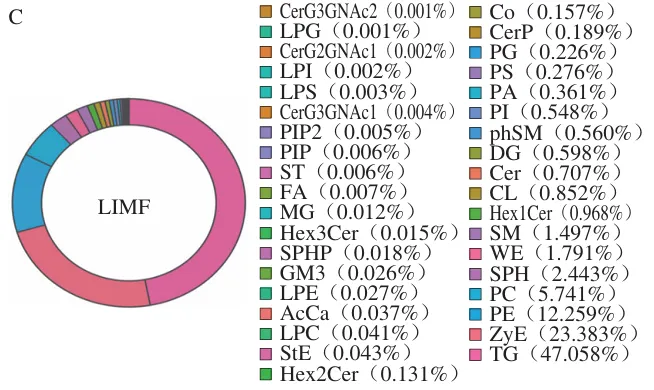
HIMF组和LIMF组在正离子和负离子模式下共鉴定出2 081 种脂质分子,归类为甘油三酯(TG)、甘油二酯(DG)、磷脂酰胆碱(PC)、磷脂酰乙醇胺(PE)、酵母甾醇(ZyE)和磷脂酸(PA)等40 个脂质亚类(图2A)。HIMF组中主要的脂质成分为TG(58.727%)、ZyE(24.494%)、PE(6.84%)、PC(3.266%),LIMF组中主要的脂质成分为TG(47.058%)、ZyE(23.383%)、PE(12.259%)、PC(5.741%)(图2B、C)。HIMF组和LIMF组中TG的含量分别为38 448.36 μg/g和18 363.69 μg/g,DG的含量分别为286.54 μg/g和233.50 μg/g,ZyE的含量分别为16 036.46 μg/g和9 124.92 μg/g,PC的含量分别为2 138.32 μg/g和2 240.35 μg/g,PE的含量分别为4 477.94 μg/g和4 784.13 μg/g(图3)。
 |  |  |

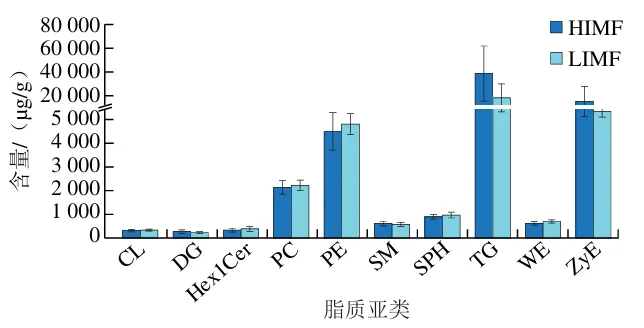 | 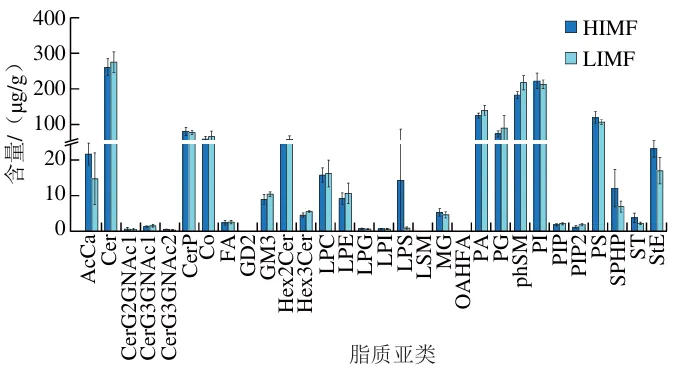 |
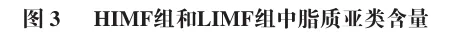
TG作为脂质代谢中的关键成分,是生物体内主要的能量储存形式,它由甘油分子与3 个脂肪酸链结合而成,主要在脂肪组织中积累。两组中TG的占比最高,说明TG是IMF的主要储存形式。Hou Xinhua等的研究表明,与IMF含量较低的约克夏猪肉相比,IMF含量较高的莱芜猪肉中TG含量显著增加,而PC和PE含量则随IMF含量的升高而降低。Fernandez等评估了IMF水平对猪背最长肌脂质组成的影响,发现IMF水平的上升主要是由于TG含量的增加,以及PC和SM含量的相对减少。张志豪等探究了IMF含量分别为3.82%、2.79%的金华猪和杜长大猪肉中脂质差异特征,发现差异脂质中的大部分TG在金华猪肉中上调,而大部分PC和PE则下调。本研究中也有类似发现,HIMF组中TG的含量高于LIMF组,而PC和PE的含量均低于LIMF组。上述现象表明,在高水平IMF条件下,脂肪组织中脂质代谢的方向优先倾向于合成TG,而PC和PE的合成或积累则受到一定抑制。DG是脂质代谢的中间产物,与TG的生物合成和分解密切相关。本研究中HIMF组的DG含量高于LIMF组,较高的DG水平意味着更多的底物被用于合成TG,这与HIMF组中TG含量较高的现象相印证。ZyE作为胆固醇合成途径中的关键中间产物,参与维持细胞膜的流动性和稳定性,对肌肉细胞的正常收缩和舒张至关重要。在猪背最长肌中,ZyE的高占比可能与胆固醇合成的活跃性、细胞膜的特殊需求以及代谢积累等因素密切相关。
03
差异脂质分析
为进一步揭示HIMF组与LIMF组间脂质分子的差异特征,本实验以变量投影重要性(VIP)>1和P<0.05为差异脂质分子筛选标准。如表2所示,共筛选出6 种TG、6 种PE和5 种Hex1Cer等25 种差异脂质分子(上调8 种,下调17 种)。TG类脂质(如TG(16:1_18:1_18:3)、TG(18:1_18:1_18:2)、TG(18:1_18:2_18:3)等)在HIMF组中显著上调,而PA(25:0_18:2)、PC(16:0_20:4)、PE(18:2e_20:1)、PE(18:2e_20:4)、PE(16:1e_18:1)等磷脂类脂质在HIMF组中大多呈现显著下调趋势。HIMF组中TG(16:1_18:1_18:3)、TG(18:1_18:1_18:2)等5 种TG含量显著高于LIMF组。这类TG富含的不饱和脂肪酸链(如18:1、18:2、18:3)是加热过程中脂肪氧化生成酯类、醛类物质的核心前体,其高含量为HIMF组特征风味物质的生成提供了物质基础。
磷脂是细胞膜的重要组成成分,其含量发生变化可能与细胞膜的流动性、信号传导功能以及细胞代谢状态有关。下调的磷脂可能意味着HIMF组背最长肌细胞在细胞膜结构的重塑或代谢调节方面存在差异,例如细胞膜的流动性可能降低,从而影响细胞的物质转运和信号转导功能。此外,Hex1Cer类脂质(如Hex1Cer(d18:1_24:1)、Hex1Cer(t20:0_20:1)、Hex1Cer(t42:1)等)在HIMF组中也显著下调,这可能与细胞内Cer代谢途径的改变有关。Cer在细胞凋亡、细胞周期调控以及细胞应激反应中发挥重要作用,其含量的降低可能反映HIMF组背最长肌细胞在这些生理过程中的代谢状态与LIMF组不同。综上所述,HIMF组与LIMF组在脂质代谢、细胞膜结构和功能以及细胞内信号传导等方面存在差异。这些差异可能与IMF含量密切相关,反映了高IMF含量背最长肌在代谢调节和细胞功能上的独特特征。
04
挥发性风味物质组成分析
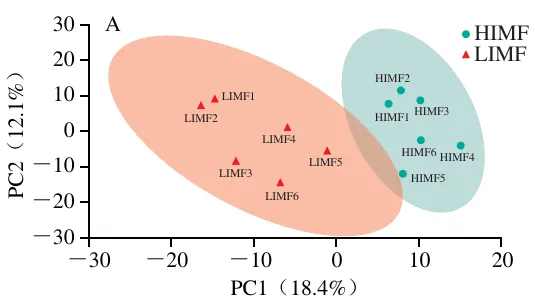
基于无监督模式识别的多元统计分析技术,本研究采用方差归一化处理的PCA模型对HIMF组和LIMF组进行质量控制评估。结果显示,两组样本的代谢轮廓在PC1(18.4%)与PC2(12.1%)构成的二维空间内呈现明显聚类分离特征(图4A)。为增强组间差异解析能力,进一步构建了基于正交信号校正的监督式OPLS-DA模型。OPLS-DA模型( RX2=0.273,RY2=0.998,Q2=0.732)显示,两组间的分离状况良好,表明该模型具备理想的分类可靠性及抗过拟合特性(图4B)。
 | 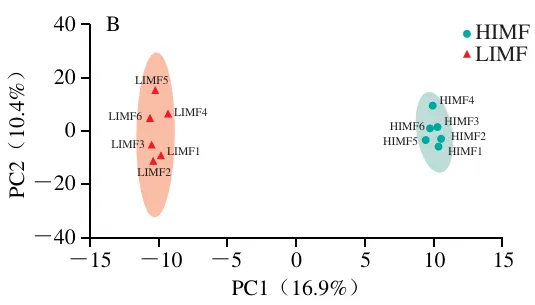 |
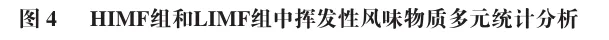
利用GC×GC-TOF MS技术对常压下沸点在50~260 ℃间的各种挥发性物质进行检测,在HIMF组和LIMF组中分别鉴定出1 649 种和1 842 种带有CAS号注释的风味物质。采用PubChem数据库及Classyfire软件对检测风味物质进行种类注释分析,并分析各种类对应风味物质的数目和相对含量。将所鉴定风味物质分为烃类、有机杂环化合物、醇类、苯型化合物、酯类、酮类、杂环化合物、醚类、脂质及类脂分子和羧酸类(风味物质数目排名前10的种类)。HIMF组和LIMF组的风味物质在种类数目和相对含量上呈现出显著差异。在风味物质种类方面,LIMF组在多数种类中的风味物质数目均多于HIMF组,例如烃类、有机杂环化合物、醇类、苯型化合物、酯类、酮类等。然而在相对含量方面,HIMF组的烃类和酯类相对含量较LIMF组分别高53.33%和34.90%,而LIMF组的醇类和有机杂环化合物相对含量较HIMF组高41.00%和43.67%(表3)。结果表明,HIMF组和LIMF组在风味物质组成上存在差异。Zhang Yingying等基于多组学分析研究岔路黑猪4 个部位(背最长肌、斜方肌、腘绳肌和腹胁肉)之间的风味差异,结果显示腘绳肌中大部分风味物质种类的数目均多于其他部位,腘绳肌中风味物质含量丰富且组成复杂。本研究中LIMF组在多数风味物质种类的数目上多于HIMF组,这意味着LIMF组具有更丰富的风味物质组成,可表现出更强的风味多样性和复杂性。在相对含量方面,HIMF组烃类和酯类的相对含量显著高于LIMF组,而醇类和有机杂环化合物的相对含量显著低于LIMF组,表明两组在风味物质的积累和代谢路径上存在差异。

HIMF组和LIMF组中己醛的质量浓度分别为0.302 2 μg/mL和0.186 1 μg/mL;戊醛的质量浓度分别为0.113 7 μg/mL和0.102 0 μg/mL。己醛含量在HIMF组中显著高于LIMF组,其前体为亚油酸(C18:2),HIMF组中富含C18:2的高含量TG提供了充足底物,经氧化裂解后生成更多己醛。戊醛主要由含有C18:2和花生四烯酸(C20:4)的脂质发生过氧化反应生成,尽管LIMF组中含C18:2的TG含量较低,但其含有C20:4的PC、PE含量较高,这两种相反的趋势相互抵消,最终导致两组的戊醛含量无显著差异。
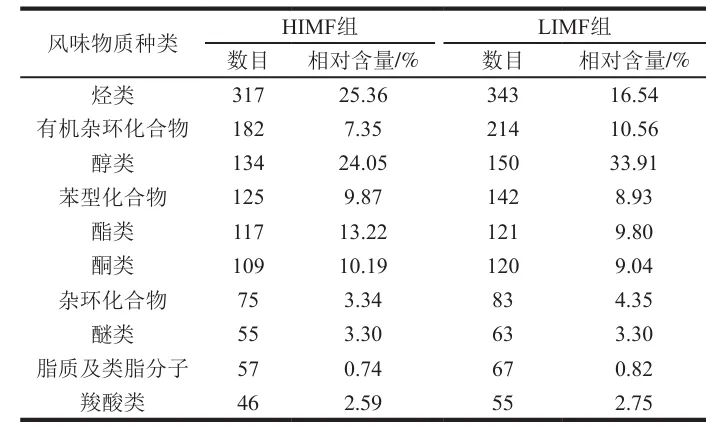
此外,利用FlavorDB数据库分析两组样品中挥发性风味物质的感官特征。如图5所示,HIMF组和LIMF组表现出不同的风味特征。HIMF组表现出较强的甜味、果味、青草味和脂肪味。而LIMF组表现出较强的乙醚味、刺鼻味、酒味、药味、溶剂味和乙醇味,表明两组在风味特征上存在显著差异,推测IMF含量与这些愉悦风味特征呈正相关。Wang Qian等的研究结论进一步支持了这一观点,研究发现与IMF含量为6.28%伯克夏猪相比,IMF含量分别为10.90%和9.06%的宁乡猪和伯宁猪(伯克夏猪×宁乡猪)具有更强烈的甜味、果味和花味等风味特征。
05
主要挥发性风味物质鉴定分析
食品风味的呈现主要取决于风味物质的感觉阈值。相对气味活度值(ROAV)是用于评价混合气味物质中单一组分对整体气味贡献强度的量化指标。ROAV>0的挥发性风味物质为重要香气贡献者,0.1≤ROAV<1的挥发性风味物质对样品总体风味起重要修饰作用,ROAV≥1的挥发性风味物质为样品的关键风味物质。如表4所示,共筛选出2,3-丁二酮、2-壬烯醛、庚醛等8 种ROAV≥1的挥发性风味物质,以及2-乙基己醇和2-十一烷等5 种0.1≤ROAV<1的挥发性风味物质,其中包括醛类7 种、酮类3 种、烃类1 种、醇类1 种、呋喃类1 种。
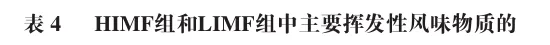
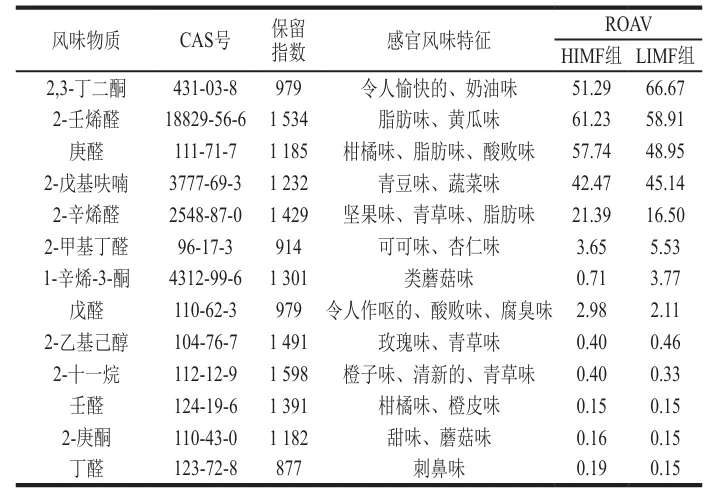
醛类是熟猪肉中的主要挥发性风味物质,其主要来源于脂质的氧化降解及美拉德反应等途径,由于醛类普遍具有较低的感官阈值,即使在微量存在条件下仍能显著贡献青草味和脂肪味等特征风味,因此被确认为肉质风味体系中关键的呈味组分。在肉类烹饪过程中,2-壬烯醛的生成与积累对肉的风味特征具有显著影响,在高浓度时可能呈现油腻味或腥味。在熟肉的风味形成过程中,庚醛的存在对整体风味的复杂性和层次感具有重要影响。在肉类加工或贮藏中,不饱和脂肪酸经氧化降解生成2-辛烯醛,其α,β-不饱和结构赋予其高反应活性与独特气味。在低浓度时,2-辛烯醛呈现脂肪味和坚果味,能够增强肉类的脂香复杂度。2-壬烯醛主要源于油酸(C18:1)的氧化:油酸在脂氧合酶催化下生成9-氢过氧油酸,进一步裂解为2-壬烯醛。庚醛和2-辛烯醛主要来自亚油酸(C18:2)的氧化:亚油酸先形成13-氢过氧亚油酸,裂解后分别生成庚醛和2-辛烯醛。HIMF组中显著上调的TG(18:1_18:1_18:2)、TG(18:1_18:2_18:3)等分子为上述3 种醛类物质的生成提供充足的底物,因此这3 种物质在HIMF组中的ROAV高于LIMF组。猪肉中的酮类是由不饱和脂肪酸或氨基酸的热氧化或降解产生,具有较低阈值,可使猪肉散发出令人愉悦的奶油香味。2,3-丁二酮具有浓郁的奶油味和焦糖味,广泛存在于肉类风味体系中,尤其是在熟肉中,是肉类风味中关键的呈味组分之一。2,3-丁二酮由糖酵解产物丙酮酸经α-乙酰乳酸合成酶生成α-乙酰乳酸,再经非酶氧化脱羧形成;该路径在加热阶段占主导,与脂质氧化无关。因此,其组间差异主要受肌肉内还原糖及肌苷酸等美拉德反应底物调控。1-辛烯-3-酮是一种具有类蘑菇味或青草味的挥发性化合物,常存在于肉类风味体系中。呋喃类主要来自碳水化合物的烯醇化和脱水反应,其阈值较低,一般赋予肉焦糖味。2-戊基呋喃是肉风味中的关键脂质氧化产物,其生成与不饱和脂肪酸氧化及美拉德反应相关。该化合物感官阈值极低,具有青豆味和蔬菜味。2-戊基呋喃在两组中ROAV相近,表明其风味贡献在两组受IMF含量的影响较小。
06
差异挥发性风味物质鉴定分析
为进一步探究HIMF组和LIMF组间的差异挥发性风味物质,以P<0.05、VIP≥1标准筛选差异风味物质。如图6所示,两组中共鉴定出76 种差异挥发性风味物质(上调33 种,下调43 种),包括酯类19 种、有机杂环化合物15 种、烃类13 种、醇类10 种、苯环型化合物5 种、醛类4 种、醚类3 种、酮类2 种、脂质和类脂分子2 种、羧酸及衍生物1 种、萜类1 种、有机卤素化合物1 种。HIMF组中特征性上调风味物质以酯类为主,包括丁酸乙酯、己酸乙酯等,这类物质多贡献果香味,是HIMF组风味更浓郁的主要来源。LIMF组中特征性上调风味物质以烃类、醇类、醛类为主,这些物质多数带有脂肪味,如3-十六烷醇、1-十四烯、十三醛、3-亚甲基十三烷、十五烷等。
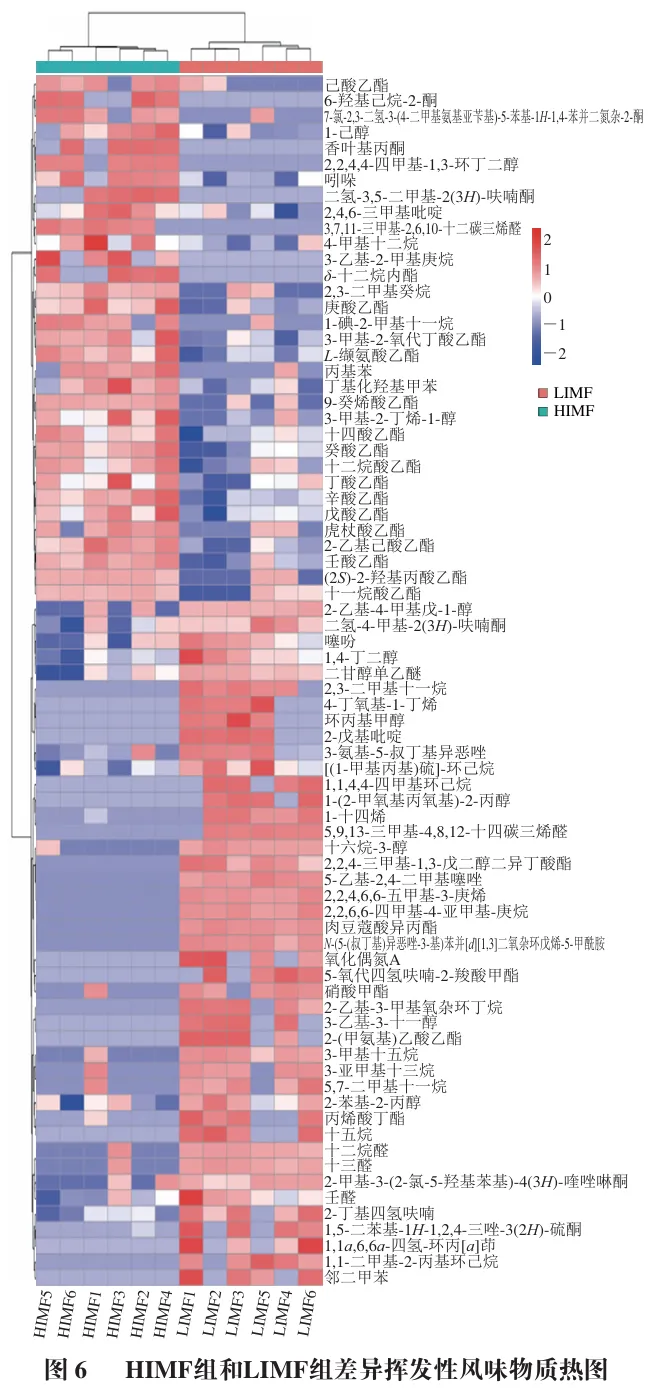
酯类作为天然植物果实、花中广泛存在的一类风味物质,具有奶油味和花果味。在本研究中,大部分酯类在HIMF组中上调(上调15 种,下调4 种)。这一现象表明,HIMF组较高的IMF含量可能促进了酯类化合物的生成或积累,进而增强HIMF组的果香风味。有机杂环化合物是一类分子环状骨架中含杂原子(如氮、氧、硫)的关键挥发性组分,具有低气味阈值和强烈的风味特征,其在烧烤和熏制肉制品加工中产生,过量摄入有诱癌风险。大部分有机杂环化合物在HIMF组中下调(上调5 种,下调10 种),该结果表明IMF含量较高的HIMF组中,这些化合物的生成或积累受到一定程度的抑制。烃类主要由脂质(尤其是多不饱和脂肪酸)氧化降解反应生成,通常饱和烃类物质的感官阈值较高,对肉制品挥发性风味的影响有限。在HIMF组中,大部分烃类呈现下调趋势(上调3 种,下调10 种)。值得注意的是,这些烃类大多属于饱和烃类,由于其气味阈值较高,因此对两组样品的整体风味贡献较小。
07
脂质组学和风味组学联合分析
基于上述脂质组学鉴定的差异脂质与风味组学筛选的特征性差异风味物质,本研究进一步开展两组学数据的关联分析,旨在阐明HIMF组与LIMF组背最长肌风味差异的内在调控机制。结果显示,两组间显著的风味差异主要通过一条调控路径介导,即脂质水解裂解驱动风味生成的直接路径:HIMF组中显著上调的TG类物质在加热初期快速发生水解反应,释放C18:1、C18:2等游离脂肪酸,有效扩充肌肉组织中的游离脂肪酸储备库;这些长链游离脂肪酸在后续高温条件下,经热化学裂解与氧化断裂作用生成丁酸、己酸等FAs,此类FAs可与肌肉内源乙醇发生酯化反应,生成丁酸乙酯、己酸乙酯等酯类,而这类酯类物质是果香风味的核心贡献者,其含量的显著提升直接强化了HIMF组的果香风味特征。而LIMF组因TG含量较低,使该反应路径的效率受限,既减少了特征酯类物质的生成,又使脂肪味相关物质相对富集,最终形成与HIMF组截然不同的风味特征。
此外,为探究脂质与挥发性风味物质之间的相关性,本研究还采用了Pearson相关性法进行分析。基于相关性系数和显著性水平筛选出排名20的挥发性风味物质和脂质(图7)。十一烷酸乙酯和十四酸乙酯与TG(18:1_18:2_18:3)、TG(16:1_18:1_18:3)、TG(18:1_18:1_18:2)、TG(18:1e_19:1_19:1)、TG(18:1e_19:0_19:1)呈较强的正相关,与PC(16:0_20:4)、PA(25:0_18:2)、PE(18:2e_20:1)、PE(16:0p_20:4)、PE(16:1e_18:1)、PE(16:1e_20:2)等呈较强的负相关。

酯类是由短链脂肪酸与脂质氧化过程中产生的醇通过酯化反应生成。短链酯类通常具有水果的甜味,而长链酯类则往往带有油腻感。十一烷酸乙酯在不同处理工艺的速溶红茶中被鉴定为关键挥发性风味物质。十四酸乙酯通常被报道为酒中的特征挥发性风味物质。十一烷酸乙酯和十四酸乙酯与多种TG呈较强的正相关,表明其生成可能与这些TG的氧化密切相关。这种正相关性可能反映了脂质氧化过程中产生的中间体或产物为这两种酯类的合成提供了必要的前体物质。相反,它们与某些磷脂呈较强的负相关,这可能表明这些磷脂的代谢过程与脂质氧化路径存在一定的竞争关系,或者这些磷脂在细胞内的分布和功能限制了这两种酯类的生成。
08
结 论
本研究基于脂质组学和风味组学技术探究了IMF对杜花猪肉的影响。脂质组学分析结果表明,在高水平IMF含量条件下,脂肪组织中脂质代谢的方向优先倾向于合成TG,而PC和PE的合成或积累则受到一定抑制;HIMF组与LIMF组在脂质代谢、细胞膜结构和功能以及细胞内信号传导等方面存在差异;与LIMF组相比,在HIMF组中显著上调TG(16:1_18:1_18:3)、TG(18:1_18:1_18:2)等5 种TG,这为HIMF组特征风味物质的生成提供了物质基础。风味组学分析结果表明,两组在风味物质的积累和代谢路径上存在差异,HIMF组在烃类和酯类的相对含量方面明显高于LIMF组,而LIMF组则具有更丰富的风味物质组成;确定2,3-丁二酮、2-壬烯醛等8 种ROAV≥1的挥发性风味物质是杜花猪肉的关键香气成分;IMF含量可能与甜味、果味等愉悦风味呈正相关。HIMF组特征性上调的风味物质以酯类为主(如丁酸乙酯、己酸乙酯等),主要贡献果香味;LIMF组则以烃类、醇类、醛类为特征性上调风味物质(如3-十六烷醇、1-十四烯、十三醛等),多数带有脂肪味。多组学联合分析结果表明,两组间的风味差异主要通过脂质水解驱动果香风味生成的调控路径介导;十一烷酸乙酯和十四酸乙酯与多种TG呈较强的正相关,其生成可能与这些TG的氧化过程密切相关。
此外,本研究尚存3 点局限:1)样本局限于单一养殖场的杜花猪背最长肌,部位与地域代表性不足;2)脂质-风味关联仅基于组学,缺乏体外氧化模型与关键基因/酶的功能验证;3)ROAV评估未辅以感官与消费者测试。未来应扩大样本来源,比较不同肌肉部位的脂质与风味差异,明确IMF调控肉品质的部位特异性;结合转录组或代谢组解析脂质调控网络,构建体外氧化体系验证脂质前体对风味物质生成的影响,并结合感官评价确立IMF最优阈值,为产业化提供精准方案。
作者简介

黄文艺,华南农业大学食品学院,硕士研究生。

实习编辑:梁雯菁;责任编辑:张睿梅。点击下方阅读原文即可查看全文。图片来源于文章原文及摄图网
近期研究热点





长按或微信扫码进行注册
为系统提升我国食品营养与安全的科技创新策源能力,加速科技成果向现实生产力转化,推动食品产业向绿色化、智能化、高端化转型升级,由北京食品科学研究院、中国食品杂志社《食品科学》杂志(EI收录)、中国食品杂志社《Food Science and Human Wellness》杂志(SCI收录)、中国食品杂志社《Journal of Future Foods》杂志(ESCI收录)主办,合肥工业大学、安徽农业大学、安徽省食品行业协会、安徽大学、合肥大学、合肥师范学院、北京工商大学、中国科技大学附属第一医院临床营养科、安徽粮食工程职业学院、安徽省农科院农产品加工研究所、安徽科技学院、皖西学院、黄山学院、滁州学院、蚌埠学院共同主办的“第六届食品科学与人类健康国际研讨会”,将于 2026年8月15-16日(8月14日全天报到)在中国 安徽 合肥召开。

长按或微信扫码进行注册
会议招商招展
联系人:杨红;电话:010-83152138;手机:13522179918(微信同号)


