合作文章丨中国农业科学院茶叶研究所周利团队揭示褪黑素在茶树农药残留控制中的新作用
- 2026-04-23 03:48:10

英文题目:Defense mechanism of tea plant (Camellia sinensis L.) to tolfenpyrad reveals emerging role of melatonin in pesticide residue control
中文题目:茶树(Camellia sinensis L.)对唑虫酰胺的防御机制揭示了褪黑素在农药残留控制中的新作用
期刊名称:Ecotoxicology and Environmental Safety
影响因子:6.2
作者单位:中国农业科学院茶叶研究所
普奈斯提供服务:植物激素检测
DOI号:https://doi.org/10.1016/j.ecoenv.2025.117916
前言
茶树(Camellia sinensis L.)是世界上最受欢迎的饮料作物之一,具有巨大的经济、健康和文化价值。茶树生长在温暖潮湿的环境中,容易受到病虫害的侵袭,因此农药是植物保护的主要措施。唑虫酰胺是一种具有代表性的吡唑酰胺类杀虫剂,对半翅目、鞘翅目、双翅目和鳞翅目等多种昆虫有效。由于它的高效性和低水溶性,已被注册并广泛应用于茶树。然而,唑虫酰胺虽对茶树害虫高效,但其残留风险及茶树响应机制尚不明确。本研究通过多组学技术(生理、代谢组、转录组和激素分析),解析茶树对唑虫酰胺的防御机制,并验证褪黑素对农药残留的调控作用。
研究路线
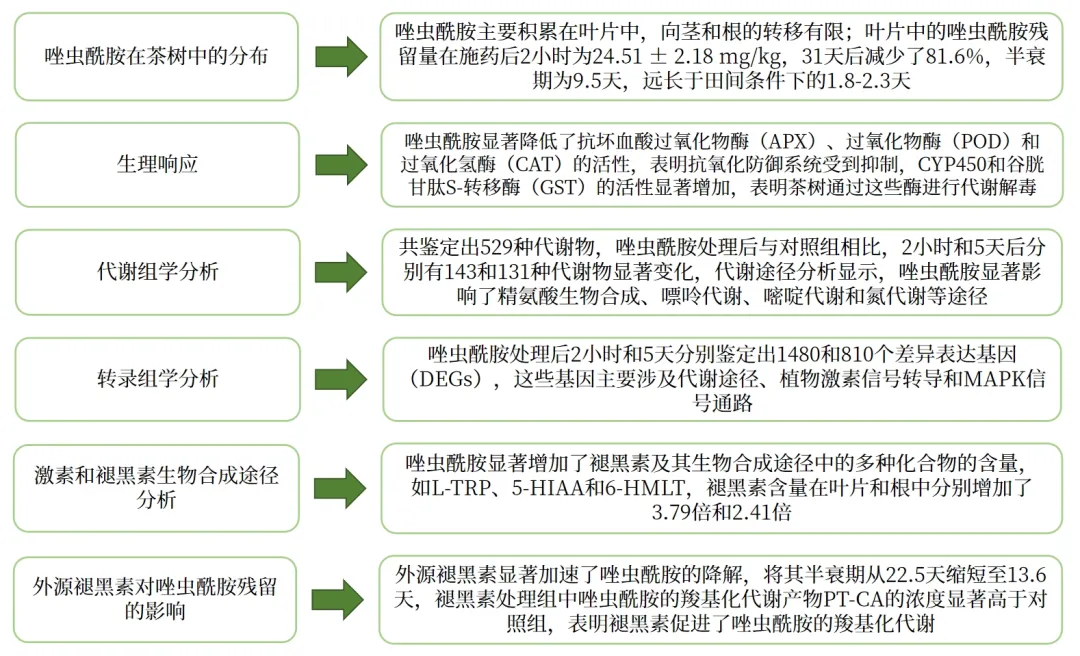
研究结果
01
茶树中唑虫酰胺的消散和分布
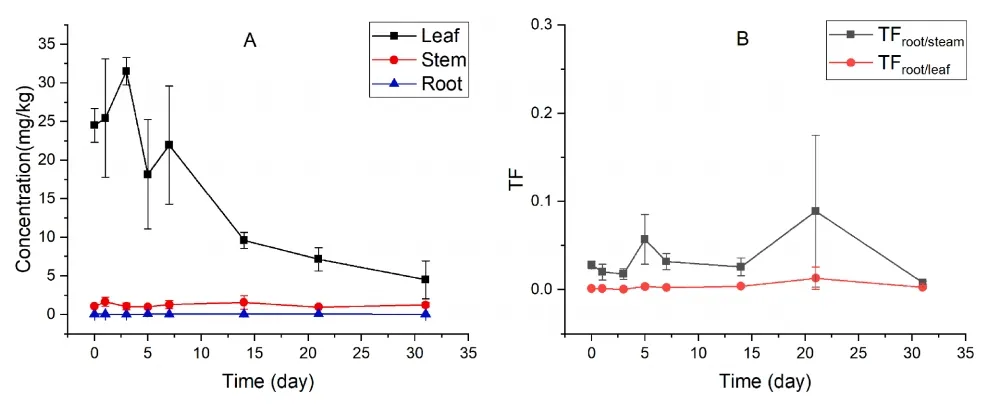
唑虫酰胺喷洒后对植物毒性并不明显。图1A显示了施药后茶树不同组织(根、茎、叶)中唑虫酰胺的动态含量。对照组在实验期间未检测到污染。数据显示,茶叶上的唑虫酰胺的消散遵循一阶动力学,Ct=30.56e-0.073t(R2=0.8299)。叶面喷施2h后,唑虫酰胺在叶片上的初始沉积量为24.51±2.18 mg/kg;在5、14和31天后,茶叶上的唑虫酰胺残留量分别下降了25.9%,60.8%和81.6%。本实验条件下,唑虫酰胺在茶叶上的半衰期(9.5d)比之前在田间条件下的半衰期(1.8d ~ 2.3d)要长得多,这是由于田间条件下生长稀释对唑虫酰胺耗散的贡献大于温室条件。
茎组织中的唑虫酰胺浓度在培养过程中相对稳定(0.96±0.14~1.67±0.59),远低于叶片中的浓度。根组织中的唑虫酰胺浓度最低,5d后上升到0.056±0.027,然后随着时间的推移逐渐下降(图1)。转位因子TFRoot/Stem在0.008±0.002~0.089±0.086之间,而TFRoot/Leaf的范围为0.0006±0.0004~0.013±0.013;两者均小于1,这表明农药从植物的地上部分向地下部分的转移很少,而唑虫酰胺主要积聚在叶片组织中。
02
茶树对唑虫酰胺的生理反应
施用唑虫酰胺后,叶片样本中的抗坏血酸过氧化物酶(APX)、过氧化物酶(POD)和过氧化氢酶(CAT)活性明显降低。如图2所示,与对照组相比,施用唑虫酰胺明显降低了CAT的活性,效应大小为1.56(Cohen's d);平均差异的95%置信区间为24.7-765.7。APX的Cohen's d值为3.15(Δave的95%置信区间为0.27-0.82),POD的Cohen's d值为3.20(Δave的95%置信区间为53.4-158.6),由此可见,APX和POD活性的降低程度高于CAT活性。即使在施用唑虫酰胺后的第5天,APX和CAT活性仍然显著降低,其Cohen's d值分别为3.14(Δave的95%CI,0.23-0.70)和1.73(Δave的95%CI,62.8-733.3)。SOD活性没有明显变化。
在代谢解毒方面,与对照组相比,施用唑虫酰胺2小时后茶叶中CYP450s总含量和谷胱甘肽S-转移酶(GST)活性显著升高,Cohen's d值分别为1.50(95%CI的Δave,8.9-115.9)和2.2(95%CI的Δave,0.0042-0.033)。此外,在施用杀虫剂后的第5天观察到了更大的效应大小,CYP450s的Cohen's d值为1.94(Δave的95% CI为27.5-135.7),GST的Cohen's d值为3.0(Δave的95% CI为0.0084-0.032)。CYP450s总量的增加表明它们参与了唑虫酰胺的第一阶段代谢。GST通过将谷胱甘肽(GSH)与农药共轭,在植物体内的农药解毒过程中发挥着重要作用,而诱导的GST活性表明,抗坏血酸-谷胱甘肽循环被激活,以应对唑虫酰胺引发的氧化损伤。
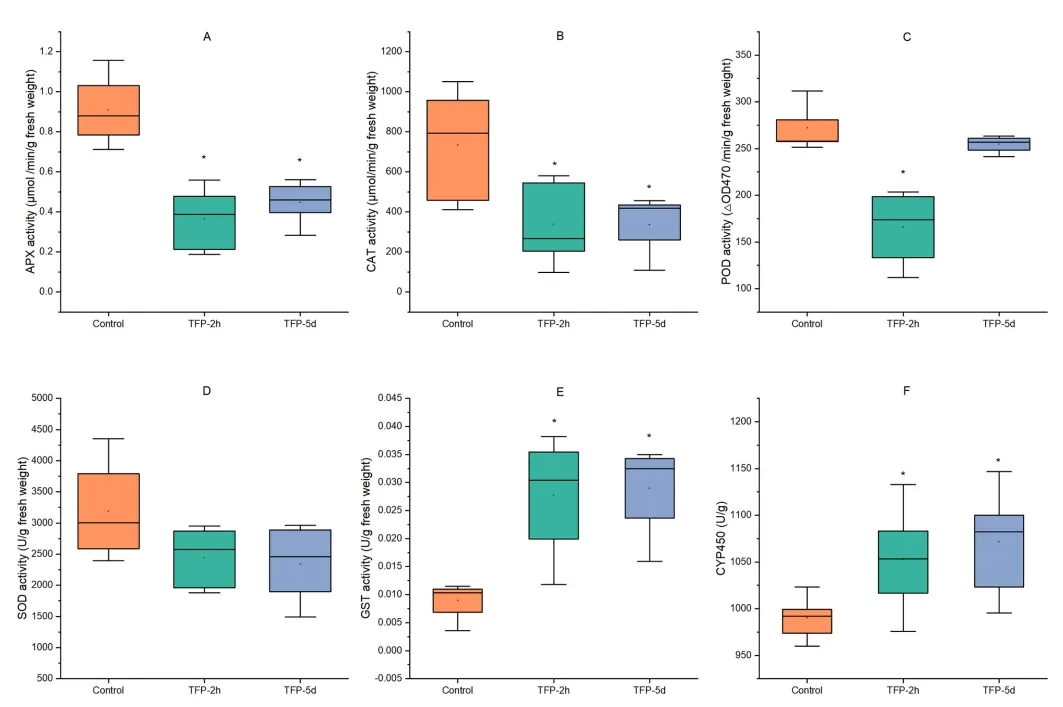
图2.唑虫酰胺对茶叶中抗氧化防御酶的影响。施用唑虫酰胺组(施用后2小时和5天)与对照组之间的显著差异用星号表示(*p<0.05)。
03
对唑虫酰胺的代谢反应
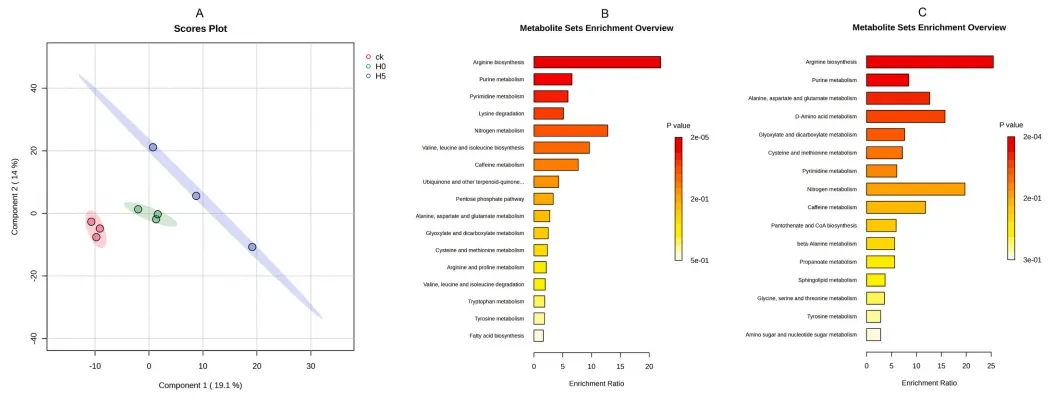
本研究采用超高效液相色谱/气相色谱-质谱联用平台进行非靶向代谢组学分析,以增强代谢物检测的覆盖率。共鉴定或推测注释了529个代谢物。然后使用MetaboAnalyst 4.0软件分析代谢组学数据,进行VIP(变量重要性投影)和代谢途径分析。如图3A所示,偏最小二乘判别分析(PLS-DA)表明,经唑虫酰胺处理的植株与对照植株明显分离,表明接触唑虫酰胺对茶树代谢产生了显著影响。PLS-DA中的VIP值>1和t检验中的FDR(错误发现率)值<0.05可用于识别显著不同的代谢物。富集分析表明,施用唑虫酰胺2小时后,精氨酸生物合成、嘌呤代谢和嘧啶代谢的3条代谢途径受到显著影响(P<0.05,富集倍数>2),而在施用唑虫酰胺后的第5天,有8条代谢途径受到明显影响(精氨酸生物合成、嘌呤代谢、丙氨酸、天门冬氨酸和谷氨酸代谢、D-氨基酸代谢、乙醛酸和二羧酸代谢、半胱氨酸和蛋氨酸代谢、嘧啶代谢和氮代谢)。因此,唑虫酰胺可能会严重破坏氨基酸的生物合成、嘌呤代谢和碳水化合物代谢(图3B-C)。
04
褪黑素通路对唑虫酰胺的激活反应
植物激素在复杂的调控机制下对抗不利影响,从而使植物在胁迫条件下生存。为了了解唑虫酰胺对茶树中植物激素的影响,在水培条件下分析了叶和根样本中 IAA、ABA、CK、JA、SA、GA、BR和MT的含量。如图4A-B所示,暴露于唑虫酰胺后,每种植物激素在叶和根组织中的含量普遍增加。特别是唑虫酰胺(1mg/L有效成分)显著提高了叶和根组织中的褪黑素水平,效应大小分别为3.79(95%置信区间Δave为1.26-2.56)和2.41(95%置信区间 Δave为1.35-4.44)。为了进一步确定褪黑素在唑虫酰胺防御反应中的作用,我们在LC-MS/MS平台上以多反应监测(MRM)模式检测了参与褪黑素生物合成途径的化合物的积累,包括 L-色氨酸(L-TRP)、色胺(TRM)、5-羟色氨酸(5-HTP)、血清素(SER)、N-乙酰血清素(NAS)、5-羟吲哚乙酸(5-HIAA)和 6-羟褪黑素(6-HMLT)(图4C)。结果表明,在1和8mg/L的剂量下,唑虫酰胺显著增加了褪黑素(MT)、L-色氨酸(L-TRP)、5-羟色胺(5-HIAA)和 6-羟基褪黑素(6-HMLT)的含量,同时在8mg/L的剂量下还显著增加了5-羟色胺(5-HTP)和色氨酸脱羧酶抑制剂(SER)的含量。然而,在唑虫酰胺的应用下,褪黑素的两个中间产物——褪黑素代谢产物(TRM)和神经元活性抑制剂(NAS)的含量则有所下降。褪黑素通路对唑虫酰胺反应的上调表明,褪黑激素可能是参与农药防御和代谢反应的调节因子之一。
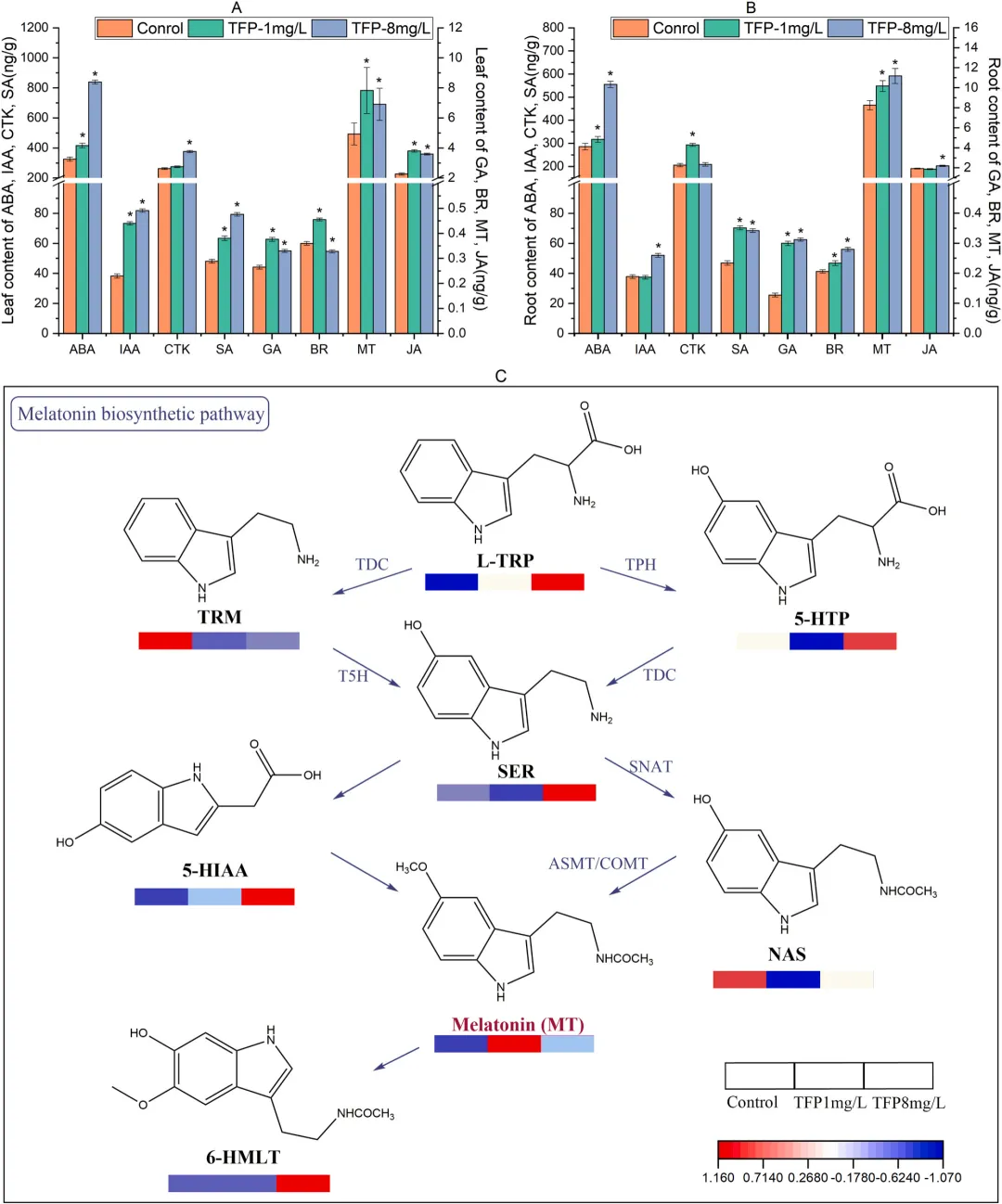
图4. 施用唑虫酰胺后茶叶(A)和根(B)中植物激素的含量。星号表示差异显著(*p<0.05)。施用唑虫酰胺后褪黑素生物合成途径相关代谢物的热图(C)。
讨论与总结



END
推 荐 阅 读
2、液相色谱方法开发与验证
3、文献分享丨长江大学与中国农业科学院团队共同揭示施用有机硒改善杂交水稻的光合特性、产量和品质的机制



