文献分享丨山东农业大学李媛媛团队解析氮素对苹果重要外在品质—表皮蜡质的调控机制
- 2026-04-23 21:12:00

英文题目:MdBT2 regulates nitrogen-mediated cuticular wax biosynthesis via a MdMYB106-MdCER2L1 signalling pathway in apple
中文题目:MdBT2通过MdMYB106-MdCER2L1信号通路调控苹果中氮介导的蜡质生物合成
期刊名称:Nature Plants
影响因子:15.8
作者单位:山东农业大学
DOI:https://dx.doi.org/10.1038/s41477-023-01587-7
研究背景
研究路线
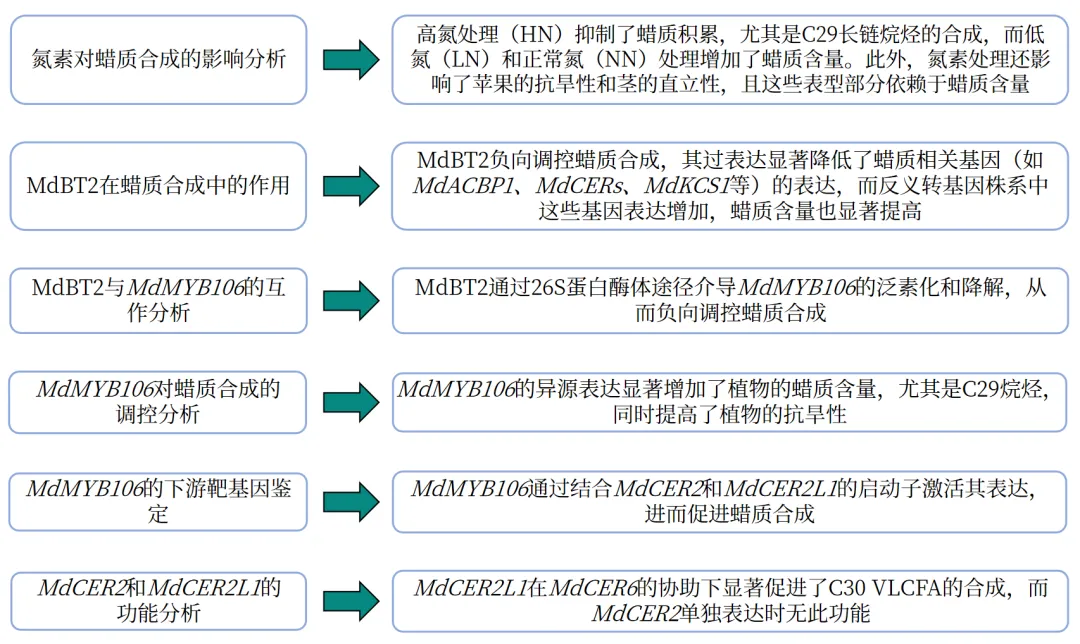
研究结果
01
N负向调控蜡质生物合成
之前研究表明氮水平与蜡质生物合成呈负相关。为了进一步验证氮肥对蜡质含量的负面影响,对8年生的‘Gala/M26/Hanlus hupehensis’树分别用低氮LN、正常氮NN和高氮HN处理1年。果实成熟后摘取叶片和果实进行蜡质含量分析和扫描电镜观察。果实滴水试验表明,LN和NN处理下苹果果皮表面的水滴黏附力更强,说明LN和NN处理下果皮表面的疏水性比HN处理强(图1a-c)。这个结果说明随着氮肥施用量的增加,蜡质含量逐渐降低。用SEM分析了不同氮处理后的苹果叶片蜡质,结果表明HN处理抑制了蜡质的形成(图1f)。对处理后的叶片和果实中的总蜡质进行了提取,结果表明,LN和NN处理下的总蜡质含量高于HN处理(图1d,g)。采用气相色谱-质谱法(GC-MS)对蜡质组分进行了定量分析,发现NN和HN处理之间的差异:LN处理下C29长链烷烃含量最高,HN处理下C27长链烷烃含量较高(图1e,h)。这一结果表明N对C27-C31烷烃的影响最为显著;过量施氮导致苹果中C27含量升高,但未能改变以C29为主的烷烃含量。
为了验证N对苹果抗旱性和茎直立度的影响是否完全或部分取决于蜡质含量的变化,在自然条件下对湖北海棠(一种苹果品种)的砧木施加LN(0.1mM)、NN(1mM)和HN(10mM)处理。同时,在LN处理中使用乙草胺(一种已报道的蜡质合成抑制剂),在HN处理中使用VLCFAs混合物,以更好地阐明蜡质在此过程中的作用。结果表明,在干旱处理下,HN处理的植物长势较差,而LN和NN处理的植物长势较好。添加乙草胺后,干旱条件下LN处理的植物比单独LN处理的植物更弱。同时,与单独HN处理相比,添加VLCFAs的HN植物较弱的表型得到部分恢复。结果表明,LN处理可以提高苹果的抗旱性,并且N对植物抗旱性的影响部分取决于蜡质(图1i)。此外,茎直立性测定表明,随着N浓度的增加,茎弯曲的角度逐渐增加,在HN处理中观察到最大程度的弯曲;施用VLCFA后,弯曲得到恢复。这一结果同样表明,N影响的茎弯曲部分依赖于蜡质(图1j-l)。总之,这些结果表明基于N的表型至少部分依赖于蜡质积累。
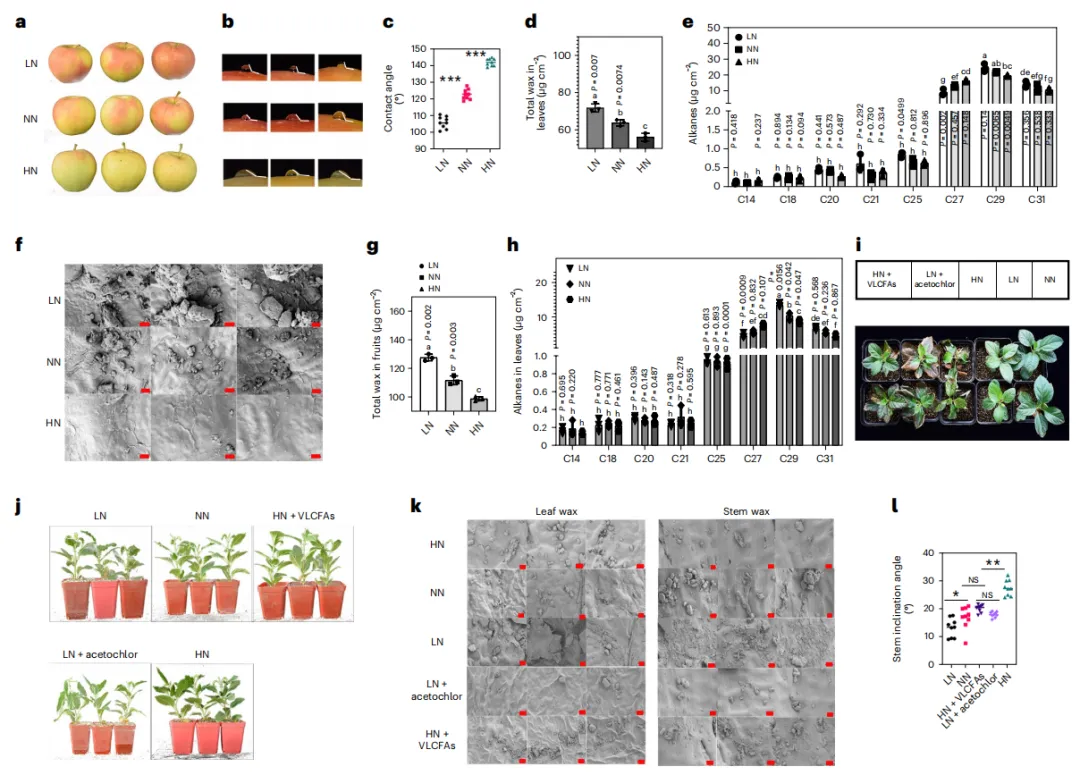
图1.N负向调控苹果蜡质的积累。(a)用HN、NN和LN浓度处理的苹果果实表型。(b,c)用不同N浓度处理的水果表面与水滴之间的接触角的照片(b)和测量值(c)。(d,e)用不同N浓度处理的果实的总蜡负荷(d)和烷烃(e)。(f)用不同N浓度处理的叶片蜡质晶体的SEM图像。Bar,2μm。(g,h)用不同N浓度处理的叶片的总蜡负荷(g)和烷烃(h)。(i)HN、NN、LN、LN与乙草胺以及HN与VLCFA混合物处理对苹果幼苗干旱程度的影响。(j)HN、NN、LN、LN与乙草胺以及HN与VLCFA混合物处理对苹果幼苗直立程度的影响。(k)HN、NN、LN、含乙草胺的LN和含VLCFA混合物的HN处理的叶片和茎蜡质晶体的SEM图像。Bar,10μm。(l)茎倾斜角的定量统计。*表示通过Student’s t检验(双侧)评估的显著差异。***P<0.001;**P<0.01;*P<0.05;NS,不显著。对于条形图,通过单因素方差分析(使用Tukey检验)评估,不同字母表示具有显著差异(P<0.01)。
02
MdBT2通过MdMYB106负向调控蜡生物合成
先前的研究表明,BTB支架蛋白MdBT2对N信号有响应(图2a)。因此,我们研究了其潜在机制,以确定N诱导的蜡质积累是否与MdBT2活性有潜在联系。使用MdBT2反义转基因苹果(antiMdBT2)叶片和果实分析蜡质的形态、晶体、含量和成分。SEM结果表明,GL3(野生型(WT))和转基因苹果叶片中的蜡质形态相似,但antiMdBT2转基因株系中的晶体数量明显高于GL3(图2b)。MdBT2抑制增加了苹果叶片和果实中的总蜡质含量(图2c-e)。随后,通过GC-MS进一步分析了蜡质成分。与GL3相比,antiMdBT2叶片和果实中大多数烷烃是主要增加的成分(图2c、e)。还分析了抗MdBT2、MdBT2过表达(MdBT2-OE)和GL3苹果幼苗叶片中的蜡质晶体、含量和成分以及相关基因表达,结果表明,MdBT2可以通过调节蜡质相关基因来负向调节苹果蜡质含量。
为了研究蜡质的形成,我们进行了酵母双杂交(Y2H)筛选,以鉴定MdBT2相互作用蛋白。几种蛋白被鉴定为MdBT2的下游蛋白,包括R2R3-MYB MdMYB106。此外,还进行了蛋白质印迹分析,并使用抗HA(流感血凝素表位)和抗MYC(v-myc骨髓增生性疾病病毒致癌基因)抗体检测了不同酵母菌株中的蛋白质水平(图2f)。结果显示全长MdBT2和全长MdMYB106之间存在强相互作用。然而,在MdBT2和MdMYB106中的调节和催化结构域之间没有观察到相互作用,这表明这两个序列的所有结构域对于MdMYB106–MdBT2相互作用都是必需的。利用免疫共沉淀(Co-IP)、体外下拉试验(pull-down试验)和双分子荧光互补(BiFC)试验进一步研究了相互作用。Co-IP试验表明MdMYB106和MdBT2在体内发生了相互作用,pull-down试验显示MdMYB106-His与抗His抗体有明显的结合,而BiFC试验表明MdMYB106和MdBT2的相互作用发生在细胞核中(图2g-i)。
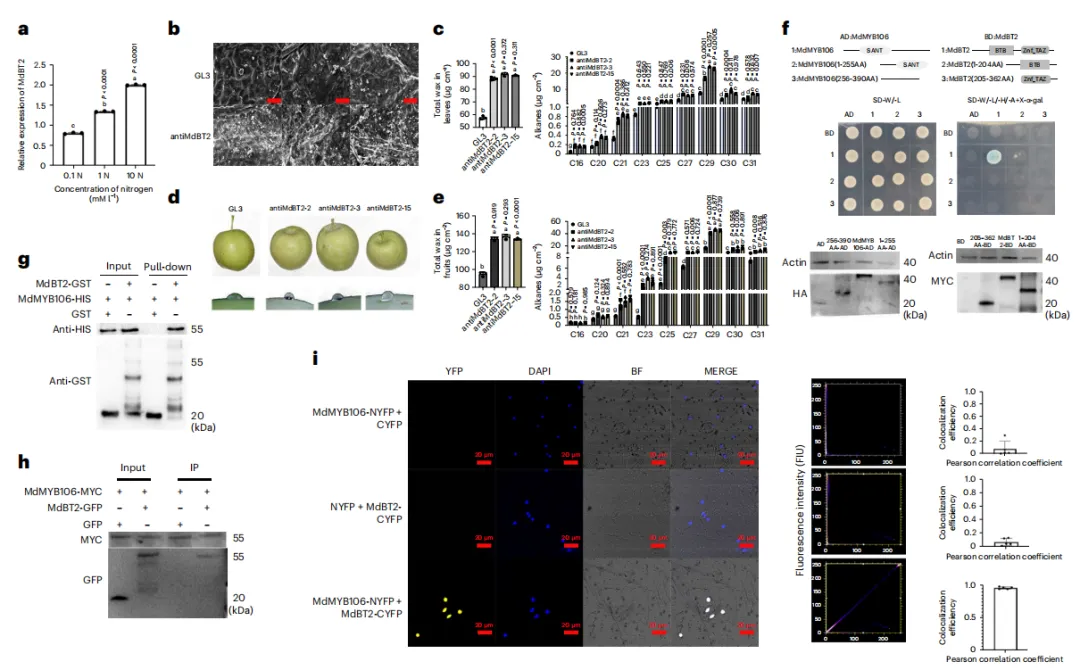
图2.MdBT2在体内和体外通过与MdMYB106相互作用对蜡质生物合成产生负面影响。(a)不同氮供应下MdBT2的相对表达水平。(b)GL3和antiMdBT2叶片蜡质晶体的SEM图像。Bar,50μm。(c)GL3和antiMdBT2叶片的总蜡负荷和烷烃。(d)GL3和antiMdBT2果实的水滴分析。(e)GL3和antiMdBT2果实的总蜡负荷和烷烃。(f)分段Y2H分析以验证MdBT2和MdMYB106之间的相互作用,并采用蛋白质印迹分析来验证每个菌株中的蛋白质表达。(g)体外用MdBT2-GST和MdMYB106-His进行下拉实验。(h)体内Co-IP试验验证MdBT2和MdMYB106与Anti-GFP和Anti-MYC抗体之间的相互作用。(i)体内BiFC试验测试MdMYB106与MdBT2之间的相互作用。然后,使用4′,6-二脒基-2-苯基吲哚(DAPI)作为核标记。YFP,黄色荧光蛋白;BF,明场;MERGE,YFP、DAPI和BF的合并视图。(f-h)中的实验至少独立重复了三次,结果相似。对于条形图,通过单因素方差分析(使用Tukey检验)评估,不同字母表示具有显著差异(P<0.01)。
03
N通过MdBT2-MdMYB106调节蜡含量
我们利用病毒诱导的基因沉默方法测试了MdBT2和MdMYB106在调节蜡质积累中的作用。表型结果表明MdBT2是花青素积累的负调节剂(图3a)。总蜡质含量和水滴分析表明,MdBT2-IL60 + MdMYB106-TRV果实的总蜡质含量最低,水滴与果实表面的接触角最大。相反,antiMdBT2-TRV + MdMYB106-IL60果实的总蜡质含量最高,接触角最小(图3b-d)。C27、C29和C31烷烃是antiMdBT2-TRV + MdMYB106-IL60果实中增加最明显的组分(图3e),与antiMdBT2转基因苹果叶片的结果一致(图2e)。
为了明确N是否通过降低MdMYB106蛋白水平对蜡质合成产生负向调控作用,首先在用HN(10N)、NN(1N)和LN(0.1N)处理的叶片中测量了MdMYB106基因的表达情况,结果表明,MdMYB106基因表达随N浓度的增加而降低,表明N在转录水平上影响MdMYB106(图4a)。因此,为了排除N对基因表达的影响,用不同N浓度处理35S::MdMYB106-MYC过表达苹果愈伤组织,在LN、NN和HN下均未发现MdMYB106表达水平的显著变化(图4b)。随后,用抗MYC抗体检测MdMYB106蛋白水平,发现MdMYB106蛋白水平随着N浓度的增加而显著降低,这表明N也通过降低MdMYB106蛋白水平负向调节蜡质合成(图 4c)。为了进一步明确该过程是否依赖于MdBT2,进行了无细胞降解试验以研究MdBT2和MdMYB106在蛋白质水平上的关系。抗His抗体的蛋白质印迹表明,MdBT2-Anti提取物中的MdMYB106蛋白水平降解速度远低于对照和MdBT2-OX提取物。然而,当添加苄氧羰基-l-亮氨酰-l-亮氨酰-l-亮氨醛(MG132)时,三种混合物中的MdMYB106降解率较低,这表明MdBT2通过26S蛋白酶体途径促进MdMYB106的降解(图4d、e)。
为进一步验证MdBT2参与了MdMYB106的泛素化修饰,我们进行了半体内和体内泛素化实验。半体内实验表明MdBT2参与了MdMYB106的泛素化修饰(图4f)。体内泛素化实验结果表明MdBT2可以通过26S蛋白酶途径介导MdMYB106的泛素化和降解(图4g)。这些结果表明N通过MdBT2介导MdMYB106的稳定性,从而负向调节蜡质积累。
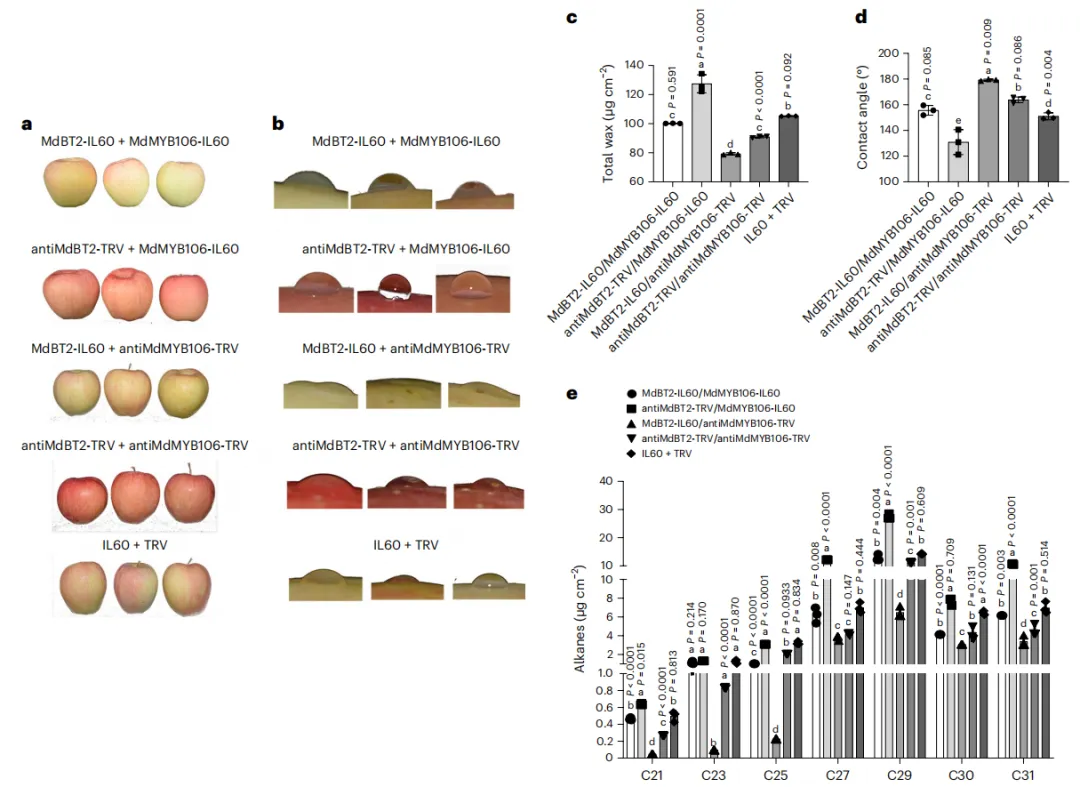
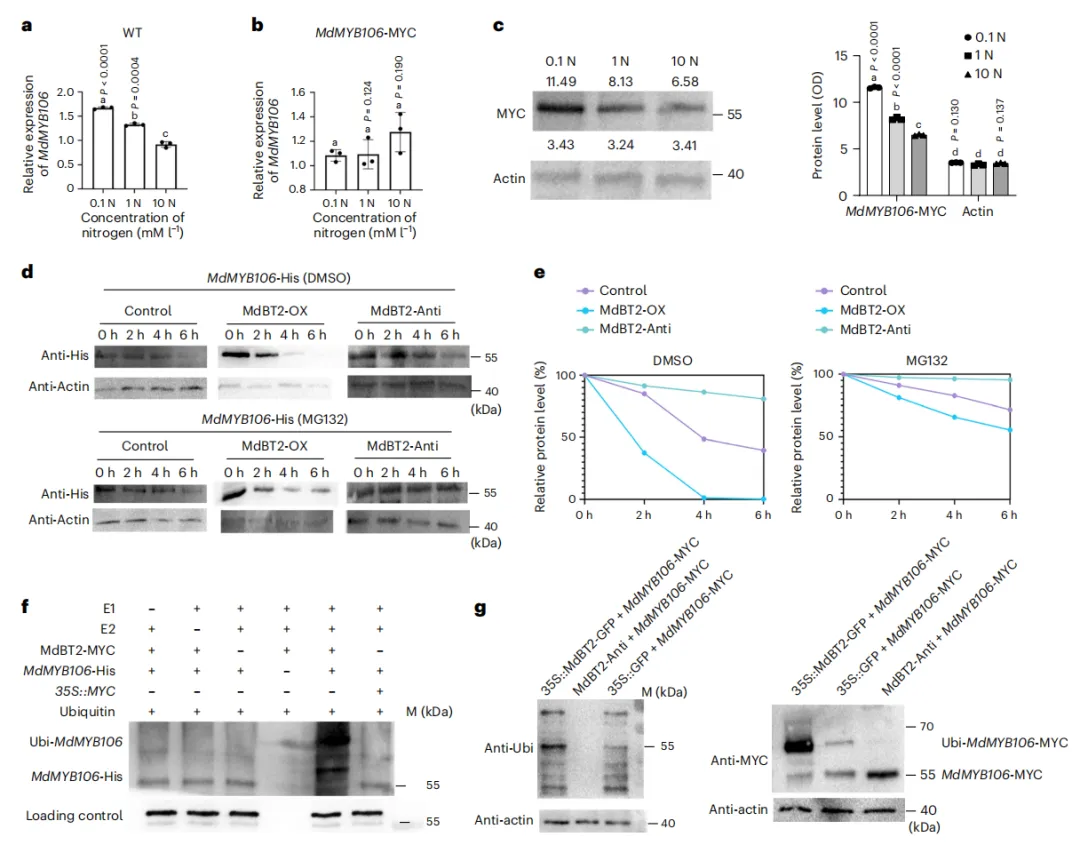
图4.MdBT2通过26S蛋白酶体途径介导MdMYB106的泛素化和降解。(a)不同氮浓度下WT中MdMYB106的相对表达水平。(b)不同氮浓度下35S::MdMYB106-MYC的相对表达水平。(c)N处理下MdMYB106的蛋白质水平。(d)转基因苹果愈伤组织蛋白提取物中MdMYB106-His蛋白的无细胞降解测定。将从MdBT2-OX(过表达)、对照和MdBT2-Anti愈伤组织中提取的蛋白质与MdMYB106-His蛋白孵育指定时间。用抗His抗体检测MdMYB106的水平。(e,d)中MdMYB106蛋白水平的量化。(f)半体内分析显示MdBT2参与了MdMYB106的泛素化。从35S::MdBT2-MYC和35S::MYC苹果愈伤组织中提取总蛋白,并将100μg兔E1、100ng人E2、1 ng泛素和MdMYB106-His添加到蛋白提取物中。用抗His抗体检测混合物。g,使用抗MYC抗体和抗Ubi抗体进行体内泛素化试验,以检测MdBT2介导的MdMYB106蛋白泛素化。c、d、f和g中的实验至少独立重复三次,结果相似。对于条形图,通过单因素方差分析(使用Tukey检验)评估,不同字母表示具有显著差异(P<0.01)。
讨论与总结
Han,J.,et al(2024).MdBT2 regulates nitrogen-mediated cuticular wax biosynthesis via aMdMYB106-MdCER2L1 signalling pathway in apple.Nature Plants.https://doi.org/10.1038/s41477-023-01587-7

END
推 荐 阅 读
2、同心聚力·蛇转乾坤!普奈斯检测2025年年会盛典暨团建圆满落幕
3、合作文章丨中科院武汉植物园杨美团队揭示莲子长寿的内在分子机制

