2.1 实验材料、胁迫处理与生理表型分析
本研究以耐寒的软枣猕猴桃(Actinidia arguta)和不耐寒的中华猕猴桃(Actinidia chinensis)为核心材料,通过农杆菌介导法构建了一系列过表达及关键位点突变的转基因中华猕猴桃株系。为探究基因功能,对野生型及转基因植株进行了严格控制的冷冻胁迫处理(4°C预处理后,阶梯降温至-4°C并复苏)。处理前后,通过测定离子外渗率、丙二醛(MDA)含量等生理指标来评估植株的抗寒表型。同时,利用扫描电子显微镜(SEM)直观比较了叶片表面蜡质晶体的形态与密度,并通过气相色谱-质谱联用技术(GC-MS)精确定量了角质层蜡质的总量及其组分变化,旨在从宏观到微观层面系统评价基因功能对植株抗寒性和蜡质合成的影响。
2.2 基因功能、表达模式与转录调控验证
为揭示核心基因的分子功能,首先通过实时荧光定量PCR(RT-qPCR)技术,分析了目标基因(如AaMYB31s、AaKCSs)在不同胁迫条件和组织中的表达模式。利用GFP融合蛋白,在烟草(Nicotiana benthamiana)叶片中进行了亚细胞定位实验,明确了AaMYB31s等蛋白的核定位特性。为验证AaMYB31s对下游蜡质合成基因(AaKCSs)的直接转录调控关系,采用了一套完整的分子生物学验证体系:通过双荧光素酶报告基因(DLR)实验在体内证明其转录激活活性;利用酵母单杂交(Y1H)实验证实了蛋白与目标基因启动子区域的直接结合;最后通过电泳迁移率变动分析(EMSA)在体外进一步确认了蛋白与启动子特定DNA序列的物理结合。
2.3 蛋白质相互作用与翻译后修饰机制探究
为深入探究AaMYB31s蛋白的上游调控网络,采用多种技术手段验证了其与SUMO E3连接酶AaSIZ1的相互作用,包括酵母双杂交(Y2H)、荧光素酶互补成像(LCI)、免疫共沉淀(Co-IP)以及体外Pull-down实验,从多个维度证实了二者在体内和体外的物理互作。在此基础上,通过体外重构SUMO化修饰体系及在原生质体和烟草中的体内实验,证明了AaSIZ1能够介导AaMYB31s的SUMO化修饰,并确定了关键的修饰位点(K76)。最后,结合蛋白酶体抑制剂(MG132)处理,设计了体内和体外的蛋白质降解实验,结果表明AaSIZ1介导的SUMO化能显著增强AaMYB31s的蛋白稳定性,揭示了其翻译后修饰调控的核心机制。
3.1 冷胁迫诱导软枣猕猴桃的蜡质合成
基因表达上调:通过对冷处理的软枣猕猴桃‘龙城2号’转录组数据进行分析,发现21个与蜡质合成相关的差异表达基因中,有16个受冷胁迫诱导表达上调。
表达模式验证:qRT-PCR结果证实,AaKCS6.1/6.2、AaKAS1.1/1.3/1.4、AaKCS4.2/4.3、AaKCS19、AaKCS2、AaKCS1、AaKCS11.1/11.2/11.3/11.4、AaKCS3.2和AaCER3等基因的表达水平均在冷胁迫下显著增加,并分别在3小时、12小时和24小时达到表达峰值。
蜡质积累增加:扫描电镜(SEM)观察显示,随着冷胁迫时间的延长,叶片表面的表皮蜡质晶体数量显著增多,形态由颗粒状逐渐转变为片状。气相色谱-火焰离子化检测(GC-FID)结果表明,叶片总蜡质含量在48小时内迅速增加。
基于转录组分析,发现多个蜡质合成相关基因在软枣猕猴桃中受冷胁迫诱导而上调。qRT-PCR进一步验证了这一结果,显示AaKCSs、AaKASs和AaCER3等基因的表达水平在冷胁迫下显著增加,并呈现出不同的表达峰值。与基因表达的变化一致,通过扫描电镜(SEM)观察到叶片表面的蜡质晶体密度随冷胁迫时间的延长而显著增加,其形态也从颗粒状转变为片状。气相色谱-火焰离子化检测(GC-FID)进一步证实,叶片总蜡质含量在冷胁迫处理的48小时内快速提升。这些结果共同表明,冷胁迫能够有效诱导软枣猕猴桃的蜡质合成 (Fig. 1)。在这些基因中,AaKCS6.1和AaKCS2的上调最为显著,因此被选为后续功能研究的主要目标。为验证其功能,构建了AaKCS2-OE和AaKCS6.1-OE转基因中华猕猴桃。结果显示,与野生型(WT)相比,转基因植株无论在正常还是冷胁迫条件下,其叶片总蜡质含量和表皮蜡质晶体密度均显著更高,这表明软枣猕猴桃在冷胁迫下的蜡质积累确实与蜡质合成基因的上调直接相关 (Fig. 2A, B)。进一步研究发现,增加蜡质合成能够显著提升植物的抗冻性。表型分析显示,AaKCS2-OE和AaKCS6.1-OE转基因植株表现出更强的抗冻能力。与表型一致,在冷冻胁迫后,转基因植株的离子外渗率、丙二醛(MDA)含量、H₂O₂含量和O₂·⁻含量均显著低于野生型,而叶绿素含量则显著高于野生型。这些结果证明,过表达AaKCS2和AaKCS6.1所导致的蜡质合成增加,显著提高了猕猴桃的抗冻胁迫耐受性,从而揭示了冷胁迫诱导的蜡质生物合成是增强猕猴桃抗冻性的重要机制 (Fig. 2C-F)。
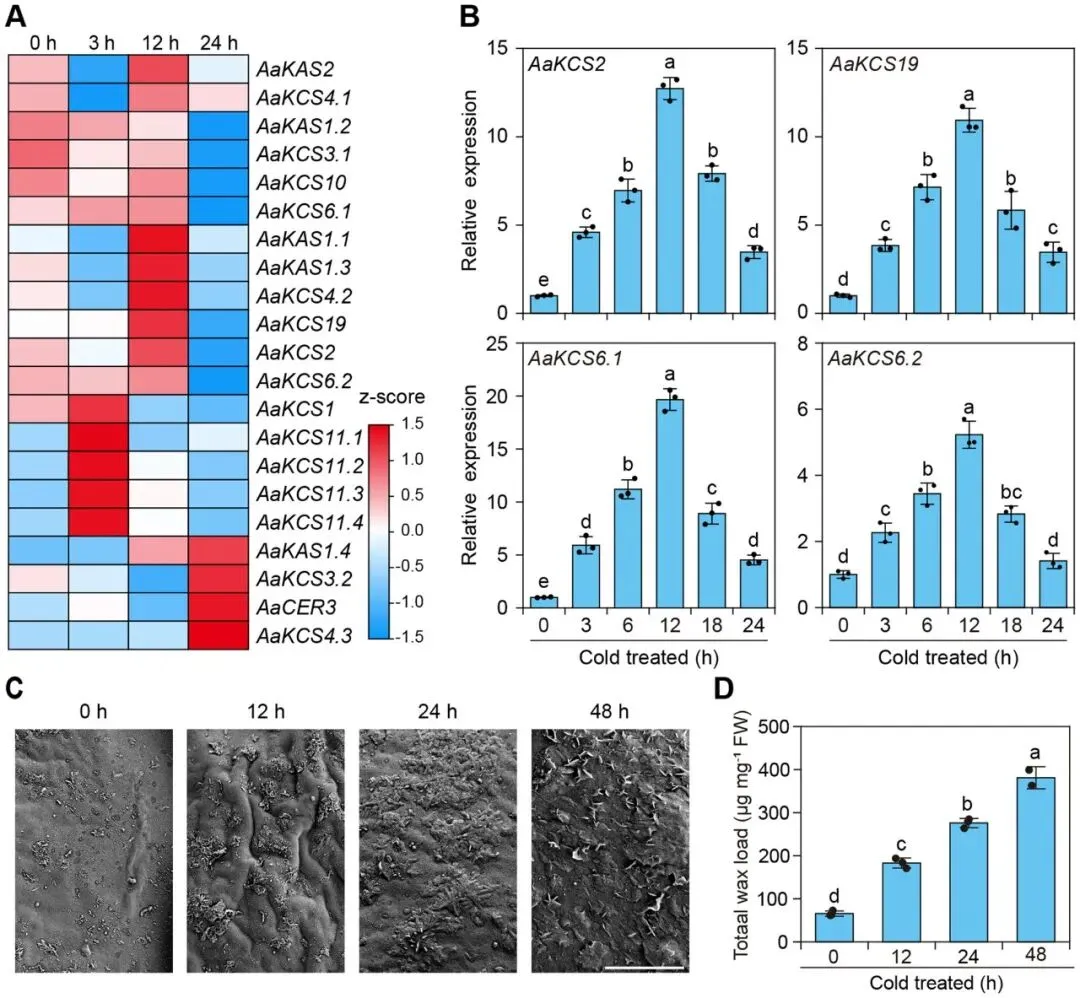
图1. 冷胁迫诱导软枣猕猴桃的蜡质合成(A) 热图展示了软枣猕猴桃单个单倍型中属于蜡质合成相关基因的差异表达基因(DEGs)。热图使用TBtools绘制,并启用了“行缩放”和“行聚类”功能。颜色梯度从蓝色到红色代表标准化的表达水平,蓝色表示低表达,红色表示高表达。(B) 在冷胁迫下,软枣猕猴桃叶片中AaKCS2、AaKCS19、AaKCS6.1和AaKCS6.2的表达模式。将7周龄的野生型(WT)软枣猕猴桃植株置于4°C进行48小时的冷胁迫处理。在指定时间点采集叶片用于qRT-qPCR分析。ACTIN8用作内参。 (C) 野生型软枣猕猴桃植株叶片表面蜡质晶体的扫描电镜(SEM)图像。此处展示的图像是三个生物学重复的代表。比例尺 = 1 μm。(D) 野生型软枣猕猴桃植株叶片的总蜡质含量。数据以三个生物学重复实验的平均值 ± 标准差表示。每个生物学重复包含三个技术重复。不同的小写字母表示根据单因素方差分析(ANOVA)和随后的Tukey HSD检验得出的显著性差异 (p < 0.05)。
图2. 蜡质生物合成增强猕猴桃的抗冻性(A) 冷胁迫下,AaKCS2-OE和AaKCS6.1-OE转基因中华猕猴桃‘红阳’植株叶片的总蜡质含量。(B) AaKCS2-OE和AaKCS6.1-OE转基因中华猕猴桃‘红阳’叶片表面蜡质晶体的扫描电镜(SEM)图像。此处展示的图像是三个生物学重复的代表。比例尺 = 1 μm。(C, D) AaKCS2-OE和AaKCS6.1-OE转基因中华猕猴桃‘红阳’植株的冷冻表型。比例尺 = 5 cm。(E, F) 冷冻胁迫下,AaKCS2-OE和AaKCS6.1-OE转基因中华猕猴桃‘红阳’植株的离子外渗率、MDA含量、叶绿素含量、H₂O₂含量和O₂·⁻含量。数据以三个生物学重复实验的平均值 ± 标准差表示。每个生物学重复包含三个技术重复。星号表示显著性差异 (** p < 0.01, 学生t检验)。
2.2 AaMYB31s直接激活AaKCSs的表达
筛选候选因子:分析冷诱导上调的MYB转录因子,共鉴定出27个。系统发育树分析显示,其中4个(AaMYB31.1、AaMYB31.2、AaMYB31.3和AaMYB31.4)与拟南芥中调控蜡质合成的AtMYB31亲缘关系最近。
锁定关键基因:表达模式分析表明,在冷胁迫下,AaMYB31.1和AaMYB31.2的表达水平显著高于AaMYB31.3和AaMYB31.4,暗示它们在冷响应中可能扮演更重要的角色。亚细胞定位显示AaMYB31.1和AaMYB31.2定位于细胞核,且在叶片中表达量最高。
验证直接互作:双荧光素酶报告(DLR)实验证明,AaMYB31.1和AaMYB31.2能显著激活AaKCS2和AaKCS6.1的表达。酵母单杂交(Y1H)和电泳迁移率变动分析(EMSA)进一步证实,AaMYB31.1和AaMYB31.2能够直接结合到AaKCS2和AaKCS6.1启动子的特定区域。
为探究冷胁迫下蜡质合成基因上调是否由MYB转录因子激活,本研究对冷诱导的MYB转录因子进行了筛选。系统发育分析鉴定出四个与拟南芥蜡质合成调控因子AtMYB31同源性较高的蛋白,命名为AaMYB31.1至AaMYB31.4。其中,AaMYB31.1和AaMYB31.2在冷胁迫下的表达响应更为显著,且主要在叶片中高表达,并定位于细胞核,因此被选为重点研究对象 (Fig. 3)。鉴于AaMYB31s的表达峰值(12小时)与AaKCS2和AaKCS6.1等蜡质合成基因的时间动态相吻合,推测它们之间存在直接的调控关系。通过双荧光素酶报告(DLR)实验,证实了AaMYB31.1和AaMYB31.2能够显著激活AaKCS2和AaKCS6.1的启动子。进一步的酵母单杂交(Y1H)和电泳迁移率变动分析(EMSA)实验均表明,AaMYB31.1和AaMYB31.2能够直接结合到AaKCS2和AaKCS6.1启动子上的特定顺式作用元件。这些结果共同证明,AaMYB31s通过直接结合并激活下游蜡质合成基因AaKCSs的表达来发挥其调控功能 (Fig. 4)。
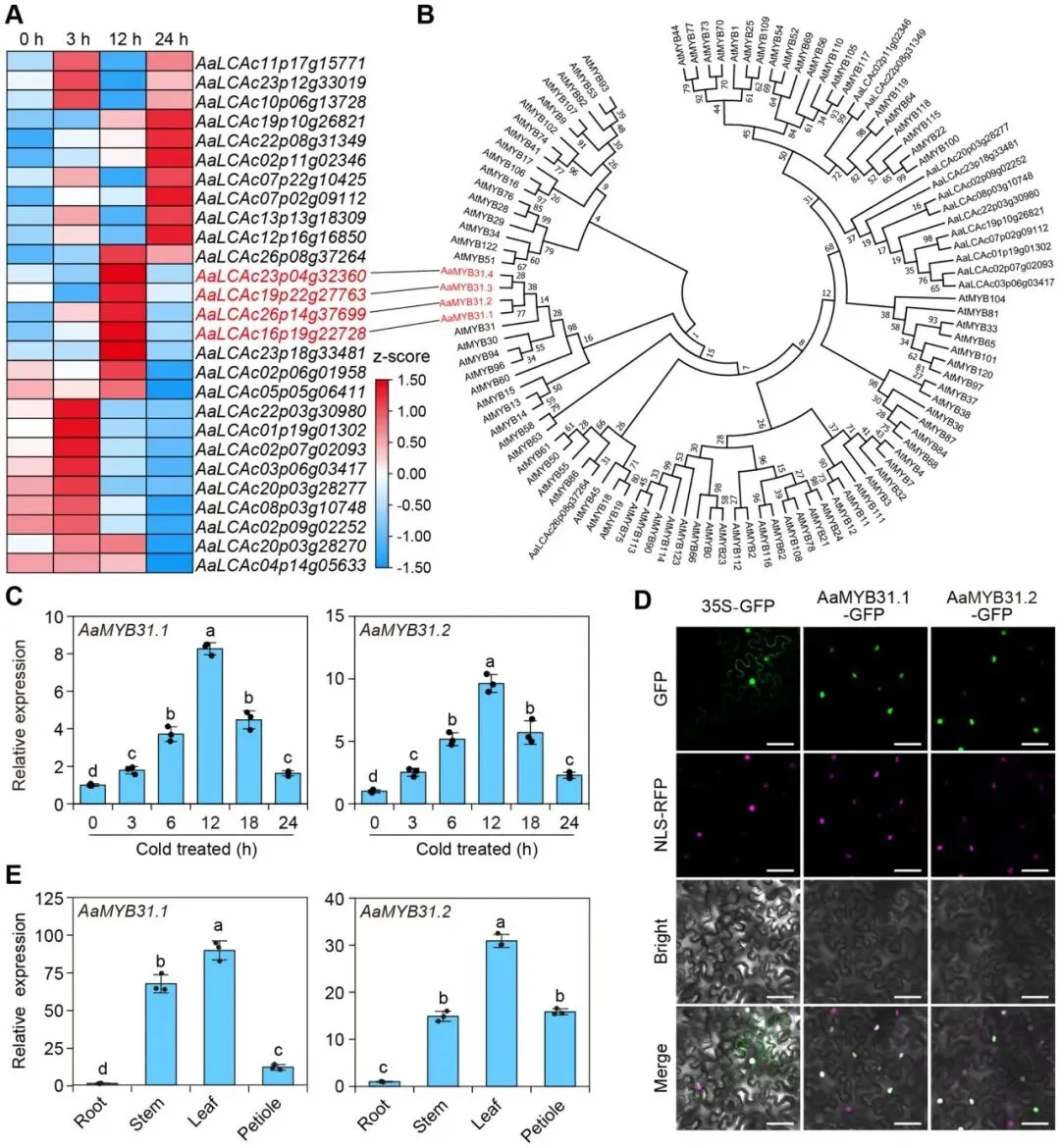
图3. AaMYB31s受冷胁迫诱导(A) 热图展示了软枣猕猴桃单个单倍型中所有冷诱导上调的MYB转录因子的表达模式。热图使用TBtools绘制,并启用了“行缩放”和“行聚类”功能。颜色梯度从蓝色到红色代表标准化的表达水平,蓝色表示低表达,红色表示高表达。目标基因以红色突出显示。(B) 软枣猕猴桃中冷诱导上调的MYB转录因子与拟南芥所有MYB转录因子的系统发育关系。软枣猕猴桃的MYB蛋白序列从NGDC数据库获取。拟南芥的所有MYB蛋白序列从Tair10获取。(C) 冷胁迫下,软枣猕猴桃植株叶片中AaMYB31.1和AaMYB31.2的表达模式。将7周龄的野生型软枣猕猴桃植株置于4°C进行48小时的冷胁迫处理。在指定时间点采集叶片用于qRT-qPCR分析。ACTIN8用作内参。(D) AaMYB31.1和AaMYB31.3在本生烟叶片中的亚细胞定位。标尺 = 50 μm。(E) AaMYB31.1和AaMYB31.3在软枣猕猴桃中的组织特异性表达模式。数据以三个生物学重复实验的平均值 ± 标准差表示。每个生物学重复包含三个技术重复。不同的小写字母表示根据单因素方差分析(ANOVA)和随后的Tukey HSD检验得出的显著性差异 (p < 0.05)。
图4. AaMYB31s直接激活AaKCSs(A, B) DLR实验表明AaMYB31.1和AaMYB31.2激活AaKCS2和AaKCS6.1的表达。(A) 色阶表示LUC信号强度(红色,高;蓝色,低)。(B) 相对LUC/REN活性。(C) Y1H实验显示AaMYB31.1和AaMYB31.2直接结合到AaKCS2和AaKCS6.1的启动子上。在AaKCS2和AaKCS6.1启动子区域的示意图中,黑线上方的P'后跟数字表示用于Y1H的区域,p'后跟数字表示EMSA中使用的探针位置。(D) EMSA显示AaMYB31.1和AaMYB31.2与AaKCS2和AaKCS6.1启动子的特定区域直接结合。数据以三个生物学重复实验的平均值 ± 标准差表示。每个生物学重复包含三个技术重复。不同的小写字母表示根据单因素方差分析(ANOVA)和随后的Tukey HSD检验得出的显著性差异 (p < 0.05)。
3.3 AaMYB31s通过正向调控蜡质合成增强抗冻性
促进蜡质合成:在正常和冷胁迫条件下,AaMYB31.1-OE和AaMYB31.2-OE转基因植株的叶片总蜡质含量均高于野生型。蜡质组分分析表明,增加的主要是C24-C30脂肪酸、C28-C32醛、C26-C32伯醇和C29-C33烷烃。SEM观察也证实转基因植株叶片表面的蜡质晶体密度显著增加。
增强抗冻表型:与野生型相比,AaMYB31.1-OE和AaMYB31.2-OE转基因植株表现出更强的抗冻性,其离子外渗率、MDA含量、H₂O₂含量和O₂·⁻含量更低,而叶绿素含量更高。同时,转基因植株中下游的AcKCSs基因表达也显著上调。
由于AaMYB31s能直接激活AaKCSs基因的表达,研究推测其在冷胁迫下能促进蜡质合成。通过构建AaMYB31.1-OE和AaMYB31.2-OE转基因中华猕猴桃,发现在正常和冷胁迫条件下,转基因植株的总蜡质含量、特定组分(如长链脂肪酸、醛、醇和烷烃)以及叶片表面的蜡质晶体密度均显著高于野生型,表明AaMYB31s在猕猴桃冷胁迫期间正向调控蜡质合成。同时,在转基因植株中,下游的内源AcKCSs基因表达也显著上调。进一步的表型分析证实,过表达AaMYB31s的植株表现出显著增强的抗冻性,其冷害指标(离子外渗率、MDA等)更低,生理状态(叶绿素含量)更佳。综上所述,这些结果表明AaMYB31s通过促进蜡质合成来增强猕猴桃的抗冻能力 (Fig. 5)。
图5. AaMYB31s通过正向调控蜡质合成来增强抗冻性(A) 冷胁迫下,AaMYB31.1-OE和AaMYB31.2-OE转基因中华猕猴桃‘红阳’植株叶片的总蜡质含量。(B) AaMYB31.1-OE和AaMYB31.2-OE转基因中华猕猴桃‘红阳’叶片表面蜡质晶体的扫描电镜(SEM)图像。此处展示的图像是三个生物学重复的代表。比例尺 = 1 μm。(C, E) AaMYB31.1-OE和AaMYB31.2-OE转基因中华猕猴桃‘红阳’植株的冷冻表型。比例尺 = 5 cm。(D, F) 冷冻胁迫下,AaMYB31.1-OE和AaMYB31.2-OE转基因中华猕猴桃‘红阳’植株的离子外渗率、MDA含量、叶绿素含量、H₂O₂含量和O₂·⁻含量。数据以三个生物学重复实验的平均值 ± 标准差表示。每个生物学重复包含三个技术重复。星号表示显著性差异 (** p < 0.01, 学生t检验)。
3.4 AaMYB31s与AaSIZ1相互作用
筛选互作蛋白:使用AaMYB31.1作为诱饵进行Pull-down质谱(Pull-down MS)筛选,鉴定到一个潜在的互作蛋白——SUMO E3连接酶AaSIZ1。该蛋白与拟南芥AtSIZ1具有显著的序列相似性。
验证蛋白互作:由于全长蛋白具有自激活活性,使用截短的AaSIZ1-N(1-664氨基酸)进行酵母双杂交(Y2H)实验,证实了其与AaMYB31.1和AaMYB31.2的相互作用。荧光素酶互补成像(LCI)、体内免疫共沉淀(Co-IP)以及体外Pull-down实验进一步从不同层面确证了AaMYB31s与AaSIZ1在体内和体外均存在直接的物理相互作用。
为进一步探索AaMYB31s的调控网络,通过Pull-down质谱筛选,鉴定出一个与AaMYB31.1互作的候选蛋白——SUMO E3连接酶AaSIZ1,其表达在冷胁迫后6小时达到峰值。考虑到SIZ1在多种生物学过程中的重要作用,研究对该互作进行了验证。通过酵母双杂交(Y2H)、荧光素酶互补成像(LCI)、体内免疫共沉淀(Co-IP)以及体外Pull-down等多种实验方法,一致性地证明了AaMYB31.1和AaMYB31.2在体内和体外均能与AaSIZ1发生直接的物理相互作用 (Fig. 6)。
图6. AaMYB31s与AaSIZ1相互作用(A) Y2H实验显示AaMYB31.1和AaMYB31.2与AaSIZ1的相互作用。BD-p53和AD-T用作阳性对照;空载体用作阴性对照。(B) LCI实验显示AaMYB31.1和AaMYB31.2与AaSIZ1的相互作用。在捕获图像前,向叶片注射1 mM荧光素。空载体用作阴性对照。(C) Co-IP实验显示AaMYB31.1和AaMYB31.2与AaSIZ1的相互作用。(D) Pull-down实验显示AaMYB31.1和AaMYB31.2与AaSIZ1在体外的相互作用。
3.5 AaSIZ1介导的AaMYB31s SUMO化修饰增强其蛋白稳定性
证实SUMO修饰:体外SUMO化实验、原生质体及本生烟叶片中的体内SUMO化实验,以及在转基因植株中的在体(in planta)SUMO化实验均表明,AaMYB31.1和AaMYB31.2是SUMO蛋白的底物,能够被SUMO化修饰。
鉴定修饰位点:通过生物信息学预测和体内定点突变实验,发现将AaMYB31.1和AaMYB31.2的第76位赖氨酸(K76)突变为精氨酸(R)后,其SUMO化水平均显著降低,表明K76是AaMYB31s发生SUMO化修饰的关键位点。
明确E3连接酶:体外及体内的SUMO化实验均显示,AaSIZ1的存在能够显著增强AaMYB31.1和AaMYB31.2的SUMO化水平,证明AaSIZ1是介导AaMYB31s SUMO化修饰的E3连接酶。
探究修饰功能:DLR实验和亚细胞定位结果表明,K76R突变(即SUMO化缺失)不影响AaMYB31s的转录激活活性及核定位。
揭示稳定机制:蛋白质降解实验发现,K76R突变体的降解速度显著快于野生型AaMYB31s。在共表达AaSIZ1或使用蛋白酶体抑制剂MG132处理后,AaMYB31s的降解均减缓,表明AaSIZ1介导的SUMO化修饰通过抑制26S蛋白酶体途径,增强了AaMYB31s的蛋白稳定性。
基于AaSIZ1与AaMYB31s的互作,研究假设AaSIZ1作为E3连接酶介导AaMYB31s的SUMO化修饰。通过一系列体外、体内(原生质体和烟草叶片)及在体(转基因植株)实验,证实了AaMYB31.1和AaMYB31.2确实是SUMO修饰的底物。进一步通过定点突变分析,成功鉴定出第76位赖氨酸(K76)是AaMYB31s发生SUMO化修饰的关键位点 (Fig. 7A-F)。随后,实验证明AaSIZ1的加入能够显著促进AaMYB31s的SUMO化,从而确认AaSIZ1是其E3连接酶 (Fig. 7G-J)。有趣的是,SUMO化修饰本身并不影响AaMYB31s的转录激活活性或其在细胞核中的定位。然而,蛋白质降解实验揭示了该修饰的关键功能:SUMO化修饰能够显著增强AaMYB31s的蛋白稳定性。与野生型蛋白相比,无法被SUMO化的K76R突变体降解速度更快。同时,AaSIZ1的共表达能够延缓AaMYB31s的降解,而这种稳定作用可被蛋白酶体抑制剂MG132模拟或增强,表明AaSIZ1介导的SUMO化通过抑制26S蛋白酶体途径来稳定AaMYB31s蛋白 (Fig. 8)。
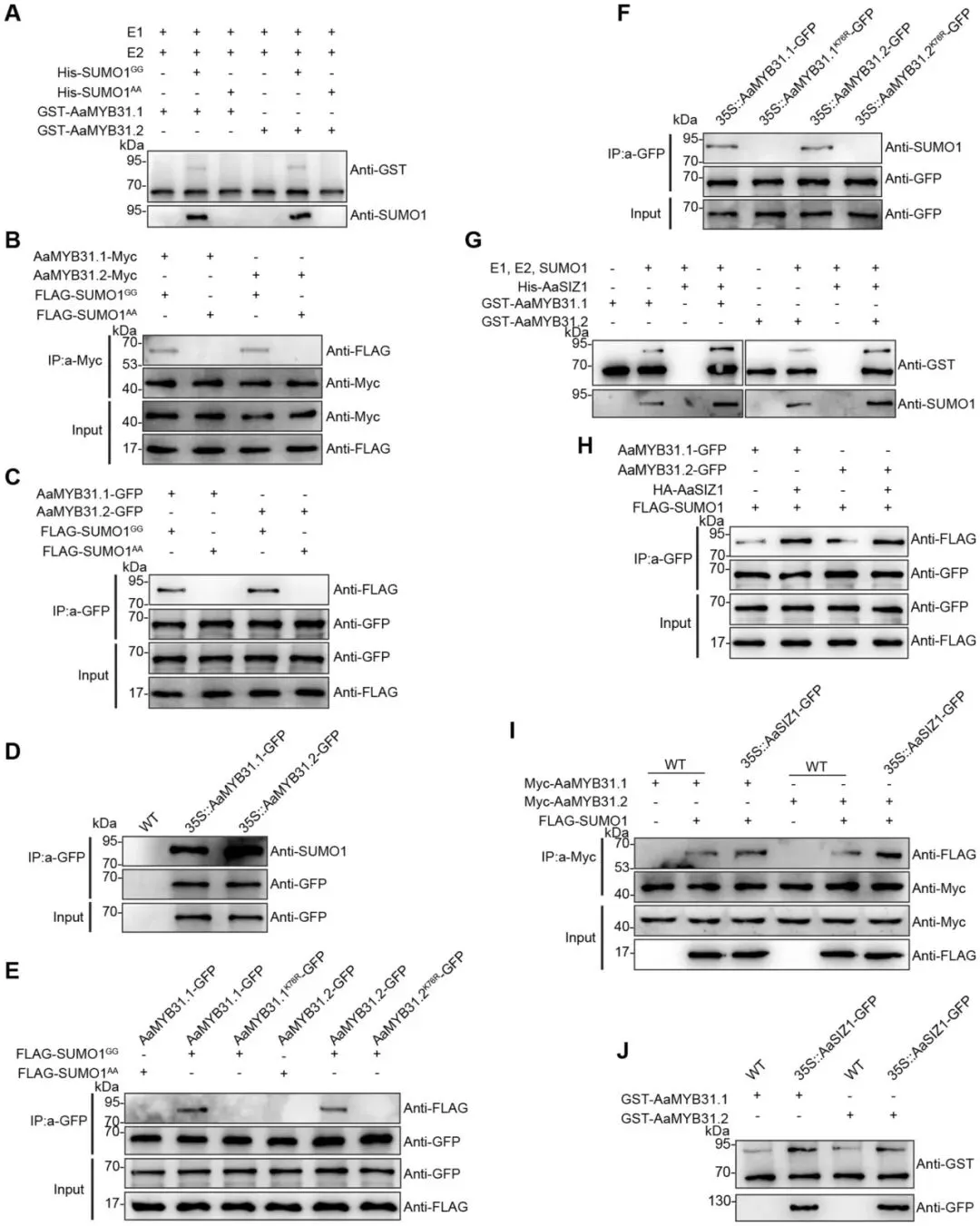
图7. AaSIZ1介导的AaMYB31s SUMO化修饰(A) AaMYB31s的体外SUMO化。使用anti-GST和anti-SUMO1抗体检测SUMO化的GST-AaMYB31.1和GST-AaMYB31.2。(B) AaMYB31s在软枣猕猴桃原生质体中的体内SUMO化。将AaMYB31.1-Myc或AaMYB31.2-Myc与FLAG-SUMO1 GG或FLAG-SUMO1 AA在软枣猕猴桃原生质体中共表达。用anti-Myc抗体免疫沉淀Myc-AaMYB31.1和Myc-AaMYB31.2,并用anti-Myc和anti-FLAG抗体检测免疫沉淀的蛋白。(C) AaMYB31s在本生烟中的体内SUMO化。将AaMYB31.1-GFP或AaMYB31.2-GFP与FLAG-SUMO1 GG或FLAG-SUMO1 AA在本生烟叶片中共表达。用anti-GFP抗体免疫沉淀AaMYB31.1-GFP和AaMYB31.2-GFP,并用anti-GFP和anti-FLAG抗体检测免疫沉淀的蛋白。(D) AaMYB31s的在体SUMO化。从野生型中华猕猴桃、35S::AaMYB31.1-GFP和35S::AaMYB31.2-GFP转基因植株的新鲜叶片中提取总蛋白,并用anti-GFP抗体免疫沉淀AaMYB31.1-GFP和AaMYB31.2-GFP。用anti-GFP和anti-SUMO1抗体检测免疫沉淀的蛋白。(E) AaMYB31.1-GFP、AaMYB31.2-GFP、AaMYB31.1 K76R-GFP和AaMYB31.1 K76R-GFP在本生烟叶片中的体内SUMO化。将AaMYB31.1-GFP、AaMYB31.1 K76R-GFP、AaMYB31.2-GFP或AaMYB31.2 K76R-GFP与FLAG-SUMO1 GG或FLAG-SUMO1 AA在本生烟叶片中共表达。AaMYB31.1-GFP和AaMYB31.2-GFP与FLAG-SUMO1 AA共表达作为阴性对照。用anti-GFP抗体免疫沉淀AaMYB31.1-GFP或AaMYB31.2-GFP,并用anti-GFP和anti-FLAG抗体检测免疫沉淀的蛋白。(F) AaMYB31.1-GFP、AaMYB31.2-GFP、AaMYB31.1 K76R-GFP和AaMYB31.1 K76R-GFP的在体SUMO化。从35S::AaMYB31.1-GFP、35S::AaMYB31.2-GFP、35S::AaMYB31.1 K76R-GFP和35S::AaMYB31.1 K76R-GFP转基因植株的新鲜叶片中提取总蛋白,并用anti-GFP抗体免疫沉淀GFP融合蛋白。用anti-GFP和anti-SUMO1抗体检测免疫沉淀的蛋白。(G) AaSIZ1在体外SUMO化AaMYB31s蛋白。使用anti-GST和anti-SUMO1抗体检测SUMO化的GST-AaMYB31.1和GST-AaMYB31.2。(H) AaSIZ1在本生烟中对AaMYB31s的体内SUMO化。将AaMYB31.1-GFP或AaMYB31.2-GFP和AaSIZ1与或不与FLAG-SUMO1在本生烟叶片中共表达。用anti-GFP抗体免疫沉淀AaMYB31.1-GFP和AaMYB31.2-GFP,并用anti-GFP和anti-FLAG抗体检测免疫沉淀的蛋白。(I) 35S::AaSIZ1-GFP转基因植株中AaMYB31s的SUMO化。从野生型中华猕猴桃和35S::AaSIZ1-GFP转基因植株的新鲜叶片中提取总蛋白,并与GST-AaMYB31.1或GST-AaMYB31.2孵育。使用anti-GST抗体检测SUMO化的GST-AaMYB31.1和GST-AaMYB31.2。(J) AaSIZ1在软枣猕猴桃原生质体中介导AaMYB31s的SUMO化。将Myc-AaMYB31.1或Myc-AaMYB31.2与FLAG-SUMO1在软枣猕猴桃原生质体中共表达。用anti-Myc抗体免疫沉淀Myc-AaMYB31.1和Myc-AaMYB31.2,并用anti-Myc和anti-FLAG抗体检测免疫沉淀的蛋白。
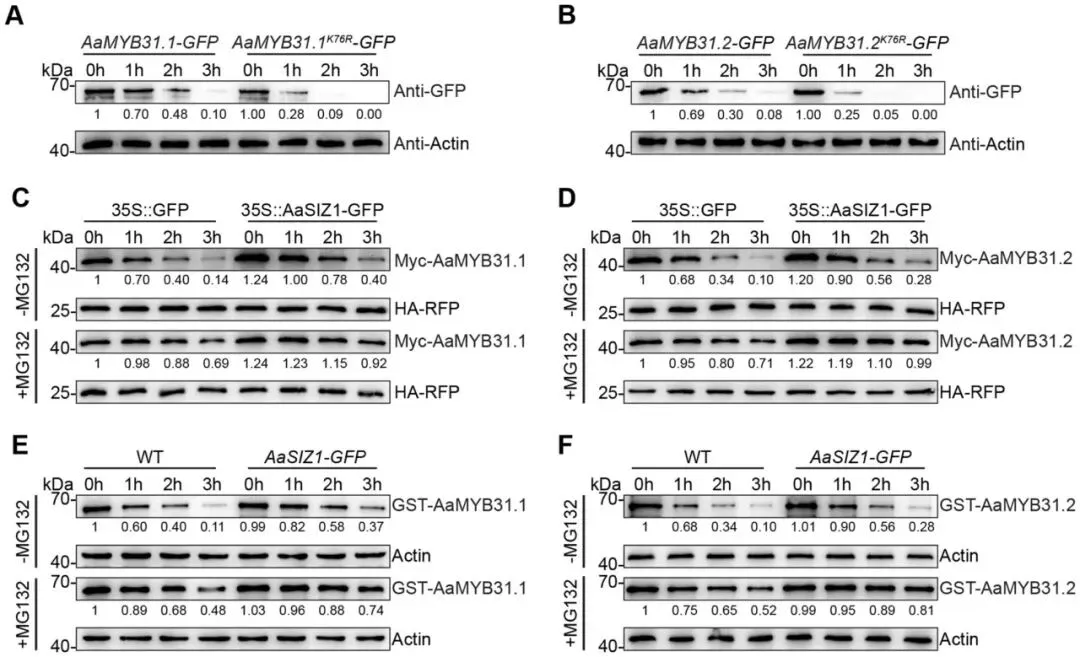
图8. AaSIZ1介导的AaMYB31s SUMO化修饰增强其蛋白稳定性(A, B) AaMYB31.1-GFP和AaMYB31.1 K76R-GFP,或AaMYB31.2-GFP和AaMYB31.1 K76R-GFP转基因植株中AaMYB31s的蛋白质降解。从AaMYB31.1-GFP和AaMYB31.1 K76R-GFP,或AaMYB31.2-GFP和AaMYB31.1 K76R-GFP转基因植株的新鲜叶片中提取总蛋白。使用anti-GFP抗体检测AaMYB31.1-GFP、AaMYB31.1 K76R-GFP、AaMYB31.2-GFP和AaMYB31.2 K76R-GFP。ACTIN用作内参。(C, D) AaMYB31s在本生烟中的体内蛋白质降解。将35S::GFP或35S::AaSIZ1-GFP与Myc-AaMYB31s和HA-RFP在本生烟叶片中共表达,并提取总蛋白。这些蛋白用DMSO (-MG132)或50 μM MG132处理指定时间后同时取样检测。使用anti-Myc抗体检测Myc-AaMYB31.1和Myc-AaMYB31.2。HA-RFP用作内参。(E, F) 35S::AaSIZ1-GFP转基因植株中AaMYB31s的蛋白质降解。从野生型中华猕猴桃和35S::AaSIZ1-GFP转基因植株的新鲜叶片中提取总蛋白,并与GST-AaMYB31.1或GST-AaMYB31.2孵育。这些蛋白用DMSO (-MG132)或50 μM MG132处理指定时间后同时取样检测。使用anti-GST抗体检测GST-AaMYB31.1和GST-AaMYB31.2。ACTIN用作内参。
3.6 AaMYB31s的SUMO化修饰在冷胁迫下增强
冷诱导SUMO化:在转基因植株中,与22°C相比,4°C冷处理显著增强了AaMYB31.1和AaMYB31.2的SUMO化水平。
冷抑制泛素化:与SUMO化相反,4°C冷处理导致AaMYB31.1和AaMYB31.2的多聚泛素化水平均显著下降。
增强蛋白稳定:蛋白质降解实验表明,AaMYB31s-GFP蛋白在4°C下的降解速度慢于22°C。而无法SUMO化的AaMYB31s K76R-GFP蛋白则在两种温度下均快速降解且速率不受温度影响。
促进蛋白互作:Co-IP实验显示,与常温相比,冷胁迫(4°C)能够显著增强AaSIZ1与AaMYB31s之间的相互作用。
为探究冷胁迫是否影响AaMYB31s的SUMO化,研究发现在4°C冷处理下,AaMYB31.1和AaMYB31.2的SUMO化水平均显著增强,而其泛素化水平则相应降低。这种翻译后修饰的动态变化直接影响了蛋白稳定性:在低温下,野生型AaMYB31s蛋白的降解速度减缓,而无法被SUMO化的K76R突变体则无论在何种温度下都快速降解。这表明冷胁迫通过增强SUMO化、减弱泛素化来稳定AaMYB31s蛋白。进一步的Co-IP实验揭示了其原因:冷胁迫能够显著增强AaSIZ1与AaMYB31s之间的相互作用,从而促进了AaSIZ1介导的SUMO化过程。这些发现共同说明,在冷胁迫下,AaMYB31s的SUMO化被增强,从而有效减缓其蛋白降解,进而可能有助于提高软枣猕猴桃的抗寒性 (Fig. 9)。
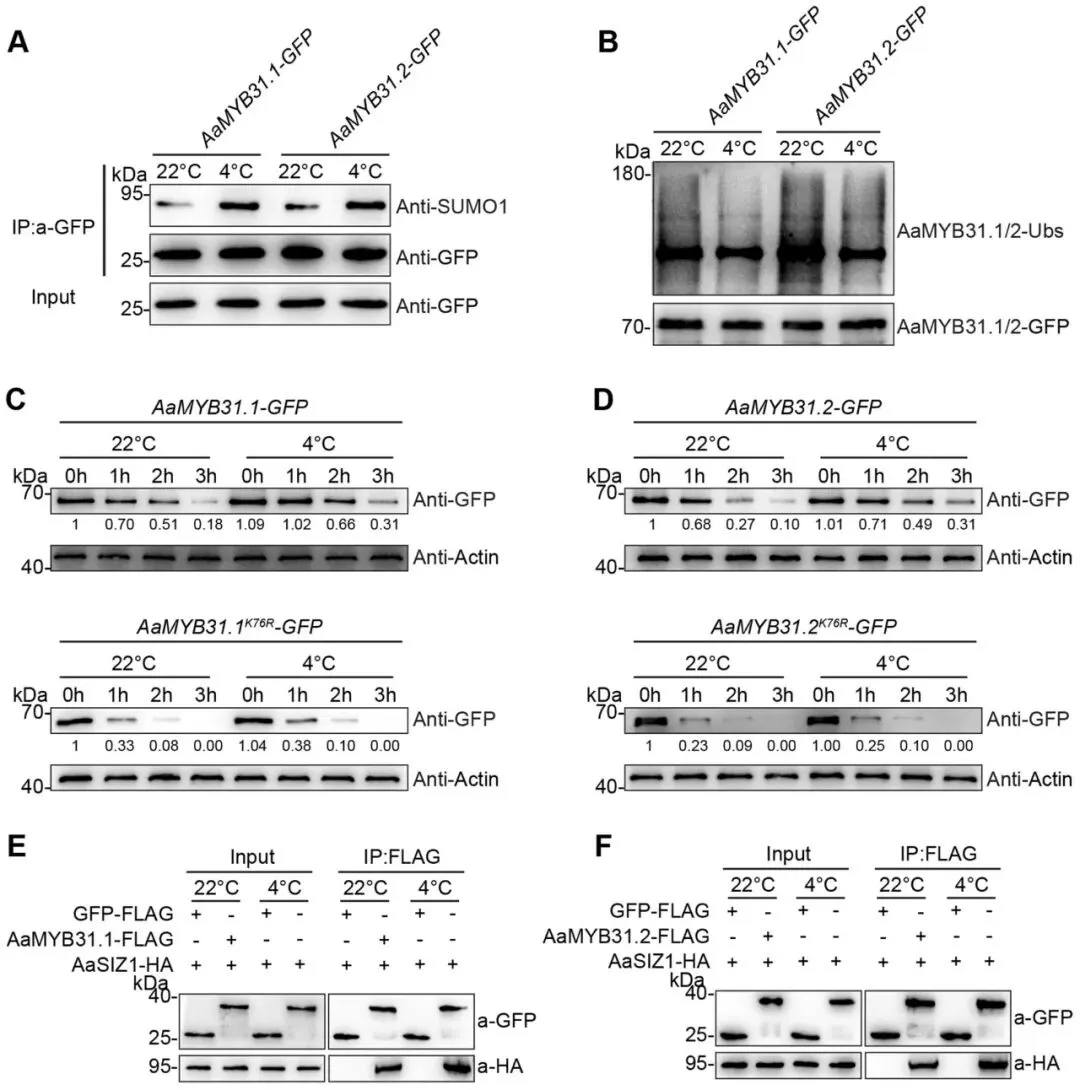
图9. AaSIZ1介导的AaMYB31s SUMO化在冷胁迫下增强(A) 低温增强了AaMYB31s的SUMO化水平。将35S::AaMYB31.1-GFP和35S::AaMYB31.2-GFP转基因中华猕猴桃植株在22°C和4°C下培养2小时,并用anti-GFP抗体免疫沉淀GFP融合蛋白。用anti-GFP和anti-SUMO1抗体检测免疫沉淀的蛋白。(B) 低温降低了AaMYB31s的泛素化水平。将35S::AaMYB31.1-GFP和35S::AaMYB31.2-GFP转基因中华猕猴桃植株在22°C和4°C下培养2小时,并用anti-GFP抗体免疫沉淀GFP融合蛋白。用anti-ubiquitin抗体检测免疫沉淀的蛋白。(C, D) 低温增强了AaMYB31s的蛋白稳定性。将35S::AaMYB31.1-GFP、35S::AaMYB31.2-GFP、35S::AaMYB31.1 K76R-GFP或35S::AaMYB31.2 K76R-GFP转基因植株在22°C或4°C下培养,然后在0、1、2和3小时取样并提取总蛋白。使用anti-GFP抗体检测AaMYB31.1和AaMYB31.2。Actin用作内参。(E, F) 冷胁迫增强了AaSIZ1和AaMYB31s之间的相互作用。将GFP-FLAG或AaMYB31s与AaSIZ1-HA在本生烟叶片中共表达,并在4°C处理或不处理后提取总蛋白。用anti-FLAG抗体免疫沉淀GFP融合蛋白。用anti-GFP和anti-HA抗体检测免疫沉淀的蛋白。
3.7 AaSIZ1通过促进蜡质合成正向调控抗冻性
调控蜡质合成:与野生型相比,AaSIZ1-OE转基因植株在正常和冷胁迫条件下均表现出更高的总蜡质含量和更密集的表皮蜡质晶体。
提升抗冻能力:表型分析显示,AaSIZ1-OE转基因植株具有更强的抗冻性,其冷害生理指标均优于野生型。
验证修饰功能:与AaMYB31s-OE植株相比,SUMO化位点突变的AaMYB31s K76R-OE植株虽然抗冻性强于野生型,但其蜡质含量和抗冻能力均显著弱于前者,这直接证明了AaSIZ1介导的AaMYB31s SUMO化修饰在调控蜡质合成和抗冻性中的关键作用。
鉴于AaSIZ1通过介导SUMO化来稳定AaMYB31s,研究进一步探究AaSIZ1本身是否通过调控蜡质合成来影响抗冻性。结果显示,过表达AaSIZ1的转基因植株(AaSIZ1-OE)在正常和冷胁迫条件下,其总蜡质含量和叶片表面蜡质晶体密度均显著高于野生型,并且表现出显著增强的抗冻表型,各项生理指标也优于野生型 (Fig. 10)。为了进一步确认这一功能依赖于对AaMYB31s的SUMO化修饰,研究比较了AaMYB31s-OE和SUMO化位点突变的AaMYB31s K76R-OE转基因植株。结果发现,尽管AaMYB31s K76R-OE植株的抗冻性仍强于野生型,但其蜡质含量和抗冻能力均显著弱于AaMYB31s-OE植株。这一结果有力地证明,K76位点的SUMO化修饰对于AaMYB31s充分发挥其促进蜡质合成和增强抗冻性的功能至关重要。综上所述,AaSIZ1通过介导AaMYB31s的SUMO化修饰,正向调控蜡质合成,从而增强了植株的抗冻性。
图10. AaSIZ1通过促进蜡质生物合成来调控抗冻性(A) 冷胁迫下,AaSIZ1-OE转基因中华猕猴桃‘红阳’植株叶片的总蜡质含量。(B) AaSIZ1-OE转基因中华猕猴桃‘红阳’叶片表面蜡质晶体的扫描电镜(SEM)图像。此处展示的图像是三个生物学重复的代表。比例尺 = 1 μm。(C) AaSIZ1-OE转基因中华猕猴桃‘红阳’植株的冷冻表型。比例尺 = 5 cm。(D) 冷冻胁迫下,AaSIZ1-OE转基因中华猕猴桃‘红阳’植株的离子外渗率、MDA含量、叶绿素含量、H₂O₂含量和O₂·⁻含量。数据以三个生物学重复实验的平均值 ± 标准差表示。每个生物学重复包含三个技术重复。星号表示显著性差异 (** p < 0.01, 学生t检验)。