研究首先从材料设计与构建逻辑入手,建立了两类可对照分析的嵌合肽:一类为树枝状分支肽BCPR,另一类为线性肽LCPR。在分子组成上,研究将N端十四烷基链作为疏水驱动单元,用于促使肽分子自组装;将PRRI重复序列作为细胞穿透核心模块;将WELQ序列嵌入主链,作为对MRSA分泌酶SplB具有特异响应的切割位点;同时在C端引入RGD序列,以便与巨噬细胞膜表面的αvβ3整合素结合,实现感染细胞识别与黏附增强。为了验证结构构建是否成功,研究采用了固相合成、RP-HPLC和ESI-MS进行纯化与鉴定,结果表明两类肽纯度均高于95%,实测分子量与理论值一致。随后,通过ANS荧光法评估自组装能力,发现BCPR与LCPR的临界聚集浓度分别约为17.8 μM和17.4 μM,说明二者均能在相近浓度区间内形成稳定纳米结构。TEM与DLS进一步证实,这两类肽在水相中均可形成约10 nm左右、分散均一的纳米颗粒;Zeta电位结果则显示,BCPR表面正电性高于LCPR,提示分支构型提高了正电荷密度,有利于增强其与细胞膜和细菌膜的相互作用。圆二色谱显示二者均以随机卷曲构象为主,这一特征与富脯氨酸肽低膜裂解毒性、适于细胞穿透的性质相一致。最后,研究通过酶切前后HPLC保留时间变化确认WELQ序列可被SplB特异识别,证明该体系具备明确的细菌酶响应性。从方法学上看,这一部分并非只是完成材料表征,而是把“为什么能自组装、为什么能穿膜、为什么能被细菌触发再加工”逐层建立起来,为后续生物功能验证奠定了严密基础。
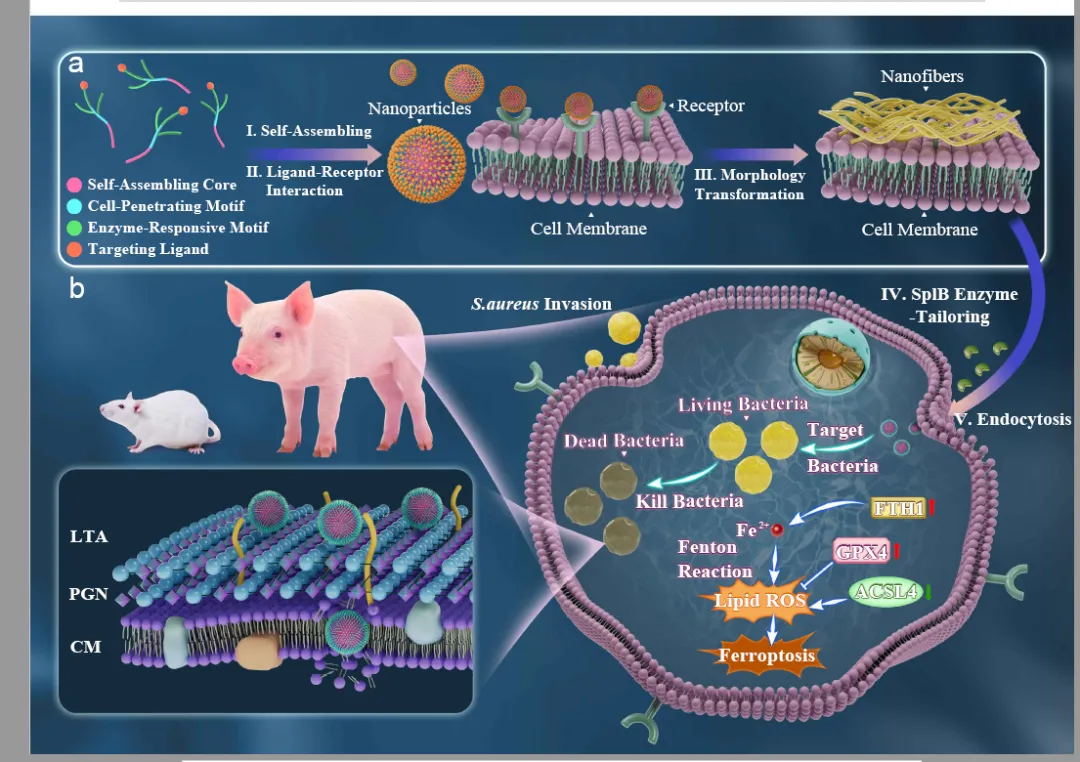
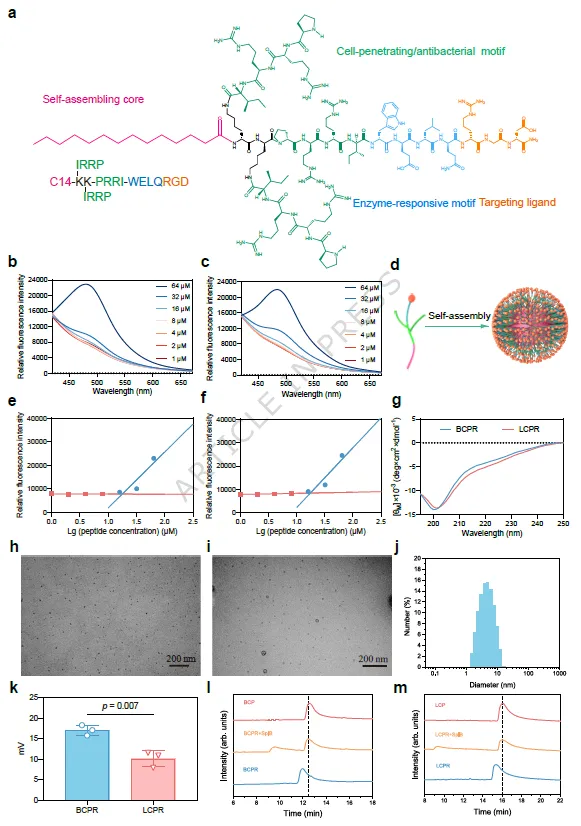
在抗菌效能与生物安全性方面,研究采用MIC/MBC、溶血实验、细胞活力检测、细胞内杀菌实验和显微成像进行了系统评估。结果显示,无论在酶切前还是酶切后,两类肽均对MRSA和多株MSSA表现出良好抗菌活性,但BCPR整体优于LCPR,提示树枝状构型确实带来了更强的功能输出。安全性方面,两类肽在128 μM的较高浓度下对红细胞的溶血率仍低于10%,明显优于多黏菌素B;在RAW264.7细胞、原代猪肺泡巨噬细胞和HEK293T细胞中的毒性也总体较低,仅在RAW264.7细胞高浓度下出现轻微影响。更关键的是,在无明显毒性的工作浓度下,这些肽表现出突出的细胞内耐药菌清除能力:在32 μM时,BCPR和LCPR对细胞内MRSA的清除率分别达到99.9%和89.7%,且BCPR优于临床常用的万古霉素。利用GFP标记MRSA构建细胞内感染模型后,研究借助共聚焦Z-stack成像清晰观察到,未经处理的巨噬细胞内可见明显细菌聚集,而经肽处理后细胞内绿色细菌信号明显下降,尤其BCPR组最为显著。杀菌动力学进一步表明,BCPR在32 μM下2 h内即可实现完全清除,在16 μM下则需约6 h,说明其在达到聚集阈值后,纳米组装形态可显著放大抗菌效率。此外,研究还将体系拓展到成熟生物被膜模型,结果显示BCPR在8 μM时就已呈现明显杀菌作用,在32 μM时对被膜内细菌的杀灭率超过80%,并可破坏已形成的成熟生物被膜。这说明该体系不仅能解决细胞内感染,也对耐药菌常见的被膜防御状态具有干预潜力。
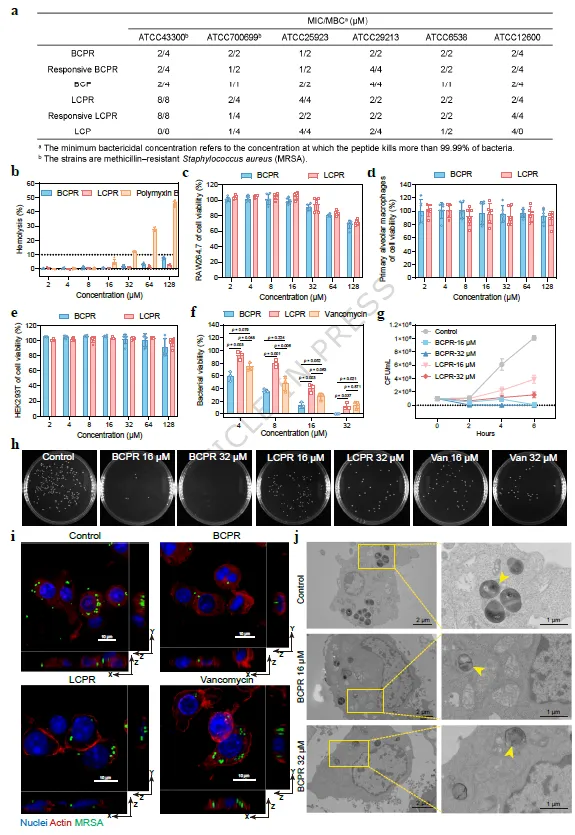
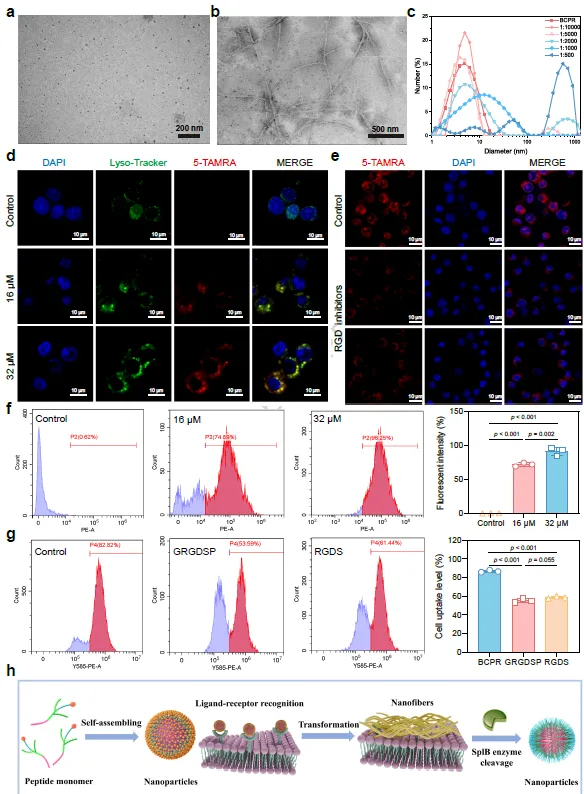
该研究最具特色的部分之一,在于把“靶向黏附”与“结构转变”有机耦合起来。作者并未满足于证明肽能进入细胞,而是进一步探究其是否能够先在靶细胞表面停留,再由病原菌触发转化为更利于穿膜的形态。结果显示,BCPR初始在溶液中为约10 nm纳米颗粒;但当其与αvβ3整合素孵育后,TEM可见其转变为纳米纤维,DLS也显示尺寸随整合素比例增加而显著增大,表明RGD-整合素识别可诱导颗粒向纤维网络重构。这一过程在功能上十分关键,因为纤维形态意味着更强的局部滞留与膜表面累积,而不是快速扩散和清除。随后,流式检测表明BCPR在16 μM和32 μM下的细胞摄取率分别达到74.89%和96.25%,呈现很高的穿透效率;而当用GRGDSP或RGDS阻断RGD受体结合后,其进入RAW264.7细胞的效率明显下降,说明该体系的高效内化并非单纯依赖正电性,而是与整合素介导的膜表面富集密切相关。更进一步,研究模拟了“先受体结合、后经SplB切割”的连续过程,发现纳米纤维在酶作用后又可转变为约5 nm的小颗粒。低温和内吞抑制实验则提示,BCPR主要通过能量非依赖性的直接跨膜转位进入细胞,而并非传统内吞途径。这一点非常重要,因为它解释了为何该体系在细胞内感染模型中能快速起效。共聚焦观察还显示,进入细胞后的肽可到达溶酶体区域,而大多数侵入性细菌最初就滞留于该类胞内囊泡中。进一步的TEM与共聚焦成像甚至直接观察到,进入细胞后的5 nm颗粒可围绕在细胞内MRSA周围,并与GFP标记细菌空间重合,说明该体系的“表面富集—酶切缩小—胞内追踪”这一设计逻辑在实验上得到了完整验证。
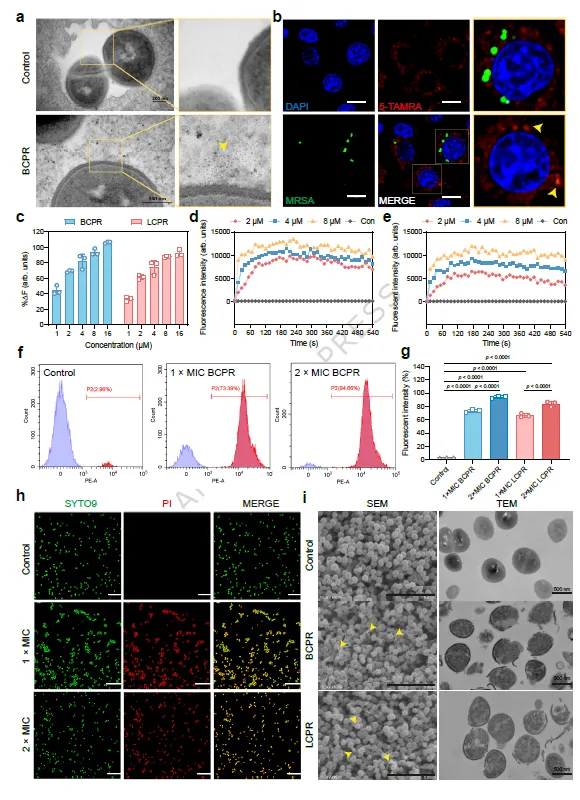
在抗菌作用机制上,研究把重点放在了细菌膜破坏这一不易诱导耐药的物理杀菌机制。首先,作者通过与脂磷壁酸(LTA)的结合实验发现,BCPR和LCPR均可剂量依赖性结合MRSA表面的阴离子组分,但BCPR亲和力更强,这与其更高的表面正电荷密度相吻合。随后,利用DiSC3-5膜电位探针检测膜去极化过程,发现两类肽在短时间内即可引起MRSA膜电位塌陷,其中BCPR作用更迅速、更剧烈,且荧光信号在120 s内迅速上升后趋于稳定,说明其可以在极短时间内穿过MRSA厚厚的细胞壁并攻击细胞质膜。PI流式检测和SYTO9/PI双染结果进一步证实,肽处理后MRSA膜完整性遭到严重破坏。以BCPR为例,在2 μM和4 μM下即可分别导致73.39%和96.42%的细菌死亡,而LCPR需更高浓度方能达到类似水平。SEM和TEM提供了更直观的结构证据:处理后细菌表面出现皱缩、孔洞和破裂,细胞内容物外泄,最终形成碎片化残骸。也就是说,该体系的主要效应并不是抑制某一个特定代谢酶或细胞壁合成靶点,而是通过带正电且具有疏水基团的纳米肽直接干扰细菌膜结构,因此理论上更难诱导经典耐药机制的产生。为了验证这一点,研究设计了持续30天的亚抑菌浓度传代实验,结果显示肽的活性几乎不下降;相反,万古霉素MIC升高了64倍,利福平则升高了512倍。这一结果不仅是“抗菌有效”的证明,更表明该体系在对抗耐药进化方面具备显著优势。
除了直接杀菌,该研究还把感染细胞本身的损伤状态纳入了评价框架,尤其关注了近年备受重视的铁死亡。作者首先用Ferrostatin-1开展拯救实验,证实MRSA感染确实会诱导巨噬细胞发生铁死亡相关损伤。TEM下可见感染后线粒体皱缩、嵴减少,伴随细胞膜破裂和LDH释放增加;而BCPR处理后,这些超微结构损伤明显减轻。进一步使用DCFH-DA、RhoNox-1和BODIPY-C11等探针检测ROS、Fe²⁺和脂质过氧化,结果显示,MRSA感染可显著提高巨噬细胞内活性氧与游离铁水平,并诱导明显脂质过氧化;相比之下,BCPR能显著抑制这些变化。MDA定量结果尤其有代表性:感染使脂质过氧化升高约2.1倍,而肽处理后可将这一反应降低约40%。在分子层面,作者又检测了铁死亡相关基因表达,发现感染后GPX4下调约2.2倍、ACSL4上调约1.4倍、FTH1下调约2.6倍、NRF2下调约4.3倍;而BCPR处理后,GPX4、FTH1和NRF2重新上升,ACSL4下降,整体趋势与抑制铁死亡一致。值得注意的是,当研究者直接用RSL3诱导铁死亡时,BCPR并不能明显逆转相关通路,这说明其并不是一个直接的铁死亡抑制剂,而是通过减少细胞内细菌负荷、减轻感染引起的氧化与铁代谢失衡,进而间接保护巨噬细胞。这一点使讨论更为严谨:作者没有把BCPR简单包装为“万能抗氧化剂”,而是明确指出其保护作用建立在高效胞内抗菌基础之上,逻辑链条更加可信。
在体内评价部分,研究首先考察了体系的广谱适配性与生物安全性。为了说明这一设计并非仅适用于MRSA,作者将原有的SplB响应序列替换为对铜绿假单胞菌明胶酶敏感的PLGLAG序列,构建出新的响应性肽树枝体,并证明其在RAW264.7细胞内同样能显著清除胞内铜绿假单胞菌,杀菌率达到97%。在此基础上,研究通过小鼠预实验确定15 mg/kg为最低有效剂量,并设置15和30 mg/kg进行连续7天腹腔注射安全性评估。结果显示,小鼠在整个给药期内无异常行为、精神状态稳定、体重无明显下降;肝肾脏器指数维持正常,ALT、ALP、CREA、TBIL、UREA等生化指标未见显著异常,肝肾H&E染色也未发现组织结构损伤。这一部分为后续感染治疗实验提供了必要前提。另一方面,研究还评估了体系在复杂生理环境中的稳定性,发现BCPR即使在不同浓度人血清或蛋白酶K处理后,其MIC基本不变,说明自组装纳米结构确实赋予了其较强的抗降解能力和生理稳定性。这一点对于肽类药物尤其关键,因为传统肽药往往受限于血清失活和蛋白酶切割,而该体系在这一方面表现出了明显改进。
随后,作者在小鼠肌肉感染模型和MRSA腹膜炎模型中验证了其体内靶向分布与治疗效果。在肌肉感染模型中,5-TAMRA标记的肽经腹腔注射后,1 h内即可在感染部位出现显著荧光富集,且感染区信号强度超过非感染区50倍以上,24 h后仍可保留清晰信号,说明其不仅能到达感染灶,而且具有较长滞留时间。连续三次给药后,感染肌肉内菌负荷显著下降,BCPR实现了4.27-log的菌量削减,即约99.9999%的杀菌效果,且优于万古霉素,组织学上也可见炎症细胞浸润和组织损伤明显减轻。在更具代表性的腹膜炎模型中,未治疗组小鼠于感染后48 h内陆续死亡,而肽治疗组和万古霉素组均显著提高生存率。更重要的是,BCPR不仅降低了肝、肾、脾、肺等脏器的总体菌负荷,而且在腹腔巨噬细胞内MRSA清除方面优于万古霉素,这与其出色的细胞穿透能力高度一致。与此同时,IL-1β、IL-6和TNF-α等炎症因子水平明显下降,LTA诱导的炎症模型也证实该肽具有一定的免疫调节效应,能够通过结合LTA阻断其与TLR的相互作用,从而减轻持续性炎症刺激。组织病理结果同样支持这一结论:与感染组相比,肽处理后肝脏、肺等组织的炎症浸润和损伤程度明显减轻。
最后,研究将验证推进到了猪仔模型,这也是其结果部分非常有说服力的一点。由于猪在免疫系统、代谢和器官生理上与人更接近,因此其结果更具转化参考价值。实验显示,在感染猪仔中,BCPR与万古霉素均可提高存活率并降低组织细菌负荷,但BCPR对猪肺泡巨噬细胞内MRSA的杀灭效果更为突出。与此同时,炎症因子水平下降,组织出血和炎症损伤减轻,整体趋势与小鼠模型高度一致。综合全文可以看到,这项研究并不是单一展示一种“能杀菌的肽”,而是建立了一套逻辑闭环完整的治疗策略:先通过RGD-整合素实现感染细胞表面靶向黏附,再通过受体诱导形成纳米纤维以增强局部滞留,随后依赖细菌分泌酶将其裁剪成更小颗粒以实现高效跨膜进入,最终通过膜破坏方式清除细胞内耐药菌,并在感染负荷下降的同时缓解巨噬细胞铁死亡与炎症损伤。因此,这项工作的真正价值在于,它把结构可编程的肽自组装材料从传统“抗菌材料”推进到了面向细胞内耐药感染的靶向、响应和多效协同治疗平台,为开发新一代不易诱导耐药的抗感染纳米药物提供了较强的实验依据。