Food Chem. 中国农业科学院-通过改造活性位点和远端位点提高Paenibacillus barengoltzii来源的β-半乳糖苷酶的半乳寡糖合成效率
2025 年 4 月 4 日,来自中国农业科学院的Haiyan Yu、Yulu Wang和Zhisen Yang等人在Nature Communications上发表了一篇题为Enhancing the synthesis efficiency of galacto-oligosaccharides of a β-galactosidase from Paenibacillus barengoltzii by engineering the active and distal sites的研究性论文。Abstract
前期研究发现,来自巴伦戈茨类芽孢杆菌的糖苷水解酶第2家族β-半乳糖苷酶具有高效的转糖基能力。本研究解析了PbBGal2A的冷冻电镜结构,揭示其具有一个扩大的酸性催化口袋,有利于碳水化合物底物的结合。通过三种基于结构的策略结合机器学习MECE平台,鉴定了能够增强半乳寡糖合成的活性位点及远端突变,并评估了它们的协同效应。最优突变体H331V在35%乳糖底物浓度下反应4小时,GOS最高产率达到76.57%。分子动力学模拟进一步表明,远端突变增强了催化口袋周围环区的刚性。本研究阐明了PbBGal2A的结构与催化机制,凸显了活性位点与远端突变在高效设计定制化β-半乳糖苷酶中的重要性。
Introduction
半乳寡糖是一类具有类似人乳寡糖功能的非消化性碳水化合物混合物。从结构上看,GOS通常由2-9个半乳糖残基组成,其还原端连接着一个末端葡萄糖。作为一种公认的益生元,GOS对宿主具有一系列促进健康的特性,例如促进有益肠道细菌的增殖和功能、调节微生物-肠-脑轴、阻止病原体粘附、减轻过敏反应以及缓解代谢性疾病。GOS的安全性已获得全球公认。鉴于全球对健康的日益关注,GOS作为功能性食品补充剂,在婴幼儿配方奶粉、婴儿食品、烘焙食品、饮料、酸奶、巧克力和许多其他食品中拥有广阔的市场前景。预计到2025年,全球商业GOS产品的市场利润将高达约105.5亿美元。
目前商业化生产GOS的方法主要是利用β-半乳糖苷酶催化乳糖或乳清发生转糖基反应生成GOS。该方法因其反应条件温和、操作简单、效率高等优点,是一种有效且适合大规模生产的方法。β-半乳糖苷酶在食品加工业中具有双重作用:作为水解酶,它能催化牛奶中乳糖的分解;而作为转半乳糖基酶,它能生产具有不同聚合度的GOS。在这两种应用中,具有优异转糖基效率的β-半乳糖苷酶都备受青睐。目前,已从微生物源中鉴定和表征了许多β-半乳糖苷酶,包括细菌和真菌,如乳酸克鲁维酵母、米曲霉和环状芽孢杆菌。然而,这些来源的GOS产率很少超过50%。这个生产水平不足以满足工业化规模、高效生产GOS的需求,因此需要进一步提高。
除了从不同来源筛选新酶外,蛋白质工程已成为增强β-半乳糖苷酶GOS合成能力的有效策略。根据碳水化合物活性酶数据库,β-半乳糖苷酶主要分为四个糖苷水解酶相关家族:GH1、GH2、GH35和GH42。这些酶通过两步双置换机制催化反应。β-半乳糖苷酶的这种反应机制为改造其活性位点以提高GOS合成产率提供了三种潜在策略:(1) 改变+1亚位点以增强底物结合,从而促进反应进行;(2) 改造-1亚位点以降低对酮糖的亲和力,从而减少酶的水解活性并增加半乳糖产率;(3) 增加活性位点的疏水性,以限制水分子参与并最大限度地减少水解反应。例如,开发了一种双疏水氨基酸扫描策略来提高β-半乳糖苷酶Bgal1-3的转糖基能力。该策略揭示,C510V和H512I突变使得GOS合成效率显著提高,分别增加了1.93倍和1.23倍。在另一项研究中,对米曲霉β-半乳糖苷酶的N140C、W806F和N140C/W806F突变体进行了工程改造,以破坏-1亚位点的半乳糖结合并增加活性位点的疏水性,结果发现所有突变体产生的GOS水平均高于野生型。突变体N140C/W806F的最高GOS产率表明两个单突变存在上位效应。
传统的基于结构的理性设计包括识别关键活性位点和重塑底物结合口袋。随着对结构-功能关系理解的加深,人们越来越认识到远端位点在维持酶功能中的重要作用。随着大量复杂生物数据集的积累,已经开发了几种基于序列的机器学习策略来预测整个蛋白质中的突变热点,其中许多并不位于活性位点。最近,引入了一种通过利用在119个不同GH家族上训练的深度神经网络模型来准确预测功能性突变的方法,即提高催化效率平台。该方法成功应用于壳聚糖酶CHIS1754的工程改造,产生了显著提高催化效率的远端突变。然而,远端位点对β-半乳糖苷酶活性和GOS合成能力的影响,以及它们与活性位点的潜在协同效应,尚未见报道。
前期研究中,来自海洋细菌巴伦戈茨类芽孢杆菌的一种新型GH2家族β-半乳糖苷酶被成功异源表达、纯化和表征。该酶表现出强大的转糖基能力,GOS产率高达47.9%,显示出良好的商业应用前景。在本研究中,解析了PbBGal2A的高分辨率冷冻电镜结构,为蛋白质工程改造提供了结构细节。采用三种基于结构的策略对PbBGal2A的活性位点进行靶向诱变,使GOS最高产率达到76.57%。此外,通过MECE策略鉴定了几个有益的远端突变,并评估了它们与活性位点突变的协同效应。本研究为PbBGal2A的结构和催化机制提供了新的见解,突显了活性位点和远端突变在有效设计定制化β-半乳糖苷酶中的重要性。
PbBGal2A 展现出显著的转糖基能力,GOS 最高产率达到 47.9%,这一产率超过了多种微生物来源的 β-半乳糖苷酶(表 1)。为探究 PbBGal2A 提高 GOS 生物合成效率的结构基础,鉴于其分子量较大(695 kDa),采用了冷冻电镜技术(图 1A)。经过不同浓度的筛选,收集了一套电镜数据集,并用于解析 PbBGal2A 的结构,整体分辨率为 2.8 Å。二维分级平均图显示 PbBGal2A 主要是一个对称的六聚体。
电镜密度图的质量能够以 AlphaFold2 预测的模型为模板,重建完整的原子模型。结构分析表明,PbBGal2A 在最终模型中形成一个六聚体,其长度为 165.4 Å,宽度为 123.2 Å,高度为 166.8 Å(图 1B),这一发现与通过 SEC-MALS 在溶液中观察到的寡聚状态一致(图 1A)。所有六个链中都缺失了 395–405、472–482 和 709–718 残基,表明这些区域具有柔性。该六聚体结构由三个同源二聚体组装成一个桶状结构。每个单体由 1014 个残基组成,并折叠成五个结构域(图 1C 和 D):结构域 1(A1-N213)、结构域 2(T214-K308)、结构域 3(V309-P603)、结构域 4(V604-E721)和结构域 5(K722-E1014),这与其他已报道的 GH2 家族 β-半乳糖苷酶中观察到的结构相似。中心的 TIM 桶状结构域(结构域 3)由八个平行的 β 链和八个 α 螺旋组成,其中包含催化残基 E443 和 E514。构成催化口袋的残基主要来自催化结构域 3。在 PbBGal2A 结构中,一个覆盖活性位点的长环插入片段(残基 472–482)不可见。在其他 β-半乳糖苷酶结构中,该环的 B 因子高于整体平均值,并在催化过程中经历构象变化。此外,辅助结构域 1 和 5 也对催化口袋有贡献,其环区(来自结构域 1 的残基 95–100 和来自结构域 5 的残基 984–988)构成了活性腔的入口。
在每个二聚体内,相邻分子的结构域 1 和 5 之间的头对尾相互作用稳定了结构(图 1E)。PISA 分析显示,二聚体界面的埋藏表面积为 4690 Ų,大多数接触为非极性接触。值得注意的是,同源二聚体中的活性位点位于相反的表面上,且暴露于溶剂中,这与二聚体、四聚体和八聚体 β-半乳糖苷酶的结构不同,在那些结构中活性位点彼此相对并埋藏在蛋白质表面之下(图 1E)。
随后,通过 DALI 服务器对 PbBGal2A 单体结构进行分析,以识别结构上最接近的蛋白质。按降序排列的匹配结果包括:来自海栖热袍菌 MSB8 的 β-半乳糖苷酶(TmLac,PDB ID: 6SD0,Z 得分为 44.3,RMSD 为 1.6 Å)、来自多形拟杆菌 VPI-5482 的 β-半乳糖苷酶(PDB ID: 3DEC,Z 得分为 44.6,RMSD 为 2.0 Å)和来自大肠杆菌 K-12 的 β-半乳糖苷酶(PDB ID: 7BTK,Z 得分为 44.2,RMSD 为 1.8 Å)。所有这些结构都属于 GH2 家族,具有相似的结构域排列。然而,它们的寡聚组装方式不同,这可能是由于某些环区的微小变异可能导致完全不同的寡聚体排列和底物特异性(图 1E)。寡聚结构的形成对于 GH2 家族 β-半乳糖苷酶的功能至关重要。
GH2家族β-半乳糖苷酶遵循通用的双置换催化机制,其中E514作为亲核试剂,E443作为酸碱催化剂。在GOS合成反应中,亲核试剂攻击乳糖的半乳糖基部分,形成共价的酶-底物中间体并释放葡萄糖基单元。随后,另一个乳糖分子作为半乳糖基受体,在酸碱催化剂通过去质子化作用的促进下,半乳糖基被转移到受体上。尽管E514是严格保守的,但与TmLac(PDB: 6SD0)、EcLac(PDB: 7BTK)和BgaD(PDB: 4YPJ)结构中的对应残基相比,PbBGal2A结构捕获了E443的翻转构象,表明在催化过程中酸碱催化剂发生了侧链翻转机制(图2A-D)。这种构象还导致在传统催化腔下方形成了一个额外的溶剂可及裂缝,该裂缝主要由酸性氨基酸组成。该腔体强烈的酸性特征促进了碳水化合物底物的结合,其扩大的体积可能使得更大的半乳糖基受体能够更有效地结合,并增强产物的解离。因此,与EcLac和TmLac相比,PbBGal2A实现了更高的GOS转化率。此外,来自环状芽孢杆菌ATCC 31382的BgaD表现出更扩展的催化口袋,这与其高转糖基能力相关,其GOS最高产率达到63.5%(图2D)。残基H331和H517被认为起着稳定过渡态的作用。与同源的GH2家族β-半乳糖苷酶相比,H331在结构上是保守的,而位于催化口袋入口处的H517,其侧链发生了约90°的旋转。此外,门控残基E469的构象变化,其特征是其侧链远离活性中心移动,导致催化口袋入口扩大且酸性增加。
对 apo 酶及其与底物、中间体和产物复合物结构的分析表明,参与配体结合的主链残基没有发生移动,但其侧链构象在催化反应的不同阶段可能表现出微小变化。将分别模拟底物和中间体的乳糖 (图 2E 和 F) 和 oNPG对接到 PbBGal2A 活性位点的计算模拟表明,存在一种识别模式,其中半乳糖基部分结合到 -1 亚位点,葡萄糖基部分结合到 +1 亚位点。如图 2E 和 F 所示,葡萄糖部分的羟基与 D195、H392 和 N442 形成氢键,半乳糖基部分通过与 Y491、E514 和 W545 的亲水相互作用而稳定。酶分子 5 Å 范围内的其他残基,包括 N97、V98、H365、S444、M490、H517、E546、F578、D581、S984 和 C985,可能在催化反应过程中与 PbBGal2A 参与疏水相互作用或范德华接触。
为提升GOS合成效率,依据引言部分概述的三种策略,对PbBGal2A催化腔周围选定的残基进行了定点诱变。在+1亚位点,将V98、M490、H365和H392替换为苯丙氨酸,旨在与吡喃葡萄糖环建立π-π堆积相互作用(图2E,策略1)。在-1亚位点,分别将N97、F578、S984、W545、C985和Y491替换为半胱氨酸、丝氨酸、天冬氨酸、苯丙氨酸、丝氨酸和苯丙氨酸,以降低糖苷结合位点对半乳糖基部分的结合亲和力(图2E,策略2)。此外,将位于-1亚位点的几个亲水性残基(C985、S984、His517、D195和H331)以及门控残基E469突变为疏水性异亮氨酸和/或缬氨酸。这一修饰旨在通过创造更疏水的微环境并加强对特定水通道的控制,来提高PbBGal2A的转糖基转化率,并最大限度地减少GOS的二次水解(图2F,策略3)。
使用oNPG作为底物评估了所有突变酶的水解活性。与野生型相比,所有突变体的相对活性均降至50%以下,表现出降低或显著降低的活性,证实了目标残基在水解催化中的关键作用(图3A)。随后,在最佳条件(40°C,pH 7.5)下测定了各突变体合成GOS的转糖基能力。考虑到每个突变体的峰值产率可能出现在不同时间点,连续监测反应24小时,以考察GOS产率随时间的变化。通过HPLC测得的如图3B所示。与野生型相比,大多数突变体的GOS产量都有所增加,这与其水解活性的降低是一致的(图3A)。位于+1和-1亚位点的残基都有助于提高PbBGal2A的转糖基能力。在众多突变体中,H331V的产率最高,达到76.57%,其次是E469V(64.17%)和H517I(61.17%)。H331V、E469V和H517I的GOS产率分别比野生型(47.9%)高出28.67%、16.27%和13.2%。大多数β-半乳糖苷酶的GOS产率在50%或以下(表1)。据报道,H331V的GOS产量是迄今为止的最高水平。值得注意的是,双突变体C985V-H517I和C985I-H517V的GOS产量相比单突变H517I/V有所降低,这表明引入C985突变会削弱活性。
在PbBGal2A结构中,H331和H517可能影响过渡态的形成,而E469可能调节底物进入催化口袋。因此,将这些残基突变为疏水性以排斥水分子,导致GOS合成有更大程度的增加。使用GROMACS2023测定了PbBGal2A的底物结合自由能。与野生型(-31.28 kcal/mol)相比,突变H331V、E469V和H517I导致与乳糖的结合能降低(分别为-13.6、-7.84和-7.317 kcal/mol),表明这些突变倾向于催化转糖基作用而非水解作用。这些结果表明,改造活性位点的氨基酸可以有效增强PbBGal2A生产GOS的能力。
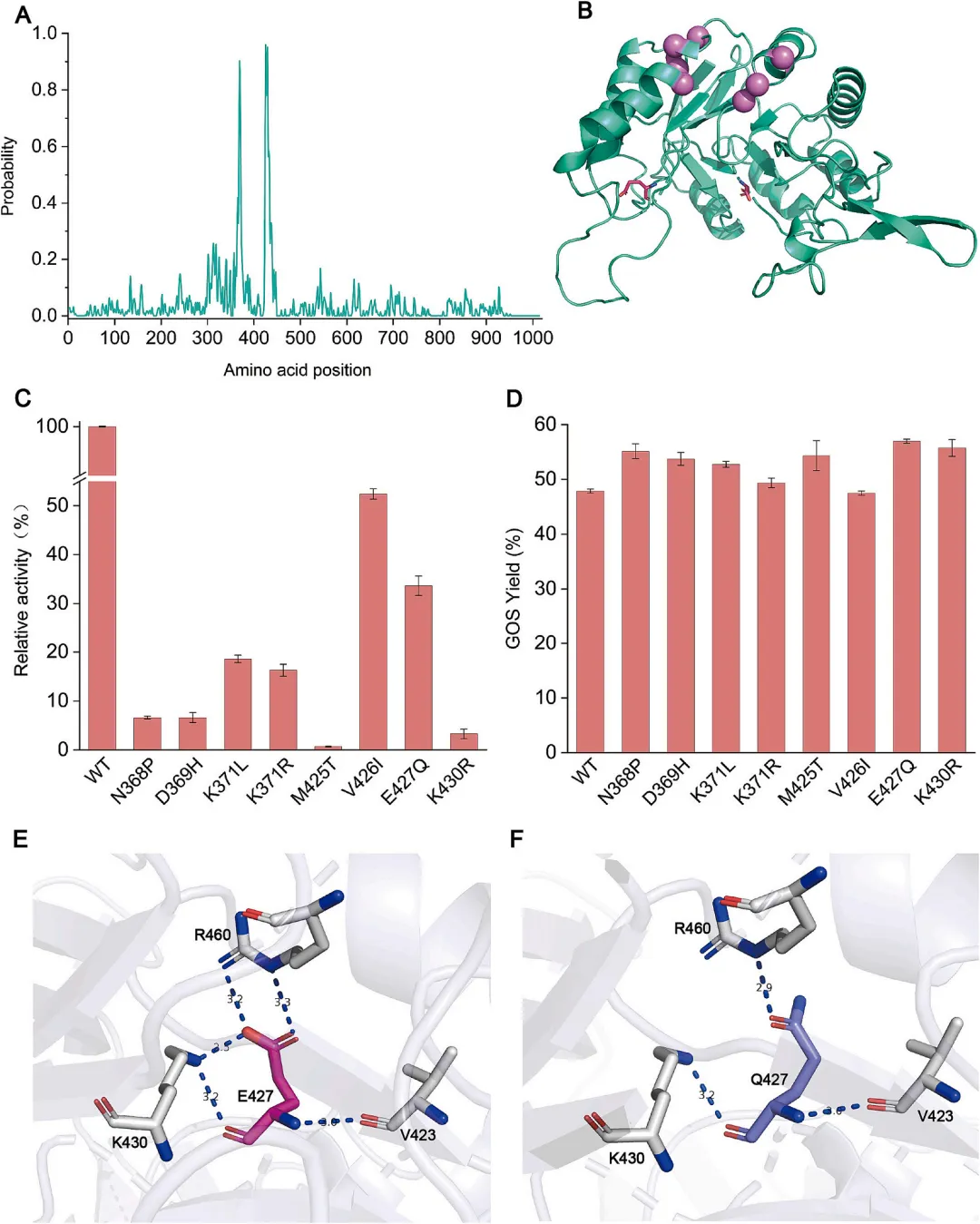
影响蛋白质结构和功能的氨基酸残基遍布整个蛋白质,从活性位点到蛋白质表面。不同研究的数据表明,远端残基通过影响活性位点残基的极性、质子传递特性、静电环境、空间排列和柔性,在酶催化中起着至关重要的作用 。为了识别远离催化中心但可能影响 PbBGal2A 催化效率的残基,应用 MECE 平台预测了每个残基有助于提高催化能力的概率,该平台提供了源自分子进化特征的突变评分指数(图 4A)。选择概率得分≥0.8 的前七个残基作为候选突变位点,以提高 PbBGal2A 的 GOS 合成能力。结构分析表明,这些残基位于催化核心结构域 3 中,距离催化中心约 14 Å(图 4B)。
基于结构可比的 β-半乳糖苷酶的序列比对,将上述七个氨基酸突变为相似残基或在其他序列中出现频率更高的残基,产生了 N368P、D369H、K371R、K371L、M425T、V426I、E427Q 和 K430R 替换。这八个突变体被表达和纯化,并使用 oNPG 作为底物定量其活性。如图 4C 所示,与野生型相比,每个突变体的活性均降至 50% 或更低,证明 MECE 策略鉴定的远端位点有助于调节蛋白质功能。随后,使用 TLC和 HPLC(图 4D)测量并分析了每个远端位点突变体的 GOS 产量。除 V426I 外,八个突变体中有七个表现出不同程度的 GOS 产量提高(49.35%–56.97%)。其中,E427Q 的 GOS 产率最高,比野生型高出约 9%。这些结果也证明了 MECE 平台对 GH 家族蛋白质的预测准确性。结构分析表明,E427 与 R460 形成 3.2 和 3.3 Å 的双齿氢键,而其羰基氧与 K430 建立极性接触。用 Gln 替换 E427 会破坏局部相互作用,并可能对活性位点产生长程效应,从而影响其 GOS 产量(图 4E 和 F)。

为研究活性位点与远端位点对PbBGal2A合成GOS的联合效应,构建了十个双突变体和一个在催化腔和远端位置均携带有益突变的三突变体(图5A)。其中,H331I-D369H突变体的活性几乎检测不到,而H331V-E427Q、C985V-D369H、C985V-E427Q和H331V-W545F-E427Q分别保留了野生型酶活性的4.56%、14.07%、41.14%和33.56%(图5B)。值得注意的是,W545F-E427Q表现出最高的活性,为野生型的107.89%,分别比单个突变体W545F和E427Q提高了2.13倍和3.2倍。在W545F-D369H中也观察到了类似的趋势,其活性分别比W545F和D369H提高了2.06倍和14.92倍。这些结果表明,在W545F中引入远端突变可能对PbBGal2A的水解活性产生上位效应。在GOS合成活性方面,很明显,与野生型相比,所有组合突变都导致了GOS产量的增加。突变体H331I-D369H表现出最高的GOS产率,为64.54%(图5C)。进一步分析了最优活性位点突变体H331V、远端位点突变体E427Q及其组合突变体在酶添加量5 U/mL、35%乳糖、40°C、pH 7.5条件下的GOS合成反应过程。在所有反应中,GOS在初始阶段快速生成,但随后发生再水解。值得注意的是,PbBGal2A野生型的GOS产率在8小时达到峰值47.9%,而H331V、E427Q和H331V-E427Q分别在4小时、4小时和8小时达到最大产率,与野生型相比分别提高了1.60倍、1.19倍和1.32倍(图5D)。这些发现表明,活性位点和远端位点的突变单独作用均能提高GOS产率和GOS合成效率。此外,可以观察到野生型和突变酶在GOS的二次水解方面表现出相似的趋势,其中H331V在24小时达到最高的GOS产率76.57%。综上所述,这些结果暗示,对于PbBGal2A的GOS合成,活性位点和远端位点的突变组合并不容易产生协同效应。
为了探究组合突变对PbBGal2A催化的机制作用,对野生型和双突变体H331V-E427Q进行了MD模拟。通过监测RMSD分析了PbBGal2A及其突变体在313.15 K下20 ns模拟期间的稳定性(图5E)。此外,使用均方根波动评估了特定区域和残基的柔性(图5F和G)。结果表明,H331V-E427Q在催化口袋周围的环95–105(结构域1)和环389–422(结构域3)中表现出增加的刚性,表明远端位点可能通过促进活性位点的稳定性来增强催化功能。
本研究报道了PbBGal2A的冷冻电镜结构,这是一种因其高转糖基能力而具有重要工业应用价值的GH2家族酶。该结构揭示了酸碱催化剂E443的翻转构象和一个扩大的酸性催化口袋,这可能改善了碳水化合物底物的结合。采用基于结构和机器学习的诱变策略,鉴定了有益的活性位点和远端突变。由此产生的突变体H331V表现出76.57%的最高GOS产率,标志着迄今为止报道的最高产率。MD分析表明,远端突变增强了催化口袋周围环区的刚性,从而提高了PbBGal2A的转糖基能力。这些发现阐明了PbBGal2A的结构和催化机制,为改造定制化β-半乳糖苷酶及其他相关GH家族酶的转糖基活性提供了有效策略。