近日,南京农业大学动物科技学院许志明博士联合 OHRG课题组Prof. dr. Fèlix Faming Wang等人在英文开源期刊《Animal Advances》发表题为 “Fecal microbiota transplantation in gastrointestinal diseases: linking human, livestock and poultry health” 的综述文章,旨在系统梳理粪菌移植技术在人类及畜禽胃肠道疾病中的应用进展,深入探讨其在 “全健康” 框架下连接人类、家畜与家禽健康的潜在价值与未来方向。
🐮 肠道里的 “健康密码”:粪菌移植如何连接人与动物的健康?
想象一下,你的肠道里住着数以万亿计的微生物,它们形成一个复杂而微妙的 “社会”,影响着你的消化、免疫、甚至情绪。这个 “社会” 就是肠道微生物群,常被科学家称为人体的 “第二基因组”。当这个 “社会” 的平衡被打破,即发生菌群失调,就可能引发一系列疾病。那么,有没有办法重塑这个失衡的“社会”呢?一种古老而又现代的技术给出了答案:粪菌移植(fecal microbiota transplantation)。
本文将这一技术的应用视野从人类拓展到了家畜与家禽,为我们描绘了一幅 “全健康” 理念下的全新图景。
什么是粪菌移植?
粪菌移植,简单来说,就是将健康捐赠者的粪便中的功能菌群,移植到患病者的肠道内,以期重建后者的肠道菌群,恢复微生态平衡,从而达到治疗疾病的目的。
这听起来或许有些不可思议,但其历史渊源可追溯至中国古代的医学实践,如使用人粪或动物粪便制剂治疗严重肠道疾病。如今,随着现代微生物学和测序技术的飞速发展,粪菌移植已从经验性的尝试,转变为有科学依据的治疗手段。从最初通过结肠镜进行移植,到现在可以制成标准化的、口服的冷冻胶囊,粪菌移植的安全性和可及性得到了极大提升。
目前,粪菌移植已被证明对多种消化道疾病有效,尤其是对复发性艰难梭菌感染,其治愈率可达80%-90%,已成为该疾病的首选治疗方案之一。此外,它在溃疡性结肠炎、肠易激综合征等疾病的治疗研究中也展现出巨大潜力。
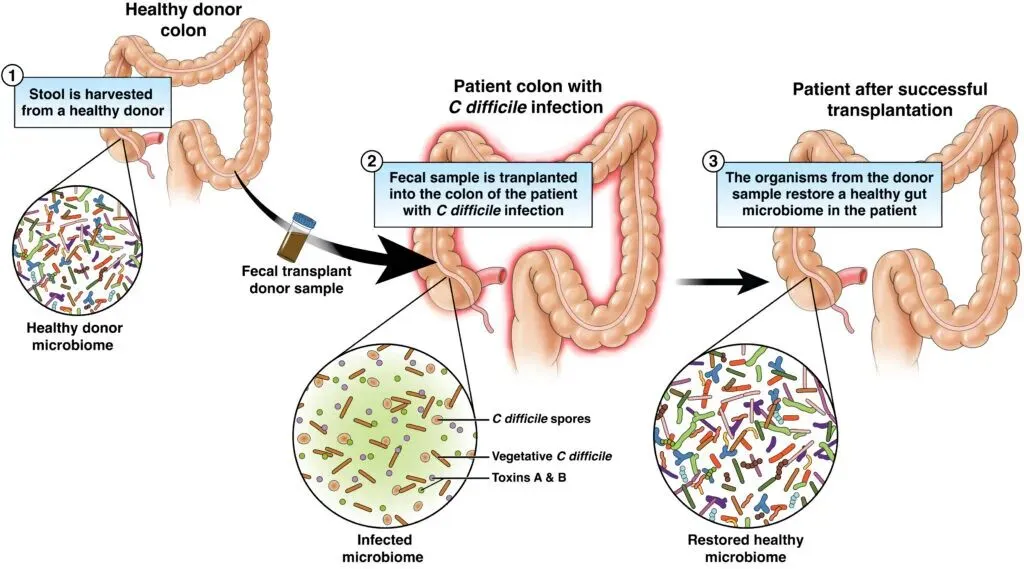
Figure 1 | 粪菌移植(fecal microbiota transplantation)示意图。
动物的肠道菌群,人类的健康 “外援”?
这篇综述的一个核心亮点在于,它深入探讨了动物肠道菌群与人类健康之间千丝万缕的联系。研究指出,动物(包括家畜、家禽和伴侣动物)粪便中的微生物群落与人类的肠道菌群存在着显著的生态位互补性。长期与动物接触,可能会丰富人类肠道菌群的多样性,增强免疫功能,甚至降低过敏和自身免疫疾病的风险。
研究提到,宠物狗粪便中的一种名为阿克曼氏菌(Akkermansia muciniphila)的有益菌,可能通过空气颗粒物传播给人类,刺激免疫细胞分泌白细胞介素-10,从而有助于降低儿童过敏性哮喘的发病率。又如,反刍动物粪便中的纤维素分解菌(如反刍兽胃球菌,Ruminococcus)在进入人体肠道后,可能激活相关通路,促进短链脂肪酸的合成,进而对肥胖人群的胰岛素水平产生积极影响。这为我们打开了一扇新的窗户:动物粪便微生物库,或许可以成为人类肠道菌群的重要外源性补充,成为开发新一代微生态制剂的宝贵资源库。
当然,这种跨物种的微生物交换是一把 “双刃剑”。动物粪便中也可能携带致病菌,如产志贺毒素的大肠杆菌和空肠弯曲杆菌,这对粪菌移植的供体筛选提出了极其严格的挑战。
Figure 2 | 跨物种微生物交换及其对患病受体潜在益处的概念模型。源自牛、猪、鸡和啮齿类动物等供体粪便的微生物,可能影响患病宿主的肠道菌群。通过促进有益共生菌和抑制致病菌,跨物种微生物交换可将失调的微生物群落转变为更为平衡的菌群,进而对肠道屏障完整性、免疫调节和代谢稳态产生有益影响。
粪菌移植在畜牧业中的潜力:减抗增效的“新武器”
在动物生产中,粪菌移植技术的应用同样方兴未艾。其核心目标与人类医学一脉相承,并针对畜牧业的特点进行了拓展,主要包括:
疾病防控:在养猪业中,抗生素的使用常导致仔猪肠道菌群紊乱,引发腹泻。研究表明,粪菌移植可以帮助重建仔猪的肠道菌群,增强肠道屏障,减轻炎症,从而有效缓解抗生素相关性腹泻。
提升生长性能:通过将高饲料转化效率肉鸡的肠道菌群移植给蛋鸡或普通鸡,可以成功建立以厚壁菌门、乳杆菌和双歧杆菌为特征的有益菌群,进而增强碳水化合物代谢和抗菌能力,最终改善肠道健康,促进生长。
改善整体健康:移植的菌群可以通过其代谢产物(如短链脂肪酸)影响骨骼发育(如增加胫骨长度)、调节脂质代谢、增强肠道免疫防御,甚至通过“菌群-肠-脑轴”影响动物的行为。
粪菌移植是如何工作的?
粪菌移植的作用机制复杂而精妙,并非简单地 “换一批细菌”。目前的研究认为,它主要通过以下几个途径发挥作用:
恢复生态平衡:移植的健康菌群像一支 “维和部队”,重新占领肠道生态位,抑制机会致病菌(如艰难梭菌)的过度生长。
补充有益代谢物:健康菌群能产生丰富的短链脂肪酸、次级胆汁酸等有益代谢物,为肠道细胞提供能量,维持肠道健康。
强化肠道屏障:通过促进黏蛋白、紧密连接蛋白和分泌型免疫球蛋白A的产生,加固肠道物理和免疫屏障,防止 “肠漏”。
调节宿主免疫:菌群信号可以调节树突状细胞介导的免疫通路,促进调节性T细胞的产生,平衡促炎和抗炎细胞因子,最终减轻炎症,维持肠道稳态。
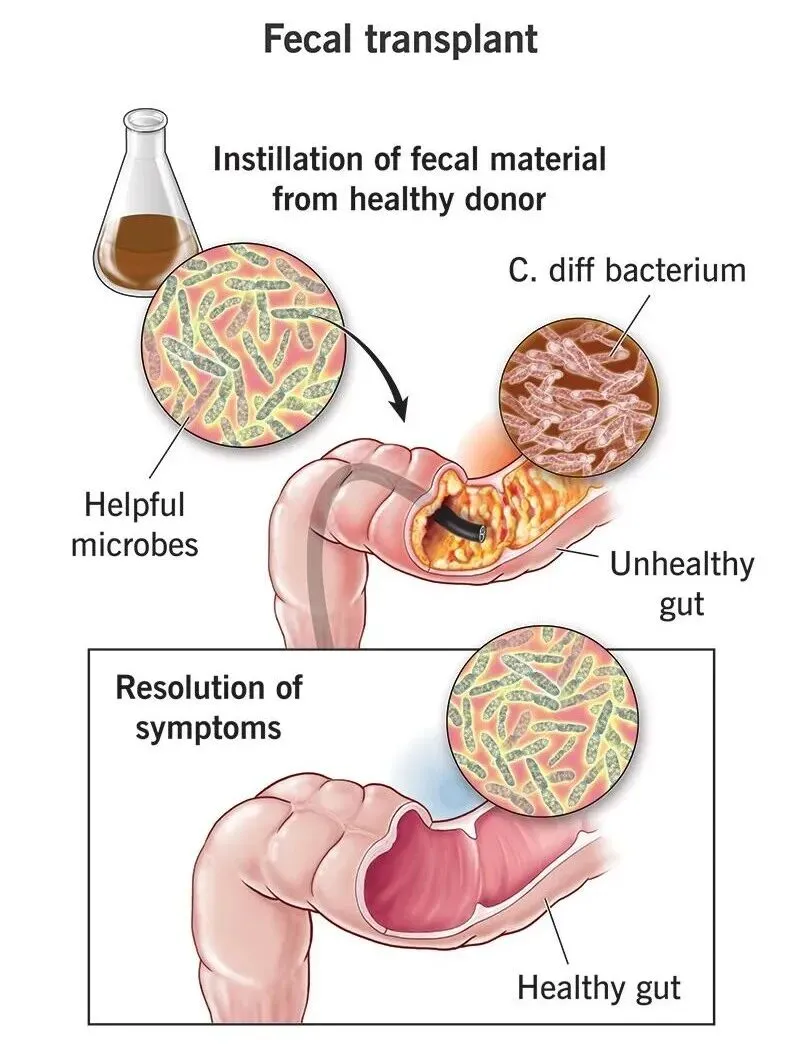
Figure 3 | 健康结肠内的有益微生物有助于治愈患病结肠。
安全与挑战:迈向标准化
尽管前景广阔,但粪菌移植并非毫无风险。短期可能出现一过性腹泻、腹胀;长期则存在诱导代谢紊乱(如肥胖)、增加自身免疫疾病风险,甚至传播抗生素耐药基因的可能。因此,建立标准化的操作流程至关重要:
供体筛选:这是保障安全的第一道关卡。除了常规的健康检查和病原体筛查外,供体还需满足特定的微生物组质量标准,如产丁酸菌(如普拉梭菌)的相对丰度要求。
样本制备:需在严格的厌氧条件下进行,以保证菌群活性。常用的冻存方法能较好地保存菌群活力。
移植途径:需根据动物种类和疾病类型选择合适的途径,如口服灌胃、结肠镜、直肠给药、或通过饲料/饮水喷洒等。
未来展望:从 “以病治病” 到 “以菌促健”
这篇综述为我们描绘了粪菌移植技术的未来蓝图。在“全健康”理念的指导下,未来研究将聚焦于:
优化供体筛选与制备工艺,开发针对人类、家畜和家禽的标准化方案。
阐明作用机制,识别关键的功能菌株和代谢物,揭示微生物与宿主相互作用的奥秘。
开发下一代微生态疗法,如基于粪菌移植原理,设计由特定菌株组合而成的 “合成菌群” 或 “定义明确的微生物治疗产品”,以提高安全性、一致性和监管可行性。
拓展应用领域,将粪菌移植从治疗胃肠道疾病,拓展到精准营养、神经行为异常、呼吸道疾病、生殖障碍乃至生长发育迟缓等更广泛的领域。
最终,通过整合人类、家畜和家禽的微生物组研究,我们有望构建一个互联互通的健康框架。这个框架不仅能推动微生物组知识向生物安全、干预设计和疾病管理的实用标准转化,还能为与动物健康、食品生产和公共卫生相关的跨部门政策提供信息。
论文结语
粪菌移植,这项连接着古老智慧与现代科技的疗法,正从实验室走向临床,从人类拓展到动物,从疾病治疗迈向健康管理。它不仅是撬开复杂肠道菌群奥秘的一把钥匙,更是践行 “全健康” 理念的生动实践。未来,随着技术的不断成熟和监管框架的完善,粪菌移植有望在保障人类和动物健康、促进可持续发展的道路上,发挥出更加重要的作用。
论文链接:https://www.maxapress.com/animadv/articles
OHRG: Advancing One Health with Excellence
订阅按赞并分享OHRG公众号,获取最新全健康前沿研究及科研实用干货!