湖南农业大学:红茶核桃肽复合物制备及对环磷酰胺诱导免疫抑制的缓解应用
1.专利号:CN121489044A,专利名称:红茶与核桃肽复合物及其制备和应用,申请日:2025.09.18,公布(开)日:2026.02.10,申请人:湖南农业大学本发明公开了红茶与核桃肽复合物及其制备方法和在缓解环磷酰胺诱导的免疫抑制中的应用。研究发现,FT‑WP治疗显著逆转环磷酰胺诱导的小鼠的体重、胸腺和脾脏指数,改善空肠CD4+T细胞亚群平衡,以及平衡细胞因子和免疫球蛋白的水平。此外,研究表明, FT‑WP影响甘氨酸、丝氨酸和苏氨酸代谢、嘧啶代谢、蛋白质消化和吸收代谢等代谢途径和胆碱、 三甲基胺‑N‑氧化物、丙硫菌唑、硬脂酰肉碱、前列腺素F2.β等代谢物的调节。红茶与核桃肽复合型食品可缓解环磷酰胺诱导的免疫抑制,调节异常的血清代谢。1.2.1 FT‑WP对免疫抑制小鼠体重和脏器指数的影响小鼠体重的体重变化如图2中(A)所示。结果显示空白组(CK)小鼠体重在实验过程 中呈正常上升趋势,而注射环磷酰胺3天后,模型组(MD)(P<0.01),盐酸左旋咪唑组(LH)、核 桃肽组(WP)和低、中、高剂量组(LTD、MTD、HTD)(P<0.001)小鼠体重极显著下降,说明模型建 立成功,环磷酰胺对小鼠机体损伤严重。 [0070] 连续10天灌胃盐酸左旋咪唑,核桃肽、和不同剂量的FT‑WP后,小鼠体重均能较好 的恢复,提示阳性药物组(LH)、核桃肽组(WP)、和低、中、高剂量组(FT‑WP)可减轻环磷酰胺 所致肝损伤小鼠体重的下降。胸腺指数、脾脏指数如图2中(B)、(C)所示,在14天的喂养期 后,与空白组(CK)相比,环磷酰胺诱导小鼠胸腺指数显著降低(p<0.05),说明环磷酰胺可以 破坏免疫器官的功能。与模型组(MD)相比,FT‑WP组胸腺指数和脾脏指数均显著升高(p< 0.05),提示FT‑WP可改善环磷酰胺诱发的免疫器官损伤。1.2.2 FT‑WP对免疫抑制小鼠脾脏及空肠组织病理变化的影响脾脏是重要的免疫器官,用环磷酰胺处理的小鼠的免疫状况可以通过检查脾脏的组织学结构来评估。如图3中(A)和(B)所示,空白组(CK)细胞排列整齐紧密,白细胞数量较多;脾小结发育良好,结构清晰,白髓和红髓界限明显,边缘区无增生,生发中心极少。与空 白组(CK)相比,模型组(MD)被膜增厚进入到脾实质内形成小粱,边缘区增生明显,边缘区增多增厚,脾小结受损严重,淋巴样滤泡增生导致白髓与红髓界限模糊。白髓异常萎缩,说明淋巴组织受损,淋巴细胞数量减少,生发中心数量较多,脾小结破损严重,红髓区充血严重。 与模型组(MD)相比,高剂量组(HTD)组生发中心不明显,边缘区厚度与模型组(MD)相比明显减少,红髓有轻微充血,白髓面积增大且内部淋巴细胞排列较密集,白髓和红髓分布比例趋近于正常组;核桃肽组(WP)、低剂量组(LTD)、中剂量组(MTD)和组脾脏的边缘区和白髓数量均有明显改善,但不及高剂量组(HTD)的恢复效果明显。CD4+T细胞是重要的免疫细胞,在接受抗原刺激后可分化为Th细胞的不同亚型并执行各种功能。环磷酰胺可通过抑制T细胞分化影响小鼠肠道免疫状态。因此,通过免疫组织化学研究了各组中 CD4+ T 细胞的面积。如图3中(B)所示,CD4+T细胞被染色成棕色。很直观可见空白组和各给药组棕色细胞较多,模型组几乎无棕色细胞。MD组CD4+T细胞表达明显低于CK组(P<0.05)。FT‑WP灌胃后CD4+T水平显著升高(P<0.05),HTD组升高幅度最高。因此,FT‑WP可以有效改善环磷酰胺诱导的空肠免疫中CD4+T细胞水平的平衡。1.2.3 FT‑WP对免疫抑制小鼠血清生化指标的影响 细胞因子主要是由免疫细胞或其他刺激物诱导的小分子可溶性蛋白质,参与不同的免疫功能。基于上述发现,我们进一步研究了血清中炎性细胞因子和免疫因子IL‑6、IFN γ 、IgM、IgG 水平如图2(D‑G)所示,与CK组相比,MD组中血清中IL‑6、IFN‑ γ 、IgM、IgG水平显著降低(p<0.05);与MD组相比,LH组、WP组、和FT‑WP组血清IL‑6、IFN‑ γ 、IgM和IgG水平显著升高(p<0.05);并且在高剂量下有更好的效果。说明Cy能显著抑制小鼠免疫因子分泌, LH、WP、和FT‑WP 治疗在一定程度上逆转了免疫因子的减少。1.2.4 FT‑WP对免疫抑制小鼠血清代谢的调节作用 基于前面实验结果分析发现,FT‑WP高剂量(HTD)研究效果最佳。通过超高效液相色谱‑质谱法进行非靶向代谢组学进一步分析,比较CK组、MD组和HTD组血清中的代谢物。在阳离子(图4中A和B)和阴离子模式下(图4C和D),正交偏最小二乘判别分析(OPLS‑DA)分析显示,MD组与CK组和HTD组明显分开,表明MD组的血清代谢物与CK组和HTD组相比有显著差异。以及在阳离子(图4E和F)和阴离子模式下(图4中G和H)置换检验分析中,所有经过置换后的Q2值均低于原始模型的Q2值,表明该模型预测结果可靠,具有较好的解释和预测能力, 不存在过拟合,本实验可继续后续分析。在混合模式下,采用VIP>2,P<0.05的选择标准;| log2倍数变化|>1,火山图表明,与CK组相比,MD组诱导了134种代谢物的变化,其中82种代谢物显著上调,52种代谢物显著下调(图4中I)。此外,与MD组相比,HTD组诱导了139种代谢物的变化,其中20种代谢物上调,119种代物下调(图4中J)。CK组与MD组、MD组与HTD组以及 CK组与HTD组的差异代谢物数量分别为134、139、152(图4中K)。分层聚类热图分析显示,三组之间的血清代谢物谱存在显著差异(图5中A和B)。这 些差异代谢物分别在HMDB数据库和KEGG数据库中进行分类。基于HMDB,CK与MD,MD与HTD相比前四个类别是羧酸及其衍生物、脂肪酰基、苯及其取代衍生物、有机氧化合物,各占9%以上(图5中C和D)。KEGG富集分析显示,根据化合物数量,富集途径排名前三位的是氨基酸代谢、脂类代谢、和碳水化合物代谢。MD组和CK组之间的差异代谢物在KEGG通路中显著富集前 三位最显著的富集通路是精氨酸和脯氨酸代谢、D‑氨基酸代谢、甘氨酸、丝氨酸和苏氨酸代 谢途径。与MD组与HTD组调节的差异代谢物显著富集于甘氨酸、丝氨酸和苏氨酸代谢、嘧啶 代谢、蛋白质消化和吸收代谢等途径(图5中E和F)。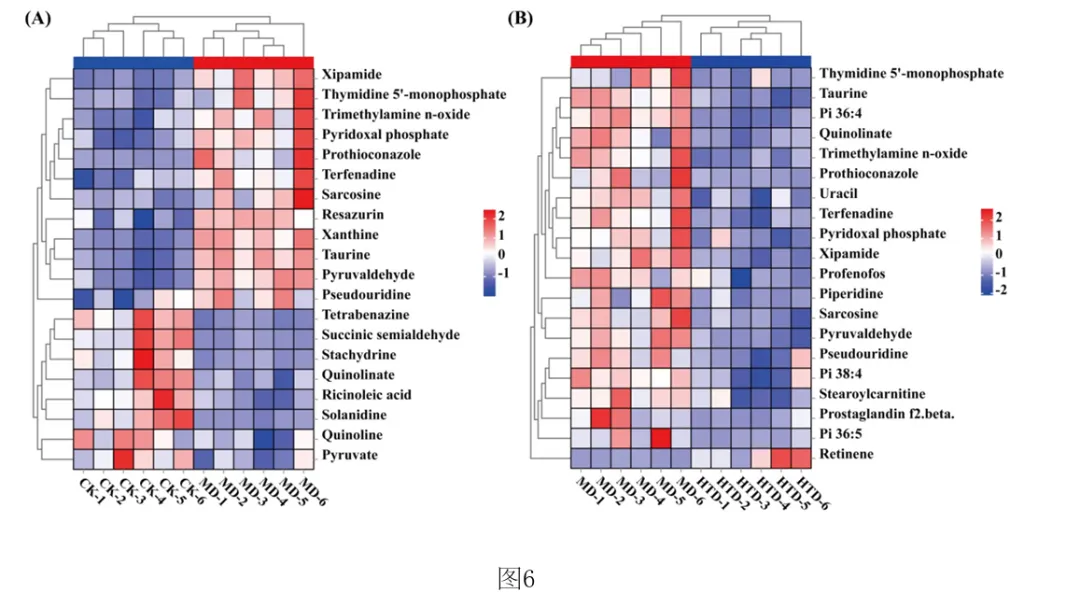 选择基于OPLS‑DA模型具有前20个差异代谢物作为潜在的生物标记物(VIP > 2)。 如热图6(A) 所示,所有20种化合物在CK组和MD组之间表现出显著差异(p<0.05),与CK组相 比,MD组有12种化合物增加(希帕胺Xipamide、Thymidine 5'‑monophosphate胸腺嘧啶5’一 磷酸、Trimethylamine n‑oxide三甲基胺‑N‑氧化物、Pyridoxal phosphate磷酸吡哆醛、 Prothioconazole丙硫菌唑、Terfenadine特非那定、Sarcosine肌氨酸、Resazurin刃天青、 Xanthine黄嘌呤、Taurine牛磺酸、Pyruvaldehyde丙酮醛、Pseudouridine假尿(嘧啶核) 苷),其余8种化合物减少(Tetrabenazine四苯喹嗪、Succinic semialdehyde琥珀酸半醛、 Stachydrine水苏碱、Quinolinate羟基喹啉铜、Ricinoleic acid蓖麻油酸、Solanidine茄 啶、Quinoline喹啉、Pyruvate丙酮酸盐);如热图6(B)所示,HTD组和MD组之间表现出显著差 异(p<0.05),与MD组相比,HTD组有19种化合物减少(Thymidine 5'‑monophosphate胸腺嘧 啶5’一磷酸、Taurine牛磺酸、Pi 36:4、Quinolinate羟基喹啉铜、Trimethylamine n‑oxide 三甲基胺‑N‑氧化物、Prothioconazole、Uracil尿嘧啶、Terfenadine、Pyridoxal phosphate、Xipamide、Profenofos丙溴磷、Piperidine哌啶、Sarcosine、Pyruvaldehyde、 Pseudouridine、Pi 38:4、Stearoylcarnitine硬脂酰肉碱、Prostaglandin F2.β前列腺素 F2.β、Pi 36:5),一种化合物增加(Retinene视网醛)。其中, Xipamide、Thymidine 5' monophosphate、Trimethylamine n‑oxide、Pyridoxal phosphate、Prothioconazole、 Terfenadine、Sarcosine、Taurine、Pyruvaldehyde、Pseudouridine这10种代谢物在MD组显 示增加,而HTD有效改善环磷酰胺引起的代谢物水平的变化。在本研究中,环磷酰胺可诱导三甲基胺‑N‑氧化物(Trimethylamine n‑oxide, TMAO)水平升高,施用HTD,胆碱(Choline)含量降低。先前的研究表明,胆碱是三甲基胺‑N 氧化物的主要前体,胆碱被肠道微生物代谢成三甲胺(TMA),随后在肝脏氧化形成三甲胺‑ N‑氧化物。三甲基胺‑N‑氧化物与多种健康结果相关,包括全因死亡率、心血管疾病、高血压、糖尿病、癌症和肾功能疾病;三甲基胺‑N‑氧化物可以激活炎症途径,诱导活性氧(ROS) 产生,同时降低抗氧化活性,破坏细胞内氧化还原平衡;三甲基胺‑N‑氧化物会导致一系列生物功能障碍,包括氧化应激、血脑屏障破坏、突触可塑性降低、炎症、线粒体功能障碍和异常蛋白质聚集;三甲基胺‑N‑氧化物已被证明通过诱导神经元衰老和加剧神经炎症和氧化应激加速大脑衰老和认知能力下降。先前的研究表明,丙硫菌唑(Prothioconazole)诱导线粒体功能障碍,可导致氧化应激和细胞凋亡,引起一些不良心血管效应,并对早期生命阶段 的斑马鱼产生发育毒性。然而灌胃FD‑WP后,胆碱含量下降,在受FD‑WP调控的代谢产物中, 与MD组相比,FD‑WP降低了三甲基胺‑N‑氧化物和丙硫菌唑水平,这表明FD‑WP可以改善环磷酰胺诱导的免疫损伤。 [0084] 与MD组相比,FD‑WP(HTD组)降低了前列腺素F2.β(Prostaglandin F2.β)、硬脂酰肉碱(tearoylcarnitine)的水平。前列腺素(PG)通过影响炎症、血管生成和免疫抑制的复杂信号通路在皮肤癌以及黑色素瘤的发病机制中起关键作用。前列腺素F2.β是前列腺素F2系列的一种异构体,属于异前列腺素类化合物。除了作为氧化应激的生物标志物外,它还充当维持生理功能稳态的介质,并参与与疾病病理过程相关的炎症和免疫反应的生物活性。 硬脂酰肉碱是一种脂肪酯类脂质分子,属于人体内源性代谢物。它在生物体内发挥着重要的角色,例如,可以作为早发先兆子痫和迟发先兆子痫的代谢组学代谢标志物。此外,硬脂酰肉碱在灌注大鼠心脏的脂肪酸链延长过程中,可以由灌注的棕榈酸酯合成而来,有研究进行多组学分析显示硬脂酰肉碱是妊娠糖尿病大鼠后代心脏代谢疾病发展的一种新的生物标志物。在HIV感染者的研究中发现,血浆中酰基肉碱的积累与这些患者在抗逆转录病毒疗法(ART)后的免疫恢复不良有关。有趣的是,MD组显示水苏碱水平下降。有研究表明水苏碱(Stachydrine)在心脑血管疾病、神经保护、抗癌、子宫调节、抗炎反应、肥胖治疗和呼吸系统疾病等方面有着重要作用。不幸的是,给药FD‑WP并没有显著改变水苏碱水平,但通过调节胆碱、三甲基胺‑N‑氧化物、丙硫菌唑、硬脂酰肉碱、前列腺素F2.β等代谢物减轻了免疫 损伤
选择基于OPLS‑DA模型具有前20个差异代谢物作为潜在的生物标记物(VIP > 2)。 如热图6(A) 所示,所有20种化合物在CK组和MD组之间表现出显著差异(p<0.05),与CK组相 比,MD组有12种化合物增加(希帕胺Xipamide、Thymidine 5'‑monophosphate胸腺嘧啶5’一 磷酸、Trimethylamine n‑oxide三甲基胺‑N‑氧化物、Pyridoxal phosphate磷酸吡哆醛、 Prothioconazole丙硫菌唑、Terfenadine特非那定、Sarcosine肌氨酸、Resazurin刃天青、 Xanthine黄嘌呤、Taurine牛磺酸、Pyruvaldehyde丙酮醛、Pseudouridine假尿(嘧啶核) 苷),其余8种化合物减少(Tetrabenazine四苯喹嗪、Succinic semialdehyde琥珀酸半醛、 Stachydrine水苏碱、Quinolinate羟基喹啉铜、Ricinoleic acid蓖麻油酸、Solanidine茄 啶、Quinoline喹啉、Pyruvate丙酮酸盐);如热图6(B)所示,HTD组和MD组之间表现出显著差 异(p<0.05),与MD组相比,HTD组有19种化合物减少(Thymidine 5'‑monophosphate胸腺嘧 啶5’一磷酸、Taurine牛磺酸、Pi 36:4、Quinolinate羟基喹啉铜、Trimethylamine n‑oxide 三甲基胺‑N‑氧化物、Prothioconazole、Uracil尿嘧啶、Terfenadine、Pyridoxal phosphate、Xipamide、Profenofos丙溴磷、Piperidine哌啶、Sarcosine、Pyruvaldehyde、 Pseudouridine、Pi 38:4、Stearoylcarnitine硬脂酰肉碱、Prostaglandin F2.β前列腺素 F2.β、Pi 36:5),一种化合物增加(Retinene视网醛)。其中, Xipamide、Thymidine 5' monophosphate、Trimethylamine n‑oxide、Pyridoxal phosphate、Prothioconazole、 Terfenadine、Sarcosine、Taurine、Pyruvaldehyde、Pseudouridine这10种代谢物在MD组显 示增加,而HTD有效改善环磷酰胺引起的代谢物水平的变化。在本研究中,环磷酰胺可诱导三甲基胺‑N‑氧化物(Trimethylamine n‑oxide, TMAO)水平升高,施用HTD,胆碱(Choline)含量降低。先前的研究表明,胆碱是三甲基胺‑N 氧化物的主要前体,胆碱被肠道微生物代谢成三甲胺(TMA),随后在肝脏氧化形成三甲胺‑ N‑氧化物。三甲基胺‑N‑氧化物与多种健康结果相关,包括全因死亡率、心血管疾病、高血压、糖尿病、癌症和肾功能疾病;三甲基胺‑N‑氧化物可以激活炎症途径,诱导活性氧(ROS) 产生,同时降低抗氧化活性,破坏细胞内氧化还原平衡;三甲基胺‑N‑氧化物会导致一系列生物功能障碍,包括氧化应激、血脑屏障破坏、突触可塑性降低、炎症、线粒体功能障碍和异常蛋白质聚集;三甲基胺‑N‑氧化物已被证明通过诱导神经元衰老和加剧神经炎症和氧化应激加速大脑衰老和认知能力下降。先前的研究表明,丙硫菌唑(Prothioconazole)诱导线粒体功能障碍,可导致氧化应激和细胞凋亡,引起一些不良心血管效应,并对早期生命阶段 的斑马鱼产生发育毒性。然而灌胃FD‑WP后,胆碱含量下降,在受FD‑WP调控的代谢产物中, 与MD组相比,FD‑WP降低了三甲基胺‑N‑氧化物和丙硫菌唑水平,这表明FD‑WP可以改善环磷酰胺诱导的免疫损伤。 [0084] 与MD组相比,FD‑WP(HTD组)降低了前列腺素F2.β(Prostaglandin F2.β)、硬脂酰肉碱(tearoylcarnitine)的水平。前列腺素(PG)通过影响炎症、血管生成和免疫抑制的复杂信号通路在皮肤癌以及黑色素瘤的发病机制中起关键作用。前列腺素F2.β是前列腺素F2系列的一种异构体,属于异前列腺素类化合物。除了作为氧化应激的生物标志物外,它还充当维持生理功能稳态的介质,并参与与疾病病理过程相关的炎症和免疫反应的生物活性。 硬脂酰肉碱是一种脂肪酯类脂质分子,属于人体内源性代谢物。它在生物体内发挥着重要的角色,例如,可以作为早发先兆子痫和迟发先兆子痫的代谢组学代谢标志物。此外,硬脂酰肉碱在灌注大鼠心脏的脂肪酸链延长过程中,可以由灌注的棕榈酸酯合成而来,有研究进行多组学分析显示硬脂酰肉碱是妊娠糖尿病大鼠后代心脏代谢疾病发展的一种新的生物标志物。在HIV感染者的研究中发现,血浆中酰基肉碱的积累与这些患者在抗逆转录病毒疗法(ART)后的免疫恢复不良有关。有趣的是,MD组显示水苏碱水平下降。有研究表明水苏碱(Stachydrine)在心脑血管疾病、神经保护、抗癌、子宫调节、抗炎反应、肥胖治疗和呼吸系统疾病等方面有着重要作用。不幸的是,给药FD‑WP并没有显著改变水苏碱水平,但通过调节胆碱、三甲基胺‑N‑氧化物、丙硫菌唑、硬脂酰肉碱、前列腺素F2.β等代谢物减轻了免疫 损伤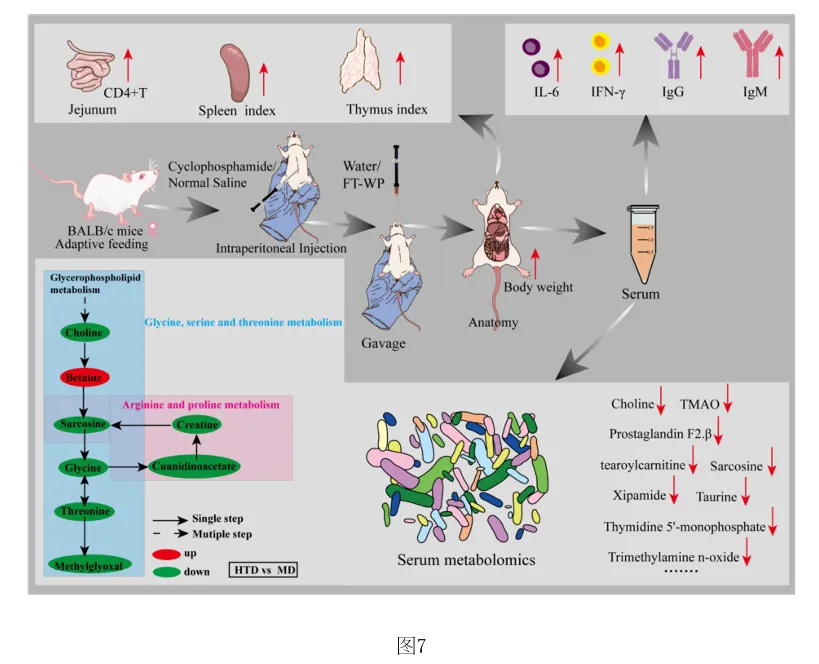 FD‑WP能改善环磷酰胺诱导的免疫抑制相关机制(如图7)。
FD‑WP能改善环磷酰胺诱导的免疫抑制相关机制(如图7)。