(一)寄主大叶白蜡的化学防御响应
研究人员对比了受害与未受害大叶白蜡韧皮部中的羟基酪醇含量。结果发现,未受害树木韧皮部的羟基酪醇浓度(5867.22 ± 208.52 ng/µL)显著高于受害虫道内的浓度(2864.09 ± 194.23 ng/µL)。这初步揭示了小线角木蠹蛾取食过程可能伴随着对防御物质的消耗或降解。
图 1未受侵染与小线角木蠹蛾侵染的大叶白蜡韧皮部中羟基酪醇浓度的显著差异。图中不同字母表示基于 t 检验分析的统计学显著差异(P < 0.05)。
(二)羟基酪醇对幼虫的毒性评估
死亡率:随着羟基酪醇浓度增加,幼虫死亡率显著上升,在 6000 ng/µL 时死亡率达到约 50%。
体重变化:高浓度的羟基酪醇显著抑制了幼虫的体重增长。
毒力值:计算得出其半致死浓度 LC50 为 5754.39 ng/µL 。
表 1. 取食不同浓度羟基酪醇后小线角木蠹蛾的死亡率存在显著差异
注:小写字母表示死亡率的差异,大写字母表示基于ANOVA和Levene ' s检验的处理间校正死亡率( P < 0.05)的差异。校正死亡率是基于羟基酪醇浓度为4000 ng/µL 和5000 ng/µL 与6000 ng/µL ( F = 13.206, df = 2 , P < 0.006)之间的ANOVA比较。
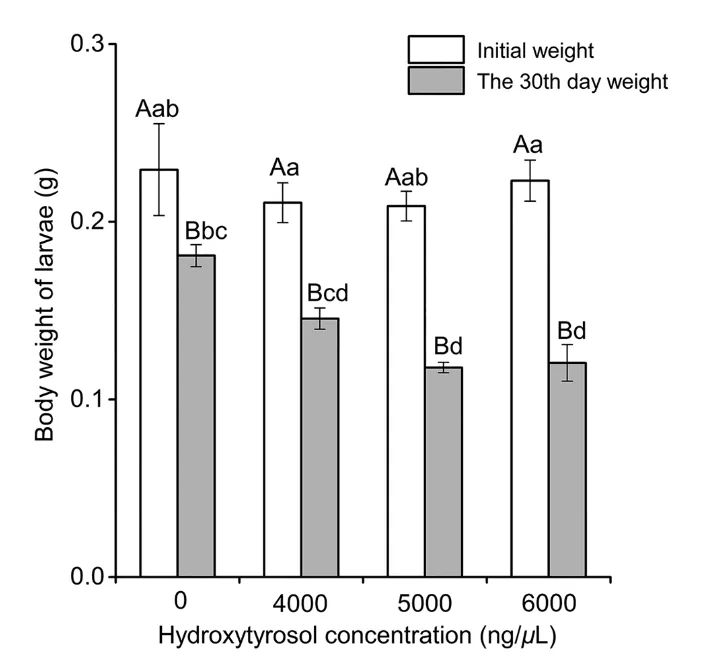
图 2. 取食添加不同浓度(0、4000、5000 和 6000 ng/µL)羟基酪醇的人工饲料后小线角木蠹蛾的体重变化。体重差异采用单因素方差分析(ANOVA)及 Duncan 氏法进行事后两两比较。大写字母表示相同浓度下不同时间的体重差异,小写字母表示不同浓度组间的体重差异(P < 0.05)。
(三)肠道菌群介导的降解机制
体内降解实验:使用抗生素清除肠道微生物后,幼虫粪便中的羟基酪醇浓度(235.44 ng/µL)显著高于对照组(35.16 ng/µL)。这证明了肠道微生物在体内降解羟基酪醇中的核心作用。
体外分离与鉴定:从肠道中分离出的5株优势菌(铜绿假单胞菌、普罗威登斯菌、沙雷氏菌、米罗氏菌、大肠杆菌)均展现出降解能力。其中,沙雷氏菌(Serratia sp. G9)的降解效率最高,在24小时内可降解 100% 的羟基酪醇。
图 3. 小线角木蠹蛾肠道细菌参与羟基酪醇降解的体内实验结果。(A) 暴露于抗生素组与对照组(无抗生素)在 LB 培养基中的肠道微生物菌落形成单位(CFU)。(B) 抗生素处理组(左)与对照组(中)肠道微生物多样性的鉴定 。最右侧为 1.5 kb DNA 分子量标准品组。(C) 分别测定暴露与未暴露于抗生素的小线角木蠹蛾幼虫粪便中的羟基酪醇浓度。不同字母表示基于 t 检验分析的统计学显著差异(P < 0.05)。
图 4. Cao等(2023a)从小线角木蠹蛾中分离并于本实验幼虫体内再次发现的肠道细菌分离株及其对 6000 ng/µL 浓度羟基酪醇的降解能力 。不同字母表示具有统计学显著差异(P ≤ 0.05,Duncan 氏检验,F = 3930.599,df = 5,P < 0.01)。
(三)代谢途径解析
共鉴定出 386 个差异代谢物。
核心途径:研究提出了两条降解路径。其中红色路径展示了羟基酪醇转化为 4-羟基苯甲酸、苯酚、儿茶酚等中间产物,最终进入 三羧酸循环(TCA) 产生 ATP 的过程 。这一发现暗示了肠道微生物不仅能解除毒素,还能变废为宝,将防御物质转化为能量 。
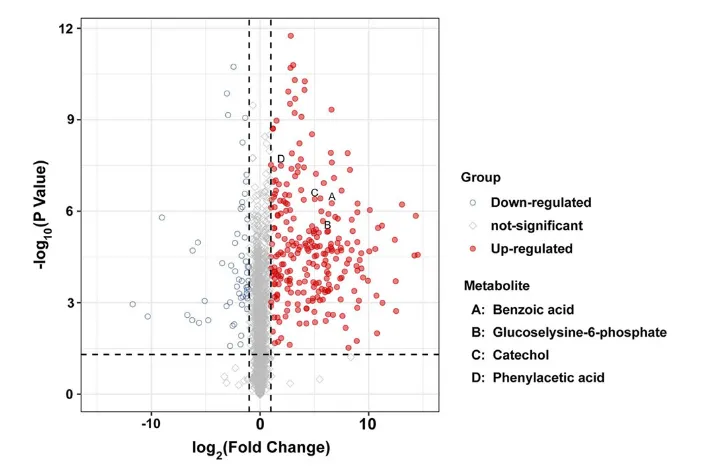
图 5. 对照组(不含羟基酪醇的细菌)与处理组(含羟基酪醇的沙雷氏菌 Serratia sp. G9 菌株)之间差异表达代谢物的火山图。上调代谢物以红色实心圆点表示,下调代谢物以蓝色空心圆点表示;非显著差异代谢物以灰色菱形表示(P < 0.05,fold-change > 1 或 < -1)。
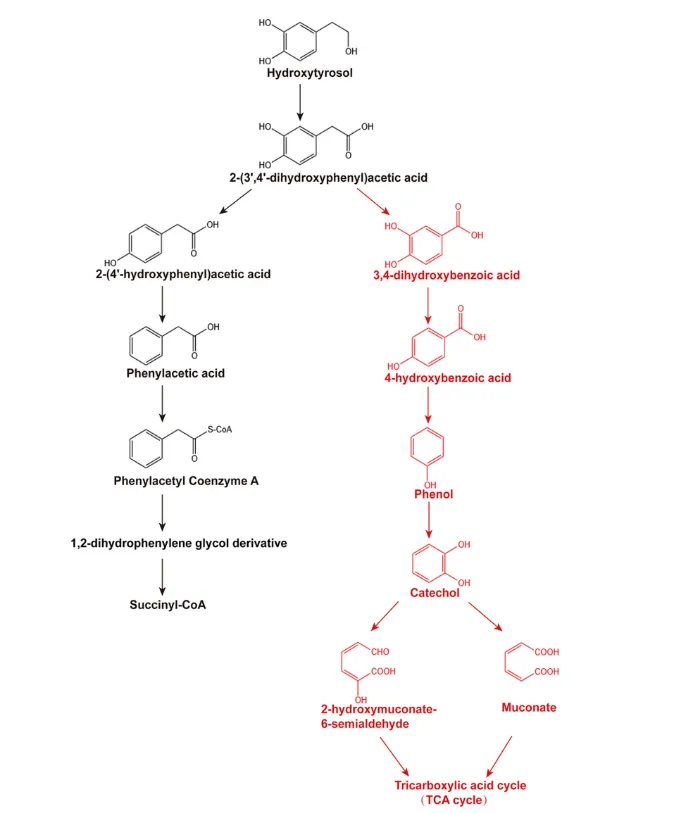
图 6. 肠道沙雷氏菌(G9)降解羟基酪醇的产物及途径。红色表示可能对小线角木蠹蛾及其肠道微生物群最有利并导致 ATP 产生的代谢途径;黑色表示羟基酪醇的一般降解途径。