东北农业大学「国家杰青」隋晓楠教授团队最新发文!
- 2026-05-26 21:30:36


ScienceShare | 科学私享
食品来源淀粉样纤维:面向来源多样性与功能复杂性的精准表征策略
导 读
2026年2月17日,东北农业大学食品学院隋晓楠教授团队在国际食品权威期刊《Trends in Food Science & Technology》(Q1,中科院1区Top,IF=15.4)发表题为“Food-Derived Amyloid Fibrils: Precision Characterization Strategies for Source Diversity and Functional Complexity”的综述性论文。
蛋白质淀粉样纤维最初因其在阿尔茨海默病和帕金森病等神经退行性疾病中的作用而受到关注,其典型特征为富含交叉β折叠结构的纤维状聚集体。该结构由β链通过分子间氢键垂直于纤维轴堆叠形成,被认为是与蛋白质序列无关的普适结构单元。近年来研究发现,在酸性加热等特定体外条件下,许多天然蛋白亦可自发形成具有相同核心结构的淀粉样聚集体;同时,通过短肽从头设计或提取高淀粉样倾向序列片段,也可构建可控的功能性淀粉样体系。食品来源淀粉样纤维(FAFs)是在加热、酸性等条件下,由乳清蛋白、卵清蛋白、大豆蛋白等经部分展开和自组装形成的纳微米级有序结构。其高长径比赋予优异的界面活性、凝胶性能和纳米支架潜力。多层级体内外安全性评价表明,FAFs具有良好生物相容性与一定营养价值;人体研究进一步证实燕麦蛋白淀粉样纤维可提升铁等营养素生物利用度。此外,纤维形成过程中暴露的肽段与疏水基团赋予其抗氧化、抗炎与抑菌活性,使其在食品保鲜、活性物稳定与功能强化中展现前景。然而,其功能高度依赖多尺度结构,而成纤维过程涉及复杂成核-生长动力学与多种中间态,导致结构调控与预测困难。为突破单一表征手段的局限,亟需整合光谱、显微、微流控与计算模拟等跨尺度技术,构建“结构—功能”关联图谱。本文系统梳理相关先进表征策略及应用进展,为FAFs的精准设计与跨学科应用奠定方法学基础。
注:最近有小伙伴反映收不到推送,因为公众号改了推送算法,现在需要加星标,多点赞/点在看,才能准时收到推送。

研究展望
(1)新型表征工具的开发
淀粉样纤维作为具有交叉β折叠结构的蛋白质聚集体,近年来因其独特的力学性能和自组装能力在食品科学领域展现出广阔潜力。然而,传统表征方法受限于分辨率不足以及对复杂环境适应性较差,从而限制了对其结构—功能关系的全面理解。
因此,开发能够在多尺度范围内实现纤维结构精准识别、定量分析与动态监测的先进表征技术,已成为推动该领域发展的关键需求。目前,TEM、AFM、CD、FTIR 和 WAXS 等成熟技术被广泛用于淀粉样纤维表征。尽管这些方法具有重要价值,但其主要局限于静态样品分析,且通常仅提供单维度结构信息。因此,这些方法难以全面捕捉复杂环境中淀粉样纤维的真实构象状态与动态行为。这一局限在食品体系中尤为明显,因为淀粉样纤维常与多糖、脂质及其他蛋白质共存。组分之间的相互作用会影响纤维的组装路径、形貌特征及功能属性。然而,现有表征方法通常缺乏足够的灵敏度和选择性,难以有效解析多组分体系中的复杂行为。
(2)多尺度与多技术协同策略
当前,关于淀粉样纤维的研究不仅关注其形成机制,也日益重视其功能角色。尤其在食品科学领域,淀粉样纤维被广泛探索作为天然、可食用功能材料的潜力。由于其结构具有多尺度复杂性,单一表征技术在结构解析方面存在固有局限。因此,有必要整合多种互补技术手段,以实现对其结构特征与功能属性的全面理解。多技术协同策略的核心在于克服单一方法的局限,实现跨尺度信息的关联与验证。
如图7a所示,受高分辨拉曼光谱与多变量曲线分辨技术启发,研究提出了一种用于识别油包水乳液体系尺度界面的新方法。该技术最初用于研究小分子水合壳层,现已成功扩展至复杂液-液界面分析,并实现了溶液中稳定的界面选择性检测,为淀粉样纤维在乳液体系中的应用奠定基础。
此外,如图7b所示,研究开发了一种基于超拉曼散射的三阶非线性光谱技术——相关振动光谱(CVS)。该技术可同时探测红外与拉曼跃迁,重点解析氢键网络中水分子的分子间或个体贡献,实现选择性检测。
同时,二维红外光谱(2D IR)可用于解析蛋白质结构动力学与聚集行为。当蛋白质引入2H、15N、13C 或 18O 同位素标记时,其红外振动特性会发生显著改变。如图7c所示,13C 和 18O 标记可使酰胺I带产生约65 cm⁻¹ 的蓝移,从而区分标记与未标记残基。氢/氘交换则使酰胺II振动频率产生60–90 cm⁻¹ 的红移,可作为监测蛋白质结构演化的探针。同位素标记技术可实现淀粉样纤维残基水平的二级结构分析。将2D IR与同位素标记结合,现已能够在残基分辨率水平解析蛋白质淀粉样形成路径。
因此,淀粉样纤维在食品领域的应用潜力日益依赖于突破多尺度结构复杂性带来的表征挑战。这不仅有助于深入理解其形成机制,也可提供前所未有的分子层面洞见。未来应重点整合并创新多种先进、互补的光谱技术,以弥补传统方法的不足,为淀粉样纤维在食品领域的精准设计与性能优化提供坚实的分析基础。
(3)人工智能的融合
近年来,在深度学习与计算能力提升的推动下,人工智能(AI)取得了显著进展。通过深度学习算法,可预测蛋白质的聚集倾向,分析其二级结构特征并识别易聚集区域,从而在实验验证前进行计算预测。然而,淀粉样纤维结构预测仍面临重大技术挑战。首先,由于纤维结构的复杂性,纯数据驱动的机器学习方法在建模精度方面存在局限。其次,尽管核心β折叠结构高度有序,但整体构象的动态变化超出了传统预测算法的解析能力。
大型语言模型(如 GPT-4)及 AlphaFold(AF)等突破性创新在蛋白质结构预测方面取得重大进展(图7d)。AlphaFold 通过深度学习技术彻底革新了蛋白质结构预测。该系统由 DeepMind 开发,是目前最先进的神经网络之一,能够基于氨基酸序列高精度预测蛋白质结构,且部分预测超出其训练数据范围。最新开发的 AlphaFold3 进一步实现了复杂生物分子体系(包括蛋白质、核酸和小分子)的联合结构预测,其优势源于先进的扩散模型架构,在结构及相互作用预测方面表现出行业领先水平。
此外,将AI与深度学习方法引入光谱数据分析,可显著提升蛋白质定量与结构解析精度。当前正在开发的基于AI的光谱检测系统,专用于高效筛选新型植物蛋白来源(图7e),有望加速可持续食品研发。通过AI驱动的算法模型优化光谱解卷积过程,可有效减少其他食品组分的信号干扰,实现不同配方体系中蛋白质动力学的预测分析。结合深度学习框架与数据融合方法,振动光谱分析性能显著提升,能够有效解决光谱重叠与水干扰等关键问题。卷积神经网络与循环神经网络在识别传统化学计量学方法难以解析的细微光谱特征方面表现出优越性能。
总之,人工智能与淀粉样纤维表征的融合有望建立蛋白质结构研究的新范式。深度学习通过自动化数据融合与预测模拟,有潜力突破传统分析方法的固有限制。随着多模态数据规模与复杂性的不断增长,AI驱动框架将显著提升纤维表征的分辨率与准确性。除增强分析性能外,该融合还为基于淀粉样纤维的功能材料理性设计提供新的可能。AI的预测能力不仅可用于表征既有纤维结构,还可高精度预测结构转变与界面相互作用,有助于阐明淀粉样纤维组装机制及决定其形貌与稳定性的关键因素。随着AI技术不断进步,其与淀粉样纤维研究的深度融合将实现更精准的表征、更丰富的数据解析以及更清晰的机制认知。
图文赏析
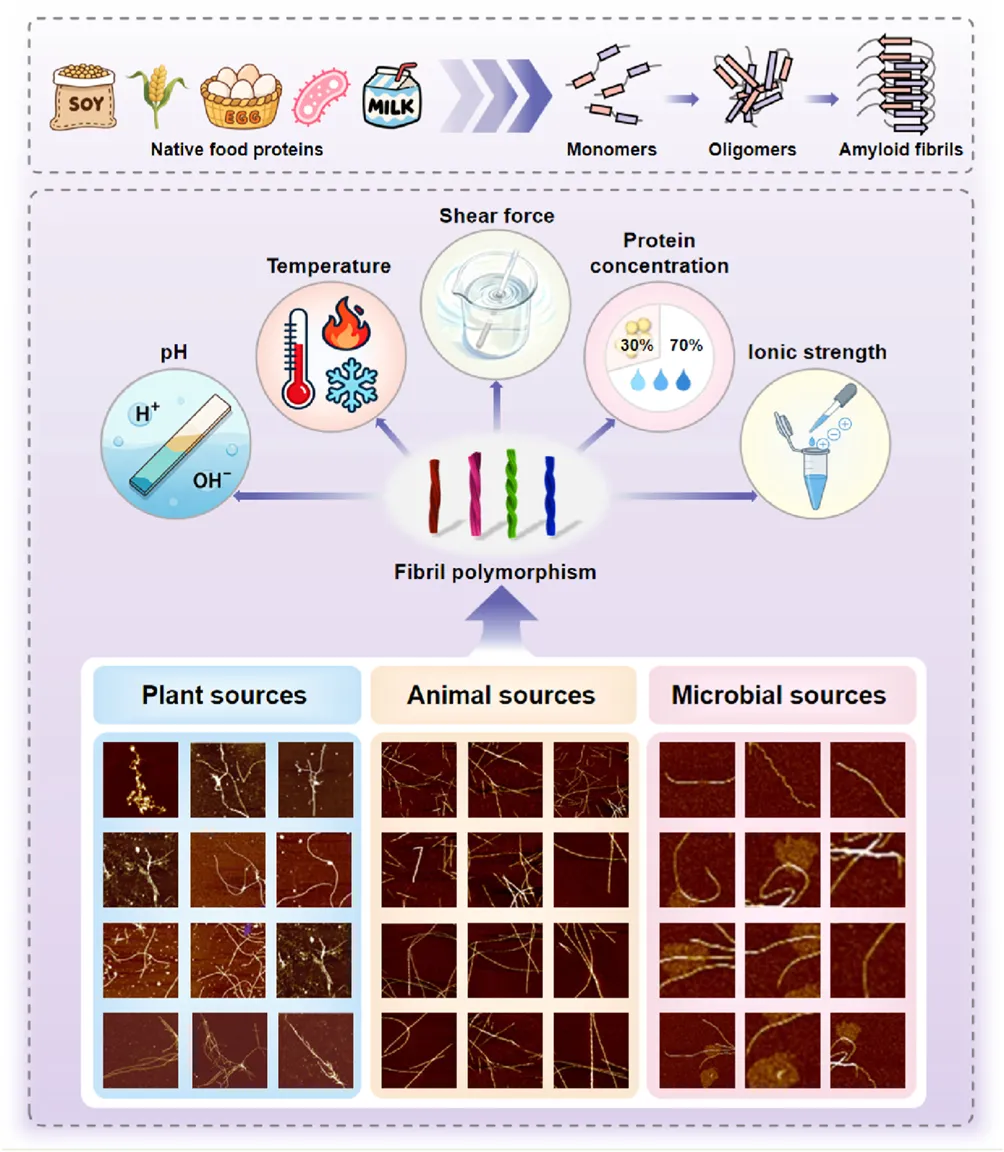
食品来源淀粉样纤维(FAFs)的形成路径、影响因素及多态性。
原文链接
https://doi.org/10.1016/j.tifs.2026.105628

① 长按二维码 或 ② 点击左下角“阅读原文”
免责声明:「原创」仅代表原创编译,水平有限,仅供学术交流,本平台不主张原文的版权,如有侵权,请联系删除。文献解读或作者简历如有疏漏之处,我们深表歉意,请作者团队及时联系《科学私享》主编(微信号:scienceshare-001),我们会在第一时间进行修改或撤稿重发,感谢您的谅解!


































































▼ 点击专家 查阅进展 ▼
▼ 点击标题 查阅专栏 ▼


