本研究成功鉴定到杀鱼爱德华氏菌higBA操纵子下游一个功能完全未知的XRE家族转录调控因子XreR。该蛋白拥有保守的DUF2442与HTH-XRE结构域,在多种致病菌中广泛存在,但其生物学功能一直未曾被揭示。通过基因敲除、过表达、启动子活性分析和EMSA实验,首次证实XreR能直接结合higA启动子并特异性激活其转录,从而确立了XreR作为higA直接上游激活因子的身份,填补了HigBA系统上游调控元件的空白(图1)。
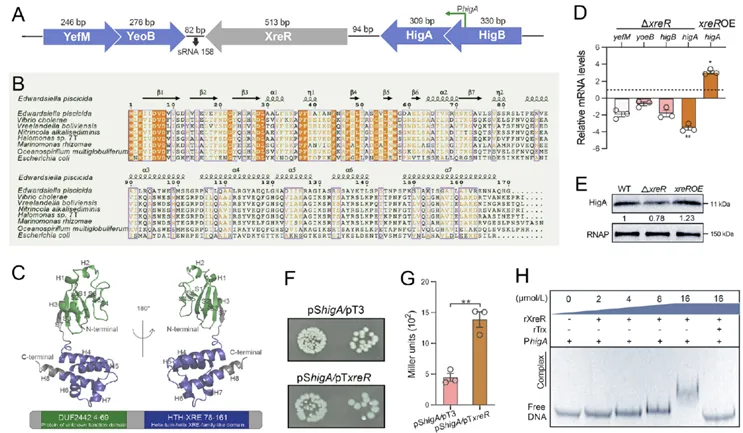
图1. XreR序列特征及对higA的表达调控
表型研究发现,XreR虽不干扰细菌生长,却显著重塑了毒力相关特征:降低运动性与生物膜形成能力,增强氧化应激敏感性,并削弱菌株在巨噬细胞内的存活;更为重要的是,xreR缺失竟显著增强菌株毒力,直接证实XreR是毒力的负调控因子。结合之前higA的致病性结果,可以得出结论:XreR通过正向调控higA来实现对细菌毒力的抑制(图2)。
图2. XreR通过调控HigA调节杀鱼爱德华氏菌的毒力
令人振奋的是,本研究发现抗毒素HigA拥有一个意料之外的新功能——直接充当转录因子调控溶血素基因。在ΔhigB菌株中,游离HigA积累可显著上调ethB表达;启动子活性分析和EMSA证明,HigA直接结合并激活ethB启动子,而XreR并不直接作用于ethB,而是借由HigA间接发挥效应。由此,一条全新的溶血调控通路:XreR-HigA-EthB被成功确立。
图3. HigA激活ethB表达并增强杀鱼爱德华氏菌的溶血作用
对EthB的功能解析表明,该蛋白对细菌氧化应激耐受、血清抗性、巨噬细胞定植乃至整体毒力均不可或缺。但ethB过量表达会诱发宿主细胞焦亡,反而不利于胞内生存,暗示EthB必须维持在适宜的表达窗口。这一发现揭示了病原菌在毒力输出与免疫逃逸之间的精妙平衡,也凸显了HigA精准控制EthB表达以维持感染稳态的独特策略(图4)。
图4. EthB在杀鱼爱德华氏菌中的功能分析
此外,本研究还解析出一条由HigA主导的氧化应激新通路。HigA可直接结合应激全局调控因子rpoS的启动子并抑制其转录,进而下调关键抗氧化酶基因katG,使细菌氧化应激耐受能力降低(图5)。而更为精妙的是,在氧化应激条件下,Lon蛋白酶可特异性识别并降解HigA,解除其对RpoS-KatG通路的抑制,从而迅速恢复细菌抗氧化能力(图6)。这揭示了一个Lon-HigA-RpoS信号轴作为细菌感知和应对氧化胁迫的分子开关。
图5. HigA通过抑制RpoS-KatG调控氧化应激耐受
图6. Lon降解抗毒素HigA
综上所述,本研究系统性揭示了以抗毒素HigA为中枢的多层级调控网络:一方面,上游XreR激活higA,再由HigA直接上调ethB驱动溶血(XreR-HigA-EthB轴);另一方面,在氧化应激下,Lon蛋白酶动态降解HigA,解除对RpoS的抑制,精准开启抗氧化防御。这些发现展现了抗毒素HigA协调溶血与氧化应激适应的双重关键作用,颠覆了抗毒素仅作为毒素抑制剂的传统认知,为深入理解TA系统在致病菌中的多功能调控提供了新思路(图7)。
图7. 抗毒素HigA协调杀鱼爱德华氏菌溶血和氧化应激适应的机制