1、Slc4a11MCD/ + 报告系统在体内标记高可塑性细胞状态
建立了研究的核心工具。通过单细胞测序确定Slc4a11为 HPCS 的最特异性标记基因,并据此构建了Slc4a11转基因报告小鼠。流式与免疫荧光证实,该模型能特异性标记约占肿瘤细胞总数 17%的 HPCS,细胞呈散在或小簇状分布,且丰度随肿瘤病理分级升高而显著增加(图1)。
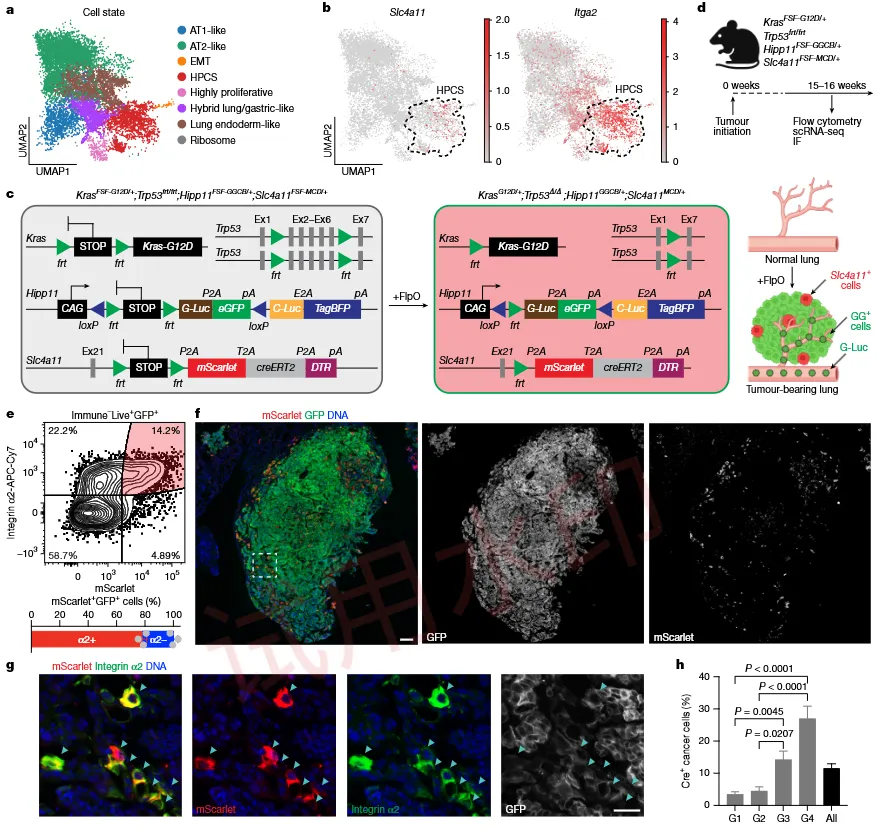
图1:Slc4a11MCD/+报告基因系统标记体内 HPCS
2、高可塑性细胞状态HPCS是体内细胞状态转换的核心枢纽
阐明了HPCS 的核心功能定位。谱系示踪证实 HPCS 可双向转化为肺癌所有已知细胞状态,是肿瘤表型多样性的核心来源。对比 AT1 样细胞,HPCS 具备高可塑性与克隆扩增能力,且非HPCS肿瘤细胞可重新获得HPCS表型(图2)。
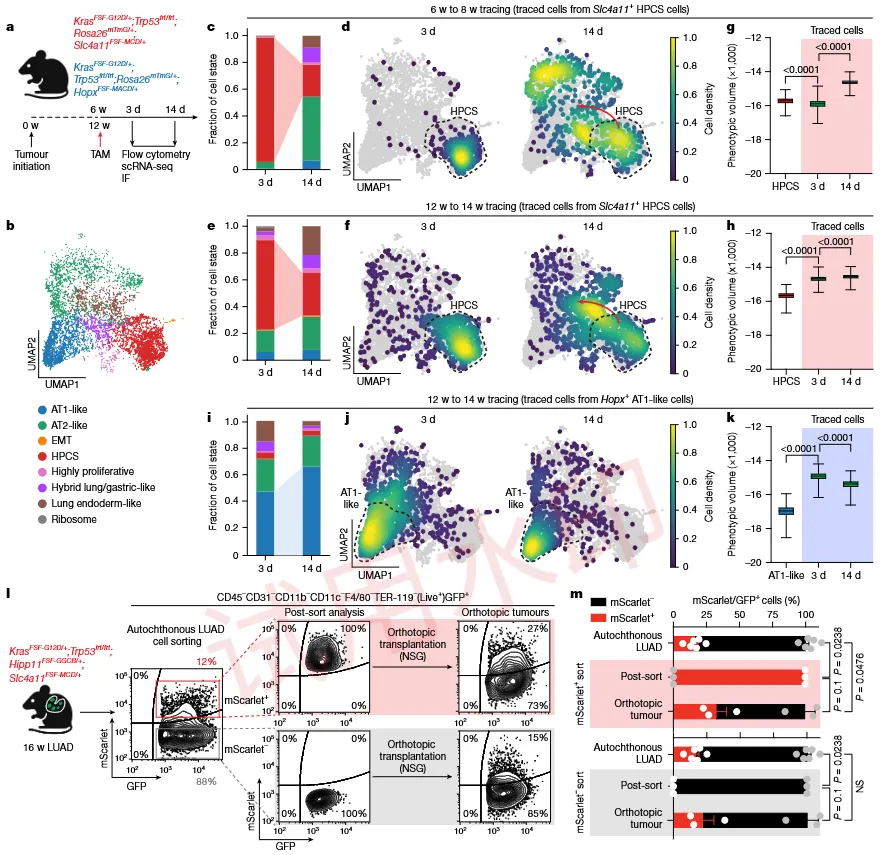
图2:HPCS 是体内细胞状态转换的枢纽
3、高可塑性细胞状态HPCS是肺癌肿瘤生长的核心驱动因素
证实 HPCS 是肿瘤生长与恶性进展的关键驱动者。HPCS 自身处于静息状态,但其分化子代快速增殖并主导肿瘤扩张。早期清除 HPCS 可阻断良性向恶性转化,晚期清除 HPCS 可显著降低肿瘤负荷,而清除AT1样细胞无治疗效果(图3)。
图3:HPCS 驱动肿瘤生长
4、高可塑性细胞状态介导肺腺癌治疗耐药的细胞起源
揭示HPCS是肺癌治疗耐药的根源。化疗与 KRAS 靶向药主要杀伤非 HPCS 细胞,HPCS 来源细胞存活并构成微小残留病灶。联合清除 HPCS 可与化疗 / 靶向药协同,近乎完全根除肿瘤;uPARCAR‑T 可特异性清除 HPCS 并发挥强效强效抑瘤作用(图4)。
图4:耐药细胞状态源自 HPCS
5、Slc4a11/Plaur 标记的类HPCS 广泛存在于多癌种及再生上皮组织
证明 HPCS 是跨癌种保守的核心细胞状态。HPCS 特征在肺、结直肠、胰腺、前列腺等多种上皮癌中普遍存在,并与耐药、复发程序高度重合。HPCS 本质是上皮损伤再生程序在肿瘤中的异常劫持,为动态可逆的过渡态而非传统癌症干细胞(图5)。
图5:由Slc4a11和Plaur标记的 HPCS 样状态广泛存在于多种癌组织及再生上皮组织中