《食品科学》:华南农业大学肖治理副教授等:重金属残留免疫分析法中抗体与抗原特异性识别及相互作用机制研究进展
- 2026-04-04 00:24:32

重金属是指密度大于4.5 g/cm3的金属,在环境中主要以游离离子、化合物等形式存在。其中,有毒重金属如汞(Hg)、镉(Cd)、铅(Pb)、铬(Cr)、砷(As)等毒性大、污染范围广,易通过土壤、水源富集到小麦、水稻、肉制品、水产品等食品中,进而在人体多种器官内蓄积,导致骨痛病、肾衰竭、高血压等疾病,甚至致癌、致畸、致突变。
重金属的检测方法可分为两类:一类是仪器分析法;另外一类是快速检测法,其中免疫分析法是基于抗体能特异性结合抗原的原理而建立的,具有特异、灵敏、高效、成本低、操作简便等优点,能够弥补上述缺陷,满足现场快速检测的需求。
抗体的特异性、稳定性直接决定了方法的检测特性。重金属的分子质量小于1 000 Da、结构单一,空间结构与其他小分子不同,单独存在时只具有半抗原的电势,不能作为一个完整的抗原决定簇引起免疫反应。因此,在重金属抗体的制备中,需要借助双功能螯合剂螯合重金属离子并偶联载体蛋白(如钥孔血蓝蛋白、牛血清白蛋白、乳铁蛋白等)以形成完全抗原,再通过动物免疫、杂交瘤技术制备特异性抗体。
目前,大部分研究中制备的重金属抗体都与其他重金属螯合物存在一定程度的交叉反应,对实际的食品检测带来不同程度的干扰。因此,研究重金属抗体对抗原的特异性识别及相互作用机制对于分析阐释抗体特异性差异的根本原因并推进食品中重金属残留免疫分析法的开发具有重要意义。
华南农业大学食品学院的黄俊钧、周孟新、肖治理*等人综述重金属抗体对抗原识别机制的3 种研究手段及其进展,包括抗原抗体结合参数的测定、抗原抗体结构的分子模拟、抗体晶体结构的解析,并分析重金属抗体与抗原特异性识别及相互作用的机制,以期为重金属抗体性能的定向调控和改造、食品中重金属免疫分析方法的开发及其他食品小分子污染物识别机制研究提供思路及参考。

01
重金属抗原抗体识别机制的研究手段及进展

关于免疫分析法用于食品污染物的检测已有许多研究,但常常面临着抗体灵敏度低、特异性差、无法达到检测要求的难题,因此不少研究者开始探究抗原抗体的相互作用方式和识别机制,希望通过设计抗原或者直接改造抗体结构等手段获得高质量的抗体,进而提升方法的检测特性。针对重金属抗原抗体识别机制的研究手段主要有3 种,如表1所示,大多数研究将几种手段相结合,以探究重金属抗体对抗原的特异性识别及相互作用机制。

1.1 抗原抗体结合参数的测定
针对重金属抗原抗体的识别机制研究,最初是通过测量抗原抗体的结合参数从而对比和评价重金属抗体对抗原的亲和特性。如通过酶联免疫吸附测试(ELISA)法测定抗体的亲和力常数(Kaff);采用固定化金属离子亲和层析法(IMAC)判断抗体与金属离子的亲和力,预测抗体的结合位点;利用KinExA免疫传感器等仪器和设备测定抗体与抗原之间的平衡解离常数(KD)、结合速率常数(Ka)、解离速率常数(Kd)等结合参数,分析抗体与抗原之间的结合程度,进而判断抗体与抗原相互作用的亲和力、时间和效果。
1.1.1 ELISA
ELISA是一种根据抗原抗体特异性结合和酶-底物相互作用的原理检测抗体特异性的方法,可以分为直接法、间接法、夹心法。ELISA所测得的数据能结合质量作用定律转化为总抗体浓度的形式,推导出式(1),进而计算抗体亲和力常数Kaff。一般认为,抗体的Kaff值在107~1012L/mol之间为高亲和力抗体。
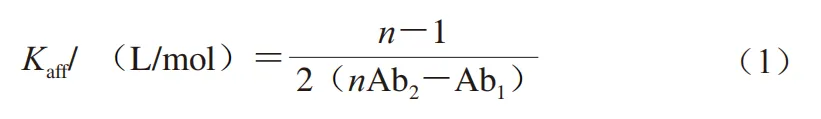
式中:n=Ag1/Ag2(Ag1、Ag2为包被浓度);Ab1、Ab2为包被浓度分别为Ag1、Ag2时50%最大吸光度(Amax)所对应的抗体浓度。
ELISA法简单快捷,多应用于高亲和力抗体的筛选以及抗体亲和力的直接评估。Zhu Xiaoxia等制备了针对Pb-DTPA的单克隆抗体,通过建立间接竞争酶联免疫吸附法(ic-ELISA)测定了抗体的Kaff值为2.19×1010 L/mol,证明抗体具有高度亲和力并用于检测饮用水的Pb残留。Xu Naifeng等制备了4 株针对Cd-EDTA的单克隆抗体,采用ic-ELISA方法测定了4 株抗体的Kaff值,结果显示4 株抗体的Kaff值均大于109 L/mol且高于文献报道的Cd抗体的Kaff值,均为高亲和力抗体,并采用其中灵敏度最好的抗体建立乳胶微球层析法以检测芦笋及蔬菜样品中的Cd残留。
利用ELISA测定抗体的Kaff值方法简单、快速、可靠,能初步判断重金属抗体对抗原的结合力强弱,筛选出具有高度亲和力的抗体用于后续免疫分析方法的建立等。但该方法只有抗体与抗原相互作用的数值信息,无法阐明抗体与抗原的相互作用方式。
1.1.2 IMAC
IMAC是利用蛋白质表面的某些氨基酸残基(如组氨酸(His)的咪唑基、半胱氨酸的巯基、色氨酸的吲哚基等)与金属离子通过配位键特异性结合以纯化目标蛋白的一种方法。
将IMAC与其他方法结合能判断抗体与重金属半抗原的亲和力,预测抗体的结合位点或者结构互补信息。Boden等在1995年首次将IMAC与平衡结合免疫分析法结合,分析了针对铟(In)-DTPA的单克隆抗体(mAb 734)对7 种金属离子的结合能力。结果发现,抗体对In-DTPA的亲和力比其他金属离子高100 倍。通过IMAC发现抗体与金属离子的结合位点中包含至少2 个His残基,同时还可能存在天冬氨酸、谷氨酸以及半胱氨酸残基。Sarada等将IMAC与ELISA结合,探究了锌-亚氨基二乙酸盐特异性免疫球蛋白(Ig)M单克隆抗体在4 种金属离子中与Zn(II)的结合效率。结果发现,Cr(III)存在时抗体与Zn(II)具有协同效应,但结合位点不同;Cd(II)存在时则表现出拮抗作用,表明抗体中的Zn(II)结合位点被阻断;而在Cu(II)存在的情况下,观察到竞争性结合;Cr(VI)存在则不影响抗体与抗原的结合。
通过这些研究能够初步推测:重金属抗体与抗原的结合通过接触部分氨基酸残基位点进行。这些结合位点直接影响抗体与抗原的结合效率,但只能推测IMAC中已知的氨基酸是否参与反应,不能完全确定参与反应的氨基酸数量、种类及反应的相互作用力类型。
1.1.3 KinExA免疫传感器
KinExA免疫传感器是一种计算机控制的荧光光谱仪,能进行抗原、抗体以及抗原-抗体复合物的分离和定量检测。测定时,抗体结合的固定化抗原数量与溶液中游离抗体的数量呈正比,并通过荧光标记的二抗检测这种相互作用,最后将荧光数据拟合到平衡结合模型中,就可以通过测定结合参数确定抗体-抗原相互作用的亲和力及稳定性。
利用KinExA仪器能直接测定抗体与不同螯合剂、金属-螯合剂配合物的结合参数。通过改变螯合剂的结构,可以探究抗原中的螯合剂部分是否影响抗体的特异性识别。Khosraviani等制备了识别Pb-环己基二乙基三胺五乙酸(CHXDTPA)复合物的单克隆抗体,通过KinExA免疫传感器测定了抗体的KD和Ka,评估了抗体对多种无金属螯合剂和金属-螯合剂配合物的相互作用能力。抗体与螯合剂CHXDTPA的亲和力为2.3×10-7 mol/L,而增加Pb(II)之后,抗体的亲和力增加了25 倍。该抗体同时具有与螯合剂EDTA、DTPA及其衍生物相互作用的能力,但其亲和力比CHXDTPA低95.49%~99.99%。由此判定,该抗体对Pb-CHXDTPA表现出高度的选择性和特异性。Jones等利用KinExA3000免疫分析仪研究了2 株镉单克隆抗体(A4和E5)与12 种不同金属螯合物的相互作用能力。结果显示,2 株可变区序列不同的抗体对金属螯合物的亲和力相似,以Cd(II)、Hg(II)与EDTA形成的复合物亲和力最高。在EDTA主链上增加环己基提高了抗体E5对金属-螯合剂半抗原的亲和力,抗体A4则相反。由此表明,重金属抗体对抗原的识别与螯合剂的种类、结构有着紧密的关系。
为了研究抗原中不同金属离子对重金属抗体与抗原相互作用的影响,Blake等制备了针对Cd-EDTA的单克隆抗体,通过KinExA测定抗体的KD,分析了抗体对16 种不同金属-EDTA复合物的识别能力。结果显示,该抗体对Cd-EDTA及Hg-EDTA具有相近的KD(分别为21 nmol/L及26 nmol/L),但与其他金属离子-EDTA配合物(如Mn(II)、Pb(II)、Cu(II)等)的亲和力比Cd-EDTA的低94.88%~99.99%。除Hg和Mg外,二价金属离子与螯合剂的结合与金属离子的大小密切相关。上述抗体对重金属半抗原存在交叉反应的原因可能是Hg(II)与Cd(II)的共价半径只相差0.1 Å,离子半径仅差0.05 Å,其分别与EDTA形成的半抗原空间构型相似所导致。
这些研究表明,螯合剂的种类、结构以及重金属离子的大小都是影响抗体识别金属螯合物半抗原的重要因素。利用某种特定螯合剂制备的完全抗原免疫动物所获得的抗体对该螯合剂具有一定的选择性,而对该螯合剂与重金属离子形成的半抗原具有高度特异性,由此推断抗体识别的不是单独的螯合剂结构或者重金属离子,而是重金属-螯合剂复合物的整体结构。此外,通过改造前处理所用螯合剂的化学结构能够提高或者降低抗体的特异性。重金属离子的大小则决定了其与螯合剂的结合程度,进而影响抗体对重金属-螯合剂复合物的识别能力。
1.2 抗原抗体结构的分子模拟
分子模拟是一种将理论和计算机软件技术结合,模拟分子的三维结构或行为的技术,主要包括同源建模、分子对接技术、量子力学、分子动力学技术等。分子模拟能通过模拟分子的空间构效,将分子间的相互关系可视化,有助于分析分子间的相互作用机理,目前已广泛运用于食品安全、食品加工与贮藏以及食品功能因子筛选等领域。近年来,分子模拟技术在食品安全免疫分析检测领域主要应用于半抗原的设计、抗原抗体识别机制研究、抗体制备等方面。在抗原抗体识别机制研究中运用的主要是同源建模及分子对接技术。利用分子模拟技术,能构建抗原、抗体的三维模型,模拟抗体与抗原相互作用的情况,预测抗体与抗原的结合位点,从三维结构角度分析抗体对抗原的识别机制和作用机理。
抗体模型的构建需要抗体的氨基酸序列信息。Blake等利用分子生物学技术,通过聚合酶链式反应推导出针对Cd-EDTA单克隆抗体(2A81G5)的重链可变区和轻链可变区氨基酸序列,利用Swiss-Model服务器同源建模构建了抗体的三维模型,最后通过分子模拟技术分析该抗体与抗原可能的结合位点。分子模拟结果发现,抗体重链96号位置上的His是抗体识别抗原的重要位点。该研究开始利用分子模拟技术初步推测抗体识别抗原的氨基酸位点及类型。
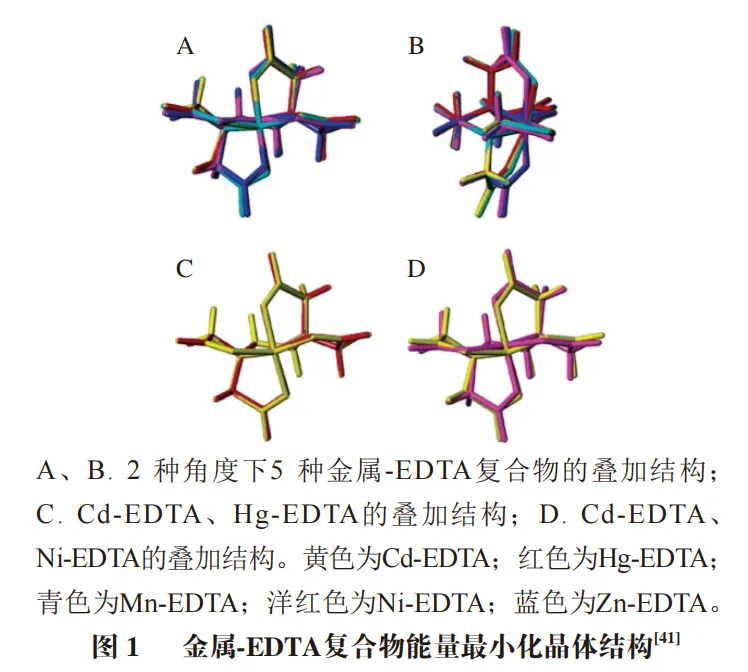
除了构建抗体分子模型外,利用分子模拟构建金属-螯合剂复合物整体的分子模型能从半抗原的空间构型角度分析影响抗体识别的半抗原空间结构特征。Jones等基于现有的晶体结构,建立了5 种不同的二价金属-螯合剂复合物的分子模型(图1A、B)。为了确定可能影响抗体识别的半抗原结构特征,将这些模型进行比较,并结合距离矩阵鉴别出几种半抗原三维结构存在差异的区域。研究发现,Cd-EDTA和Hg-EDTA结构中原子位置的距离差都在0.2 Å以下,这两种配合物的三维结构非常相似(图1C),这可能是导致抗体对两种不同半抗原有相似亲和力的原因。而Cd-EDTA和镍(Ni)-EDTA的结构差距最大(图1D)。由此推断,抗体亲和力与这些金属-EDTA复合物总体结构的差异程度密切相关。
分子模拟最大的缺陷在于其准确性,但结合定点突变、共价修饰等手段能侧面验证分子模拟的结果是否可靠。Delehanty等用两个针对不同金属螯合物(Cd-EDTA及Pb-DTPA)的单克隆抗体(E5及5B2)分别制备了重组的抗原结合片段(Fab)。通过同源模建和诱变鉴定,发现有3 个氨基酸残基影响Cd抗体(E5)对Cd-EDTA的识别,分别为重链52号位置的色氨酸(Trp52)、96号位置的组氨酸(His96)和轻链96号位置的精氨酸(Arg96)。其中His96可能介导了抗体与Cd(II)的直接连接;Trp52似乎参与了螯合剂苯甲基部分的疏水叠合;Arg96似乎与螯合剂部分形成静电相互作用或氢键。采用分子模拟结合共价修饰、定点突变等方法预测出Pb抗体(5B2)重链58号位置的赖氨酸(Lys58)与Pb-EDTA接触,并与螯合物上的羧基形成离子对或氢键。该研究将分子模拟技术与定点突变等技术结合,推断出了影响两株抗体识别抗原的关键氨基酸位点及形成的作用力。
以上研究基于分子模拟技术建立了重金属抗体、金属-螯合剂半抗原的三维结构模型。通过三维结构对比分析半抗原空间结构上的区别,并结合同源建模、分子对接、共价修饰、定点突变等技术初步预测影响抗体识别抗原的关键氨基酸位点和作用力类型。这些研究表明,抗体主要通过互补决定区(CDR)上一定数量、类型的氨基酸与金属螯合物半抗原整体进行接触、识别。
利用分子模拟技术分析重金属抗体与抗原的相互作用与识别机制简单、快捷、方便,但这种技术只停留在预测和推断的阶段,且分子模拟的结果对计算机算法的依赖性过大,后续还需结合定点突变等手段验证关键氨基酸位点,较难真实、准确地反映抗体与抗原的结合情况。
1.3 抗体晶体结构的解析
与分子模拟不同,基于晶体对抗体或抗原抗体复合物进行三维结构解析,能更准确、真实地获得完整且可靠的三维结构,如实呈现抗体与小分子的相互作用界面,更好地分析重金属抗体对抗原的识别机制。近年来,有许多研究制备出抗体晶体,并对晶体结构进行解析,分析抗体与抗原的互作机制。
目前,蛋白质晶体结构解析的手段主要有X射线衍射(XRD)技术、核磁共振(NMR)技术、低温冷冻扫描电镜(Cryo-SEM)技术3 种。表2总结了3 种技术的优缺点。其中,NMR技术及Cryo-SEM技术具有成本过高、制样无法满足分析要求等局限性,在抗体结构解析中应用较少。XRD技术是目前应用最广泛、技术最成熟的方法。截至2024年,蛋白质结构数据库(https://www.rcsb.org/)中有85%以上的蛋白质晶体结构是通过XRD技术获得的。

XRD技术的工作原理为:当X射线照射在晶体上时,晶体中晶胞的原子按规则排列分布,这些原子在空间的排列方式、距离、方位、强度等信息会反映在衍射图上,最后利用计算机软件处理并分析晶体衍射数据,解析出晶体的结构信息。XRD法解析晶体结构信息通常包含以下5 个步骤:蛋白的制备和纯化、晶体的培养、XRD、数据处理、解析相位。其中,由于蛋白质结晶的条件难以摸索,晶体的培养是这个技术中的难点和瓶颈。对于抗体而言,完整抗体结构中CH1和CH2功能区之间有一段由脯氨酸组成的区域称为铰链区,铰链区富有弹性,这种特性导致完整的抗体三维结构信息难以获取。因此,各种研究采用抗体活性片段分析抗体对抗原的相互作用,如Fab、单链抗体(scFv)等。
采用XRD技术解析重金属抗体结构的研究较少,可能是由于抗体活性片段制备困难或晶体培养的难度大,目前仅有一篇文献报道。Love等制备了针对In-硫脲基-L-苯基-EDTA(EOTUBE)的单克隆抗体CHA255,与其他金属离子螯合物的亲和力对比发现,该抗体对In螯合物具有高度特异性。为了探究这种高特异性,该研究制备了抗体CHA255的Fab’,将其分别与In-EOTUBE、铁(Fe)-EOTUBE反应,形成抗原-Fab’的复合物。分别在2.2、2.8 Å的分辨率下通过分子置换确定并细化了两种复合物的晶体结构。通过结构解析发现,In-EOTUBE半抗原的EDTA部分半包埋在抗体CDR区中心附近,且Fab’上6 个CDR区中有5 个通过蛋白质侧链原子而非主链原子与半抗原相互作用。Fab’上共6 个氨基酸残基与半抗原直接接触,形成了5 个氢键与1 个配位键。特别的是,Fab’中重链CDR3区的His与In(III)直接产生了配位作用,距离为2.4 Å,但Fab’与Fe-EOTUBE的结构解析中则没有发现这种配位反应。分析两种半抗原的空间结构发现,两种半抗原在构象上有细微的差别,使得金属离子Fe(III)不易接近His,His不再与Fe(III)配位。这可能是抗体CHA255对铟半抗原比对铁半抗原亲和力要高20 倍的原因。
该研究首次对重金属In特异性单克隆抗体片段与抗原的复合物进行结晶,并发现半抗原空间结构的细微变化对抗体特异性识别半抗原有重要影响,而抗体与半抗原中的重金属离子直接接触能使抗体特异性识别、捕获相应半抗原。关于其他重金属特异性抗体的晶体结构信息尚鲜见报道,重金属抗体与抗原的特异性识别机制尚未完全阐明,有待进一步深入研究。
02
重金属抗体特异性识别及相互作用机制分析及其应用

2.1 重金属抗体特异性识别及相互作用机制分析
上述研究采用结合参数测定、分子模拟、晶体结构解析等手段对重金属抗体特异性识别及相互作用机制进行了初步探讨,结合研究结果,可以分别从抗原和抗体的角度剖析重金属抗体特异性识别及相互作用机制。
与食品中其他小分子污染物不同,重金属半抗原包含螯合剂和重金属两部分结构。因此,从抗原角度分析,影响重金属抗体特异性识别抗原的原因主要有以下3 点:1)螯合剂的化学结构、空间构型,如大部分二价金属离子与EDTA形成六配位结构化合物,与DTPA则形成八配位结构化合物;2)重金属离子的半径、特性,离子半径相似,容易存在交叉反应,产生高特异性抗体难度较大;3)重金属离子与螯合剂形成的复合物整体空间构型、稳定性。Jones等将半抗原中的螯合剂由EDTA替换为1,2-环己二胺四乙酸(CDTA)后,抗体的亲和力明显上升。这是由于CDTA-金属配合物引入了环己基环,碱性增强,增加了氮与金属离子的配位键强度,提高了金属-螯合物的稳定性;Blake等利用1,10-菲罗啉-2,9-二羧酸(DCP)作为螯合剂制备免疫原,获得了对六价铀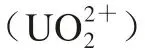 具有高度特异性的抗体。通过分析
具有高度特异性的抗体。通过分析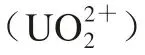 -DCP复合物的分子模型并与EDTA、DTPA形成的螯合物对比发现
-DCP复合物的分子模型并与EDTA、DTPA形成的螯合物对比发现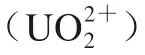 能更大程度地暴露在螯合剂DCP表面,引起更强大的免疫反应,产生的抗体特异性更高。
能更大程度地暴露在螯合剂DCP表面,引起更强大的免疫反应,产生的抗体特异性更高。
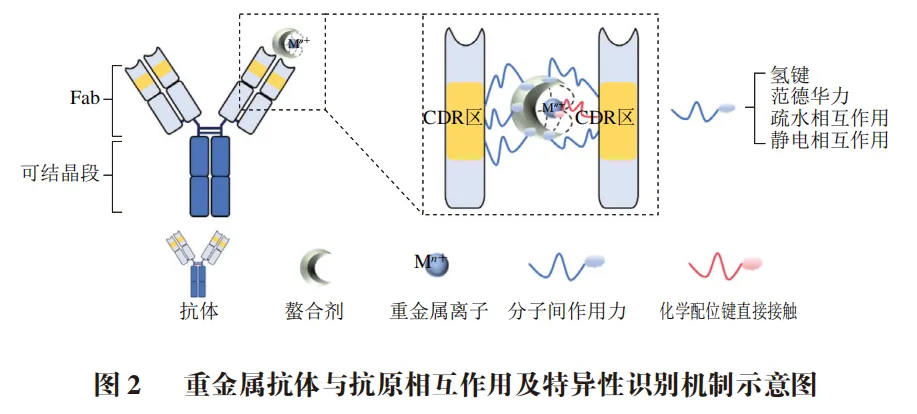
抗体的本质是由氨基酸组成的蛋白质,重金属抗体能和抗原相互作用,主要依赖抗体CDR区上一定数量的氨基酸残基与重金属半抗原形成的两类接触(图2):一类是与螯合剂部分形成的分子间作用力,主要包括氢键、范德华力、疏水相互作用、静电相互作用;另一类是与重金属离子通过化学配位键的直接接触。其中,氨基酸与金属离子形成的配位直接接触或许更有利于抗体特异性捕获、识别重金属半抗原,此类抗体的特异性更强,但只有部分种类的氨基酸(如His、天冬氨酸、谷氨酸、半胱氨酸等)能与金属离子发生配位反应。Delehanty及Love等的研究结果中,除了抗体与螯合剂的分子间作用力外,抗体与对应重金属离子的直接接触均为His残基介导。Delehanty等利用亮氨酸残基取代His后发现抗体的结合性能有所降低,Love等则是通过晶体学的手段发现抗体的高特异性正是His与In(III)的直接配位反应导致。
2.2 重金属抗体特异性识别及相互作用机制的应用
目前,已有较多针对不同重金属的抗体被研制出来应用于食品中重金属残留的免疫分析,但仍缺少重金属抗体与抗原特异性识别及相互作用的机制信息。因此,选择高特异性重金属抗体,利用测定亲和力、分子模拟、晶体结构解析等手段揭示抗体对重金属-螯合剂半抗原的特异性识别及相互作用机制,有助于重金属半抗原的设计、抗体的开发以及免疫分析方法的建立。
1)半抗原设计:根据抗原抗体的结构互补信息,可以对半抗原结构进行设计、修饰、改造,采用不同种类或不同功能的螯合剂,增加重金属离子的暴露或创造重金属的配位点,以产生特异性更强的重金属抗体。比如对于Hg(II),可以采用含有巯基的螯合剂,如谷胱甘肽或6-巯基烟酸(MNA)。这类螯合剂能与Hg(II)直接偶联,增加Hg(II)的暴露,从而产生特异性更高的抗体。靳雪雪用MNA作为双功能螯合剂制备了针对Hg-MNA的抗体并建立ic-ELISA检测法,方法的检出限低至0.079 ng/mL。但目前这种现象未在其他重金属离子的检测中发现。
2)抗体开发:根据识别机制中关键的氨基酸及相互作用方式,可以对重金属抗体进行定点突变、修饰或通过基因工程手段直接设计、制备重金属特异性的重组抗体,人工调控重金属抗体的特异性和灵敏度,以提高抗体的性能,并为相似重金属抗体的制备提供参考。如Wang Fangyu等通过分子对接预测有16 个氨基酸影响环丙沙星抗体对环丙沙星的识别,并将160号位置的缬氨酸定点突变为丝氨酸后,抗体的灵敏度增加了16.6 倍,突变后的抗体可应用于食品中环丙沙星的高灵敏检测。
3)免疫分析方法:通过识别机制的研究,基于半抗原设计、高特异性抗体的开发,能够建立特异性更强、更灵敏、更高效的免疫分析方法,用于食品中重金属残留的特异性快速检测。
03
重金属免疫分析法在食品检测中的应用

重金属由于其毒性大、容易在食品中残留蓄积的特点已经引起人们的广泛关注。我国于2023年实施的GB 2762—2022《食品中污染物限量》规定了各种重金属在食品中的残留限量标准,其中以Cd在饮用天然矿泉水中的限量指标最低(0.003 mg/L)。因此,开发高灵敏度、高特异性的重金属免疫分析法用于食品中重金属残留的快速检测具有良好的前景和应用价值。表3总结了近5 年来部分文献报道的重金属免疫分析法及其效果。其中,Ling Sumei等制备了Hg单克隆抗体,采用ic-ELISA法测定其性能,发现该抗体的灵敏度高,检测限远低于先前报道的Hg抗体。基于该抗体,Ling Sumei等开发了两种免疫层析试纸条,以检测多种食品中的Hg残留。结果表明,两种试纸条兼具高灵敏度和高特异性,能满足现场快速、高效、便携式检测的需求。Xu Naifeng等建立了乳胶微球免疫层析法以检测芦笋中的Cd残留。该方法灵敏度虽高,但与Hg有16%的交叉反应率,特异性欠佳。因此,综合重金属免疫分析法的研究现状,高质量抗体的开发是未来重金属免疫分析技术的研究重点。结合重金属抗体对抗原的特异性识别与互作机制研究能够为重金属的免疫分析法提供性能更优异的抗体核心试剂。


04
结 语

本文综述了重金属抗体与抗原特异性识别及相互作用机制的3 种研究手段及进展,探讨了影响重金属抗体特异性识别抗原的关键因素,并结合食品检测中重金属免疫分析法的发展趋势,解释了重金属抗原抗体识别机制研究的重要性。目前重金属抗体对抗原的识别机制尚缺乏系统性研究,仍有进一步的探索空间。对其识别机制、相互作用的研究能为螯合剂或半抗原结构的设计及改造、抗体的定向人工调控提供理论依据,为食品中高特异性、高灵敏度的重金属免疫分析法的建立奠定基础,对其他食品小分子污染物的抗原抗体识别机制也具有一定的参考价值。根据识别机制研制出特异性更强、稳定性更高的重金属抗体并应用于实际检测,对于推进食品中重金属污染残留快速检测技术的发展具有重要意义。
引文格式:
黄俊钧, 周孟新, 吕晓丹, 等. 重金属残留免疫分析法中抗体与抗原特异性识别及相互作用机制研究进展[J]. 食品科学, 2025, 46(5): 301-309. DOI:10.7506/spkx1002-6630-20240715-139.
HUANG Junjun, ZHOU Mengxin, LÜ Xiaodan, et al. Research progress on specific recognition and interaction mechanism between antibody and antigen in immunoassay for heavy metal residues[J]. Food Science, 2025, 46(5): 301-309. (in Chinese with English abstract) DOI:10.7506/spkx1002-6630-20240715-139.
点击下方阅读原文即可查看文章相关信息。
实习编辑:李雄;责任编辑:张睿梅。点击下方阅读原文即可查看全文。图片来源于文章原文及摄图网
近期研究热点



长按或微信扫码进行注册
为系统提升我国食品营养与安全的科技创新策源能力,加速科技成果向现实生产力转化,推动食品产业向绿色化、智能化、高端化转型升级,由北京食品科学研究院、中国食品杂志社《食品科学》杂志(EI收录)、中国食品杂志社《Food Science and Human Wellness》杂志(SCI收录)、中国食品杂志社《Journal of Future Foods》杂志(ESCI收录)主办,合肥工业大学、安徽农业大学、安徽省食品行业协会、安徽大学、合肥大学、合肥师范学院、北京工商大学、中国科技大学附属第一医院临床营养科、安徽粮食工程职业学院、安徽省农科院农产品加工研究所、安徽科技学院、皖西学院、黄山学院、滁州学院、蚌埠学院共同主办的“第六届食品科学与人类健康国际研讨会”,将于 2026年8月15-16日(8月14日全天报到)在中国 安徽 合肥召开。

长按或微信扫码进行注册
会议招商招展
联系人:杨红;电话:010-83152138;手机:13522179918(微信同号)

