
 论文摘要
论文摘要  植物真菌病害对农业生产及采后农产品质量安全构成严重威胁,因此开发高效环保的新型杀菌剂具有重要意义。本研究将天然来源的对羟基肉桂酸与高活性二酰胺结构基序相结合,设计并合成了一系列新型对羟基肉桂酸 - 二酰胺衍生物。体外抗真菌活性筛选显示,多个化合物对多种植物病原真菌具有显著抑制效果,其中化合物 1-14 对核盘菌(EC₅₀=15.70 μg/mL)、化合物 1-13 对辣椒疫霉(EC₅₀=22.04 μg/mL)表现出优异活性。化合物 1-13 在辣椒叶片和果实上对辣椒疫霉展现出显著的体内抗真菌活性,化合物 1-14 对番茄和阳光玫瑰葡萄上的灰葡萄孢则呈现明显的浓度依赖性抑制作用。通过体内活性测定、碘化丙啶(PI)染色、质子动力势(PMF)评估、琥珀酸脱氢酶(SDH)活性检测及扫描电子显微镜(SEM)观察等进一步研究表明,目标化合物通过多种机制发挥抗真菌作用,包括破坏细胞膜完整性、干扰能量代谢及抑制 SDH 酶活性。分子对接和分子动力学模拟揭示了化合物与 SDH 活性口袋的稳定结合模式,密度泛函理论(DFT)计算进一步验证了其电子结构与稳定性。本研究为开发新型植物源杀菌剂提供了有价值的候选分子和理论依据,不仅为防治核盘菌、辣椒疫霉等病原菌引发的采后病害提供了高活性候选化合物,所阐明的结构 - 活性关系及多重作用机制也为天然产物基农药的合理设计提供了新思路。
植物真菌病害对农业生产及采后农产品质量安全构成严重威胁,因此开发高效环保的新型杀菌剂具有重要意义。本研究将天然来源的对羟基肉桂酸与高活性二酰胺结构基序相结合,设计并合成了一系列新型对羟基肉桂酸 - 二酰胺衍生物。体外抗真菌活性筛选显示,多个化合物对多种植物病原真菌具有显著抑制效果,其中化合物 1-14 对核盘菌(EC₅₀=15.70 μg/mL)、化合物 1-13 对辣椒疫霉(EC₅₀=22.04 μg/mL)表现出优异活性。化合物 1-13 在辣椒叶片和果实上对辣椒疫霉展现出显著的体内抗真菌活性,化合物 1-14 对番茄和阳光玫瑰葡萄上的灰葡萄孢则呈现明显的浓度依赖性抑制作用。通过体内活性测定、碘化丙啶(PI)染色、质子动力势(PMF)评估、琥珀酸脱氢酶(SDH)活性检测及扫描电子显微镜(SEM)观察等进一步研究表明,目标化合物通过多种机制发挥抗真菌作用,包括破坏细胞膜完整性、干扰能量代谢及抑制 SDH 酶活性。分子对接和分子动力学模拟揭示了化合物与 SDH 活性口袋的稳定结合模式,密度泛函理论(DFT)计算进一步验证了其电子结构与稳定性。本研究为开发新型植物源杀菌剂提供了有价值的候选分子和理论依据,不仅为防治核盘菌、辣椒疫霉等病原菌引发的采后病害提供了高活性候选化合物,所阐明的结构 - 活性关系及多重作用机制也为天然产物基农药的合理设计提供了新思路。 研究背景
研究背景  植物真菌病害是威胁全球农业安全、生产及可持续发展的主要生物限制因素,其危害贯穿从田间种植到消费者手中的整个产业链,在作物生长阶段可直接导致减产甚至绝收,在采后储存、物流和销售环节则会引发真菌腐烂,造成巨大经济损失的同时,还可能因霉菌毒素污染带来严重食品安全风险。随着消费者对优质农产品需求的增长及冷链物流的快速发展,农业和食品科学领域迫切需要开发高效、绿色的保鲜剂来控制采后病害、延长农产品货架期。天然产物凭借结构多样性、环境相容性好及作用机制独特等优势,成为新型绿色农药分子开发的重要先导化合物来源。对羟基肉桂酸作为一种广泛存在于水果、蔬菜和谷物中的酚酸,本身参与植物防御反应,其衍生物具有抗氧化、抗真菌等广谱生物活性,在农产品采后保鲜中展现出巨大潜力;而二酰胺类化合物作为合成化学中的 “优势结构”,在医药和农用化学品领域已取得显著成功,部分含二酰胺基序的杀菌剂对卵菌引起的植物病害具有优异防治效果。基于此,本研究通过合理缀合环境友好的天然对羟基肉桂酸骨架与合成易达且高效的二酰胺基序,旨在开发新型抗真菌剂,借助协同效应克服现有杀菌剂的局限性,为采后病害防治提供候选分子及天然产物基农用化学品的合理设计框架。
植物真菌病害是威胁全球农业安全、生产及可持续发展的主要生物限制因素,其危害贯穿从田间种植到消费者手中的整个产业链,在作物生长阶段可直接导致减产甚至绝收,在采后储存、物流和销售环节则会引发真菌腐烂,造成巨大经济损失的同时,还可能因霉菌毒素污染带来严重食品安全风险。随着消费者对优质农产品需求的增长及冷链物流的快速发展,农业和食品科学领域迫切需要开发高效、绿色的保鲜剂来控制采后病害、延长农产品货架期。天然产物凭借结构多样性、环境相容性好及作用机制独特等优势,成为新型绿色农药分子开发的重要先导化合物来源。对羟基肉桂酸作为一种广泛存在于水果、蔬菜和谷物中的酚酸,本身参与植物防御反应,其衍生物具有抗氧化、抗真菌等广谱生物活性,在农产品采后保鲜中展现出巨大潜力;而二酰胺类化合物作为合成化学中的 “优势结构”,在医药和农用化学品领域已取得显著成功,部分含二酰胺基序的杀菌剂对卵菌引起的植物病害具有优异防治效果。基于此,本研究通过合理缀合环境友好的天然对羟基肉桂酸骨架与合成易达且高效的二酰胺基序,旨在开发新型抗真菌剂,借助协同效应克服现有杀菌剂的局限性,为采后病害防治提供候选分子及天然产物基农用化学品的合理设计框架。 图文赏析
图文赏析 
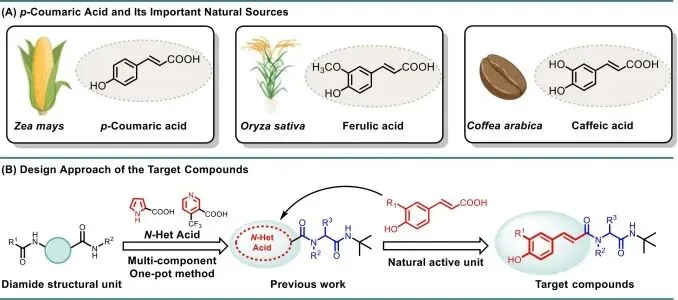 图 1:目标化合物的设计思路。(A) 对香豆酸及其重要天然来源;(B) 目标化合物的设计路线
图 1:目标化合物的设计思路。(A) 对香豆酸及其重要天然来源;(B) 目标化合物的设计路线
图 2:目标化合物的体外抗真菌活性。(A) 化合物 1–14 和 2–6 在不同浓度下对核盘菌的抑制效果;(B) 化合物 1–14 和 2–6 对核盘菌的半数有效浓度(EC₅₀);(C) 化合物 1–5 和 1–14 在不同浓度下对灰葡萄孢的抑制效果;(D) 化合物 1–5 和 1–14 对灰葡萄孢的半数有效浓度(EC₅₀);(E) 化合物 1–13 和 3–2 在不同浓度下对辣椒疫霉的抑制效果;(F) 化合物 1–13 和 3–2 对辣椒疫霉的半数有效浓度(EC₅₀)
图 3:体内活性测试。(A) 化合物 1–14 和啶酰菌胺对番茄灰葡萄孢的保护作用;(B) 化合物 1–14 和啶酰菌胺对番茄灰葡萄孢的治疗作用;(C) 化合物 1–14 和啶酰菌胺对阳光玫瑰葡萄灰葡萄孢的防治效果;(D) 化合物 1–13 和啶酰菌胺对辣椒果实辣椒疫霉的保护作用;(E) 化合物 1–13 和啶酰菌胺对辣椒果实辣椒疫霉的治疗作用;(F) 化合物 1–14 和啶酰菌胺对油菜核盘菌的防治效果;(G) 化合物 1–13 和啶酰菌胺对辣椒叶片辣椒疫霉的防治效果;(H) 化合物 1–13 和啶酰菌胺对辣椒幼苗辣椒疫霉的防治效果;(I) 辣椒幼苗的病情指数(“*” 表示差异显著(P<0.05),“ns” 表示无显著差异)
图 4:抗真菌作用机制阐明。(A) 化合物 1–14 和二甲基亚砜(空白对照)处理后的孢子碘化丙啶(PI)染色图;(B) 化合物 1–14 和二甲基亚砜(空白对照)处理后的菌丝碘化丙啶(PI)染色图;(C) 化合物 1–14(50 µg/mL)和二甲基亚砜(空白对照)处理后核盘菌菌丝的扫描电子显微镜(SEM)分析;(D) 质子动力势和碘化丙啶(PI)染色的荧光强度;(E) 化合物 1–13 和啶酰菌胺对琥珀酸脱氢酶(SDH)的抑制率
图 5:分子对接和分子动力学模拟。(A) 化合物 1–13 和啶酰菌胺与琥珀酸脱氢酶(SDH)的分子对接结果;(B) 化合物 1–13 与琥珀酸脱氢酶(SDH)结合的能量分解分析;(C) 啶酰菌胺与琥珀酸脱氢酶(SDH)结合的能量分解分析;(D) 化合物 1–13 和啶酰菌胺与琥珀酸脱氢酶(SDH)的结合模型及其在模拟过程中的均方根偏差(RMSD)变化;(E) 模拟过程中琥珀酸脱氢酶(SDH)核心结合位点的均方根波动(RMSF)值;(F) 化合物 1–13 和啶酰菌胺与琥珀酸脱氢酶(SDH)结合形成的氢键数量随时间的变化
图 6:化合物 1–13、1–14 和啶酰菌胺的密度泛函理论(DFT)计算结果。(A) 化合物 1–13、1–14 和啶酰菌胺的分子静电势(ESP)及极值分布;(B) 三种化合物的分子静电势(ESP)分布定量数据;(C) 三种不同分子的前线轨道分布及相应轨道能量
 研究结论
研究结论 本研究成功设计并合成了一系列新型对羟基肉桂酸 - 二酰胺衍生物,并对其抗真菌活性进行了系统评价。结构 - 活性关系分析阐明了不同取代基对活性的影响,发现 R³ 取代基的电子性质是决定病原菌谱选择性的关键因素:吸电子卤素基团有利于提升对核盘菌的活性,而供电子羟基则有助于增强对辣椒疫霉等卵菌的活性。代表性化合物 1–14 和 1–13 在体外和体内试验中均表现出显著的抗真菌功效,对核盘菌、灰葡萄孢和辣椒疫霉具有良好的防治潜力。机制研究表明,这些化合物通过多种途径发挥抗真菌作用,包括破坏细胞膜完整性、抑制琥珀酸脱氢酶(SDH)酶活性以及干扰能量代谢。计算生物学研究进一步明确了它们与靶标酶的稳定相互作用模式。本研究不仅为防治农产品采后病害提供了具有潜力的候选分子,还为天然产物基农药的合理设计提供了新的思路和方法学支持。柯少勇:湖北省农业科学院研究员。目前主要研究领域:天然资源导向的农药及药物的先导发现及化学生物学。
本研究成功设计并合成了一系列新型对羟基肉桂酸 - 二酰胺衍生物,并对其抗真菌活性进行了系统评价。结构 - 活性关系分析阐明了不同取代基对活性的影响,发现 R³ 取代基的电子性质是决定病原菌谱选择性的关键因素:吸电子卤素基团有利于提升对核盘菌的活性,而供电子羟基则有助于增强对辣椒疫霉等卵菌的活性。代表性化合物 1–14 和 1–13 在体外和体内试验中均表现出显著的抗真菌功效,对核盘菌、灰葡萄孢和辣椒疫霉具有良好的防治潜力。机制研究表明,这些化合物通过多种途径发挥抗真菌作用,包括破坏细胞膜完整性、抑制琥珀酸脱氢酶(SDH)酶活性以及干扰能量代谢。计算生物学研究进一步明确了它们与靶标酶的稳定相互作用模式。本研究不仅为防治农产品采后病害提供了具有潜力的候选分子,还为天然产物基农药的合理设计提供了新的思路和方法学支持。柯少勇:湖北省农业科学院研究员。目前主要研究领域:天然资源导向的农药及药物的先导发现及化学生物学。曹秀芳:华中农业大学化学学院副教授,硕士生导师。主要研究方向:新杂环农药、医药的设计合成;天然活性物质提取及结构衍生化。
本研究得到以下项目的资助:
国家重点研发计划(项目编号:2023YFD1700700)
作物遗传改良国家重点实验室开放基金(项目编号:ZK202401)
湖北省农业科学院青年科学基金(项目编号:2025NKYJJ34)
湖北省农业科技创新中心(项目编号:2025-620-000-001-023)
https://doi.org/10.1016/j.postharvbio.2026.114180
标注 “原创” 仅表明为原创编译,本平台不主张对原文享有版权。
本平台转载内容仅出于学术交流与信息传播之目的,并不代表本平台观点,亦不意味着证实内容的真实性。
转载文章的版权归原作者所有,若原作者不希望作品被转载或存在侵权行为,请联系本平台删除。
由于编译水平有限,推文或简历中若有不妥之处,我们深表歉意,请联系本平台进行修改或删除。