
导读:围绕胃肠环境下屎肠球菌与单核细胞增生李斯特菌的相互作用展开系统探究,通过动物活体实验、体外胃肠模拟、转录组分析与基因敲除验证等手段,明确了屎肠球菌 B1 对李斯特菌的抑制效果,发现李斯特菌会通过形成细菌微室抵御益生菌胁迫,且屎肠球菌的 enlA 基因是触发这一防御反应的关键因子,同时 pduA 基因参与调控细菌微室的形成以增强致病菌抗性,该成果揭示了胃肠环境中益生菌与致病菌全新的互作规律,为食品微生物安全防控与益生菌功能开发提供了重要理论支撑。
 研究背景
研究背景 
(一)食源性致病菌的安全威胁
单核细胞增生李斯特菌是危害极高的食源性致病菌,可通过污染肉制品、乳制品等食物进入人体,能耐受低温环境,还可突破人体胃肠道屏障引发系统性感染,对孕妇、老人、免疫力低下人群的致死风险显著,全球范围内多次爆发相关食品安全事件,成为食品行业与公共卫生领域的重点防控对象。
(二)益生菌抑菌的研究空白
屎肠球菌作为常用益生菌,在抑制李斯特菌、调节肠道健康等方面展现出良好潜力,已有研究证实其可通过多种方式抵御致病菌感染,但大多聚焦于抑菌效果的表面验证,对于胃肠道复杂环境下,屎肠球菌如何发挥抑菌作用、李斯特菌又通过何种机制抵抗益生菌胁迫的深层分子机制,始终未能得到清晰阐释。
(三)胃肠环境下互作机制亟待突破
人体胃肠道存在胃酸、胆盐等复杂应激条件,会显著改变细菌的生存状态与基因表达,常规体外培养环境无法还原真实互作场景。同时,细菌微室作为致病菌适应环境胁迫的重要结构,其在益生菌与李斯特菌互作中的作用尚未被挖掘,厘清这一机制,对开发高效益生菌制剂、精准防控致病菌感染至关重要。
 核心内容
核心内容 
(一)屎肠球菌 B1 可有效抑制李斯特菌感染
作者团队通过小鼠灌胃实验证实,提前摄入屎肠球菌 B1,能显著降低李斯特菌感染后小鼠的体重下降幅度,减少致病菌在肠道、肝脏、脾脏等组织中的定殖量,同时降低肠道炎症因子水平,修复肠道黏膜损伤。在体外模拟胃肠消化体系中,屎肠球菌 B1 同样能显著抑制李斯特菌的存活,下调其应激耐受通路与毒力基因的表达。
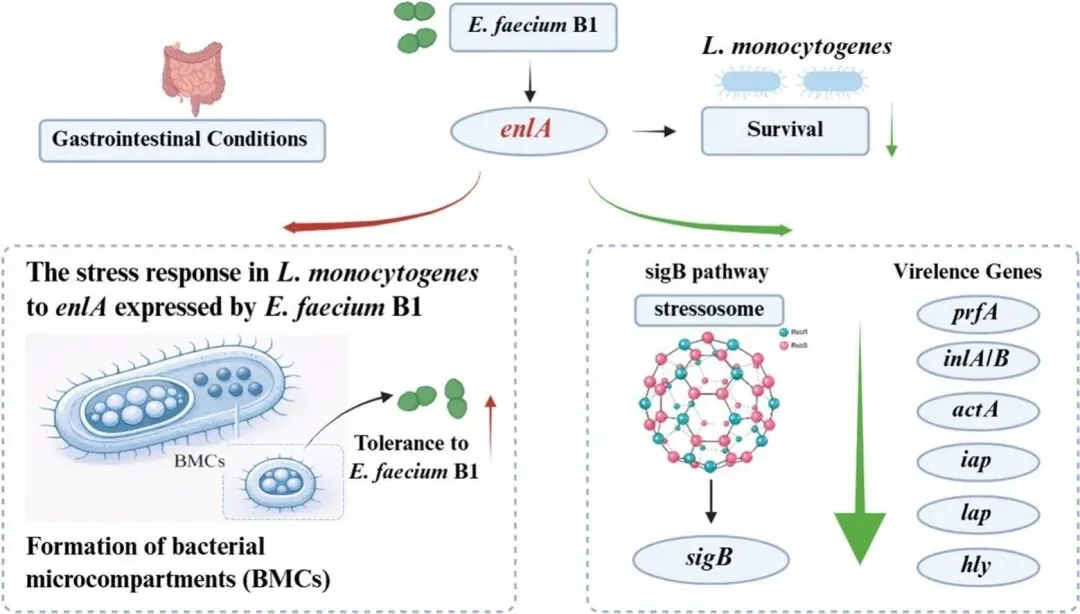
(二)李斯特菌通过形成细菌微室抵御益生菌胁迫
研究团队通过转录组分析与电镜观察发现,在屎肠球菌 B1 的胁迫下,李斯特菌体内细菌微室相关基因表达大幅上调,并成功形成细菌微室结构。进一步通过基因敲除验证证实,李斯特菌的 pduA 基因是维持细菌微室结构的关键,该基因缺失后,李斯特菌抵御屎肠球菌的能力显著下降;而屎肠球菌的 enlA 基因是触发李斯特菌形成细菌微室的核心因子,缺失该基因后,益生菌无法诱导致病菌产生这一防御结构。
 亮点价值
亮点价值 
(一)科学层面:首次揭示全新互作调控通路
该研究突破了传统益生菌抑菌研究的局限,首次在胃肠环境下证实 **“益生菌关键基因→致病菌防御结构→生存抗性”** 的完整调控通路,明确了 enlA 与 pduA 两个核心基因的功能,填补了益生菌诱导致病菌形成细菌微室这一领域的研究空白,为解析微生物间互作机制提供了新的理论范式。
(二)应用层面:为食品安全与益生菌开发提供靶点
在食品工业中,该成果可指导开发针对李斯特菌的新型生物防控技术,提升发酵肉制品等食品的安全性;在益生菌领域,明确 enlA 基因作为核心抑菌功能靶点,可用于高效益生菌菌株的筛选与改造,同时基于 pduA 基因设计防控策略,能有效阻断李斯特菌的防御途径,提升抑菌效果,兼具科学价值与产业应用潜力。
 图文赏析
图文赏析  图 1 屎肠球菌 B1 缓解小鼠体内单核细胞增生李斯特菌的感染图 4 体外胃肠消化过程中 pduA 基因在调控单核细胞增生李斯特菌对屎肠球菌 B1 抗性中的作用图 5 体外胃肠消化过程中屎肠球菌 B1 的转录组学研究图 8 屎肠球菌 B1 的 enlA 基因介导抑制小鼠体内单核细胞增生李斯特菌感染
图 1 屎肠球菌 B1 缓解小鼠体内单核细胞增生李斯特菌的感染图 4 体外胃肠消化过程中 pduA 基因在调控单核细胞增生李斯特菌对屎肠球菌 B1 抗性中的作用图 5 体外胃肠消化过程中屎肠球菌 B1 的转录组学研究图 8 屎肠球菌 B1 的 enlA 基因介导抑制小鼠体内单核细胞增生李斯特菌感染
结论展望 
(一)研究总结
该研究系统解析了胃肠环境下屎肠球菌 B1 抑制单核细胞增生李斯特菌的作用机制,证实 enlA 基因是屎肠球菌发挥抑菌作用的核心,同时发现李斯特菌可通过 pduA 基因调控细菌微室形成应对应激,构建了完整的益生菌与致病菌互作网络,为理解肠道微生物相互作用、保障食品微生物安全提供了全新的科学依据。
(二)未来展望
后续可基于该研究成果,开展多菌株、多环境下的验证研究,拓展益生菌抑菌机制的适用范围;同时可围绕 enlA 基因开发重组益生菌制剂,结合 pduA 基因抑制剂设计复合防控方案,进一步提升李斯特菌防控效率。此外,还可深入探究该互作机制对人体肠道菌群的影响,推动基础研究成果向食品、医疗等实际应用场景转化。
叶可萍:南京农业大学教授、博士生导师,现任国家肉品质量安全控制工程技术研究中心副主任,南京农业大学食品科技学院食品质量与安全系主任,农业农村部肉及肉制品质量检验测试中心(南京)质量负责人。近年来主要围绕肉品品质及贮藏保鲜、肉品中病原菌预测与控制、真菌蛋白仿制肉等方向开展研究工作。主持国家自然科学基金面上项目和青年项目3项,国家“十四五”重点研发计划项目课题、国家“十四五”重点研发计划揭榜挂帅项目任务,以及江苏省自然科学基金面上项目、新疆重大科技专项任务、国家食品安全风险评估中心项目和企业重大产学研合作项目等20余项。以第一作者或通信作者在Chemical Engineering Journal、Food Hydrocolloids、Food Chemistry、Food Control、Food Packaging and Shelf Life、Frontiers in Cellular and Infection Microbiology、International Journal of Molecular Sciences、Frontiers in Microbiology、Meat Science、Food Research International等期刊发表论文70余篇。申请发明专利5项,获授权发明专利2项、实用新型专利2项,参与制定标准1项,参编教材与书籍2部,获中国食品科学技术学会科技创新一等奖。
国家自然科学基金(32172267)
江苏省自然科学基金(BK20221516)
国家卫生健康委食品安全风险评估重点实验室项目(202403)
https://doi.org/10.1016/j.cej.2026.175904

本文为编译科普解读,仅用于非商业学术交流、学习参考,不构成出版、转载或商用行为。文中核心研究内容、数据、图表版权均归原作者及期刊出版机构所有,原文请查阅期刊官方平台。
标注 “原创” 仅代表本账号原创梳理、翻译解读,不侵占原文著作权;内容为独立撰写,不代表原论文作者、期刊、出版机构及本平台立场,不佐证相关研究真实性。
如不希望相关内容被转载或存在侵权等问题,均可联系平台小编,即刻安排修改、下架删除;受编译整理水平所限,内容若有疏漏不足,恳请谅解,欢迎随时私信我们调整完善。
如不希望相关内容被转载或存在侵权等问题,均可联系平台小编,即刻安排修改、下架删除;受编译整理水平所限,内容若有疏漏不足,恳请谅解,欢迎随时私信我们调整完善。