《食品科学》:中国农业大学吕晨艳教授等:蛋白质自组装:从单分子设计到多维度超分子组装
- 2026-05-08 11:23:55

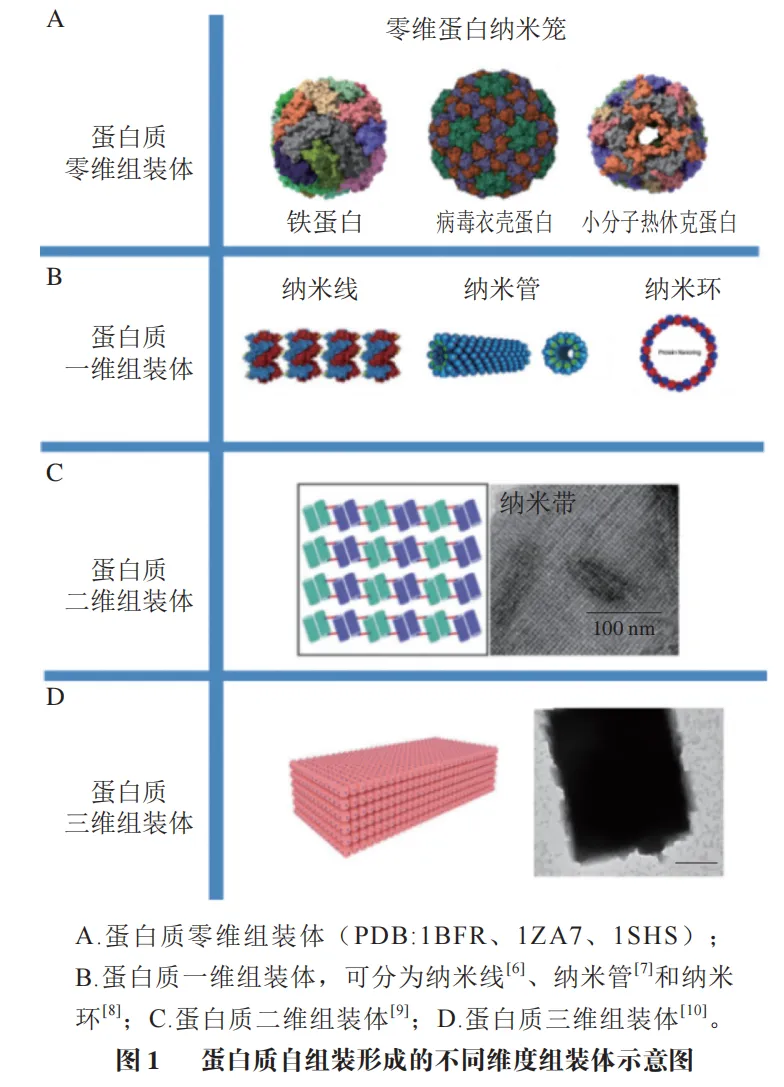
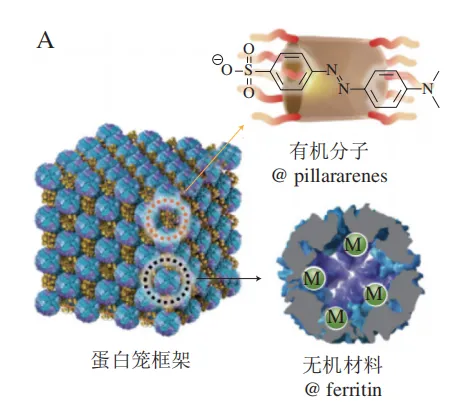
蛋白质的自组装行为广泛存在于自然界中,能够执行精细而复杂的生化功能,例如肌动蛋白作为肌原纤维结构的一部分可以形成纤维状结构,参与细胞骨架形成和肌肉收缩;藻胆蛋白组装形成的光捕获系统在光合作用中实现高效能量传递;细菌S层蛋白则通过高度有序的排列实现分子识别与环境适应功能。这些天然系统不仅展现出蛋白质自组装在结构与功能的核心作用,也揭示了其背后精密的分子设计原理。然而,天然蛋白质组装体系往往受到结构单一性和环境敏感性的限制,难以直接满足多样化的人工应用需求。此外,某些蛋白质的错误组装还与疾病状态密切相关,如β-淀粉样蛋白聚集与神经退行性疾病的发生相关,进一步凸显了对蛋白质组装过程进行理性调控的重要性。根据组装维度的不同,蛋白组装体可以分为4 种:1)蛋白质寡聚体通过单分子设计形成零维笼状结构;零维组装体在空间的所有3 个维度上尺寸都有限,形成一个封闭的纳米结构(如铁储藏蛋白和病毒衣壳)(图1A)。2)蛋白质沿一个方向延伸形成的一维结构,包括纳米线、纳米环和纳米管等,而在另外2 个维度上的尺寸是纳米级(图1B)。3)蛋白质在2 个方向上延伸,形成片层、薄膜或晶格结构,而在第3个维度(厚度)上的尺寸是纳米级(图1C)。4)蛋白质在3 个空间维度上都进行延伸,形成晶体、超晶格或框架结构(图1D)。
目前,随着基因工程、超分子化学、计算机模拟计算、人工智能等技术的快速发展,研究者已能够通过对蛋白质序列、结构和界面相互作用的精确设计,实现从零维纳米笼到三维超晶格的多维度可控组装。这种“自下而上”的仿生设计策略,不仅使人们能够更好地理解天然蛋白质组装的结构基础与调控机制,更为创造具有新颖功能和优异性能的人工蛋白质材料提供了强大工具。通过合理设计蛋白质亚基间和分子间的共价与非共价相互作用,研究者已成功构建出多种结构精确、功能可编程的蛋白质组装体,并在活性物质包埋与递送、人工光捕获系统、生物催化等领域展现出广阔的应用前景。
中国农业大学食品科学与营养工程学院的孙明炀、臧佳辰、吕晨艳*等旨在系统梳理蛋白质自组装领域的最新研究进展。首先涵盖蛋白质自组装策略,包括对称融合表达、计算机从头设计和关键界面设计等方法;继而详细讨论蛋白质组装中的作用力类型及其调控手段;最后,将从单分子(零维)和多维(一维、二维、三维)两个层面深入分析蛋白质组装体的设计原理、结构特性与功能应用,以期推动蛋白质材料在基础研究和实际应用中的进一步发展。


01
蛋白质自组装的策略
天然蛋白质通常具有均一尺寸、明确结构及广泛的生物学功能,然而其尺寸和形状单一,限制了其进一步应用。通过蛋白质自组装策略,可以设计和构建零维蛋白质及其一维、二维和三维阵列,从而克服天然蛋白质笼的局限性,实现更广泛的应用。用于蛋白质自组装的设计策略主要有对称融合表达策略、计算机从头设计策略和关键界面设计策略。
1.1 对称融合表达策略
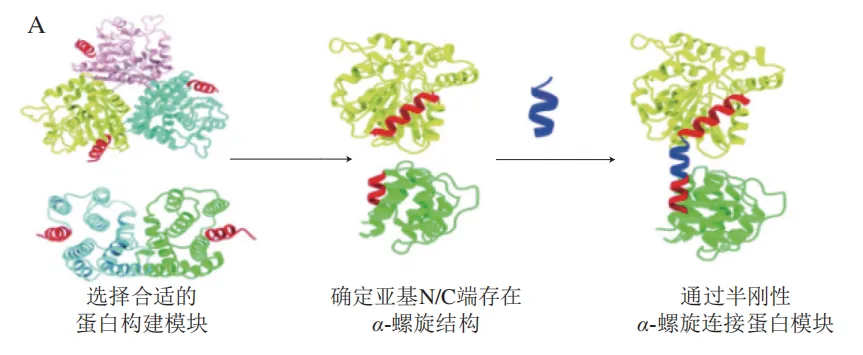
目前晶体结构已经被解析的蛋白通常具有良好的对称性,基于天然蛋白固有对称自组装的特性,研究人员提出了对称融合表达策略,用于构建形状不同、结构多样的多维蛋白质组装体。该策略通过基因融合技术将天然蛋白寡聚体与不同功能的蛋白质连接,以实现自组装。一般来说,对称融合表达策略包括如下3 个步骤(图2A)。1)筛选合适的蛋白构建模块:从天然蛋白中选择合适的同源多聚体(如二聚体或三聚体),要求其N端或C端含有α-螺旋结构,以便后续连接;2)基于对称性进行排列组合:依据几何对称原则,优化蛋白构建模块的组合方式,使其符合预设的空间结构;3)连接蛋白质构建模块:将蛋白模块通过半刚性α-螺旋(通常由5~9 个氨基酸组成)首尾连接,最终自组装形成高分子质量多面体。基于上述策略,Padilla和Lai等通过半刚性α-螺旋将二聚体流感病毒基质蛋白与三聚体溴代过氧化氢酶连接,自组装形成了形状各异的蛋白结构,包括四面体、八面体和十二面体。对称融合策略不仅可用于构建蛋白质多样的结构,还能拓展至多维蛋白质组装体的设计。通过选取具有不同对称性的蛋白质,并采用基因融合技术将其连接,已成功制备出一维线性结构、二维平面晶格及三维组装体。尽管该策略已取得一定成果,但基因融合过程可能影响蛋白质折叠和空间构象的精确调控。因此,其在角度设计与结构稳定性方面仍存在诸多问题,限制了进一步应用。
 |  |  |

1.2 计算机从头设计策略
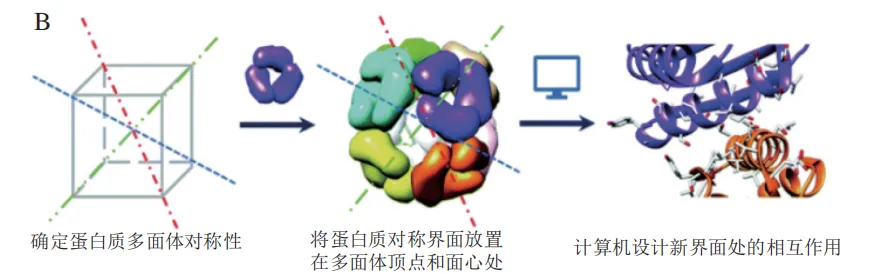
蛋白质的从头设计是一种通过计算机辅助建模,设计出能够折叠成目标结构氨基酸序列的策略。其核心原则是蛋白质会折叠到最低自由能状态,因此在设计过程中,优化界面能量和构象稳定性是关键。近年来,随着计算生物学的快速发展,科学家们已开发出多种软件工具(如Rosetta、AlphaFold、I-TASSER),通过计算机模拟实现蛋白质的精准设计。2024年诺贝尔化学奖获得者David Baker率先提出了计算机从头设计策略用于蛋白质组装,主要步骤如下(图2B):1)根据目标结构将蛋白建模块进行对称对接;2)设计低能量的蛋白质-蛋白质界面,以驱动自组装。David Baker团队以三聚体蛋白为构建模块,将其三重轴界面精准定位在四面体和八面体的顶点与面心处。随后,通过Rosetta进行序列设计,构建出低能量且对称的蛋白质-蛋白质界面。该策略成功驱动三聚体蛋白组装成具有八面体对称性的二十四聚体,以及具有四面体对称性的十二聚体纳米笼。此外,David Baker团队近期还推出了基于扩散模型的蛋白质设计工具RoseTTAFold Diffusion(RFdiffusion),在对单体数目和序列长度进行限定后,RFdiffusion可以设计出单体亚基,并按照指定的点群对称性空间排布得到对称寡聚蛋白,该工具目前已成功应用于二面体、四面体以及二十面体蛋白组装体的设计。
1.3 关键界面设计策略
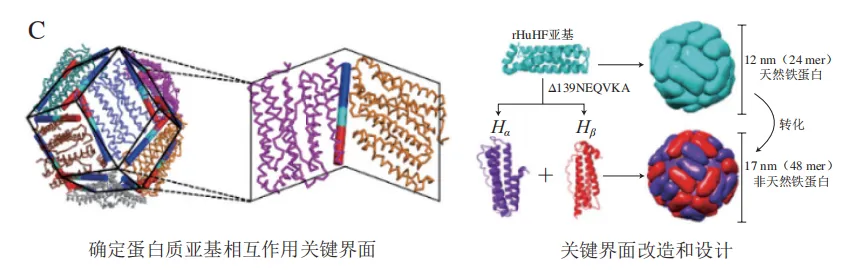
尽管上述策略在诱导蛋白质组装方面已取得了诸多进展,但是其设计周期长、操作复杂、对精度的要求非常高。天然蛋白质关键亚基间界面的作用力在维持蛋白质的构象中起着非常关键的作用,设计和改造蛋白关键界面对蛋白质的组装可能会有重要影响。近年来,本课题组提出了关键界面设计策略,该策略主要包括3 步:1)根据晶体结构对蛋白质进行界面分析,确定关键界面;2)进行关键界面设计,在关键界面去除位阻效应,引入共价或非共价作用力(图2C);3)调节溶液的环境条件(pH值、盐浓度)诱导蛋白质自组装,形成零维、一维、二维和三维组装阵列。利用该策略,通过在铁蛋白C3~C4界面移除特定氨基酸序列可以将二十四聚体铁蛋白笼转化为四十八聚体纳米笼,而插入特定氨基酸序列可诱导形成十六聚体扁球体。与其他蛋白质组装策略相比,该策略具有成本低、操作简单、可保持蛋白质天然活性、普适性强等优点。

02
蛋白质自组装的作用力及影响因素
对称融合表达策略、计算机从头设计策略和关键界面设计策略的成功实施,离不开对驱动组装过程中作用力的精准调控。这些策略通过合理设计或改造蛋白质间的相互作用界面,有效利用了多种化学作用力,从而实现对自组装路径与最终结构的精确控制。此外,蛋白质作为生命活动的主要承担者,其功能的实现依赖于精确的三维结构,这些结构的形成和维持同样离不开多种作用力的协同调控。蛋白质自组装是一个复杂而精妙的过程,主要由亚基间和蛋白质分子间的作用力共同驱动,包括共价作用和非共价作用两大类。
2.1 蛋白质亚基间自组装作用力
蛋白质在亚基间作用力的驱动下组装构成了蛋白质零维结构,对这些作用力进一步改造可以实现蛋白质的单分子设计。在构成亚基间的作用力中,非共价作用在蛋白质亚基间作用力中起主导作用,主要包括静电相互作用、氢键、疏水相互作用等。其中,氢键在维持蛋白质结构中起着极其重要的作用,它不仅是构成蛋白质二级结构的主要作用力,还广泛用于维持蛋白的三级结构,如蛋白质亚基间侧链与侧链的相互作用。氨基酸序列、离子浓度、温度、pH值等因素影响着氢键的形成与稳定性。除氢键外,疏水相互作用同样是稳定蛋白质结构的关键因素,在维持蛋白质三维结构中发挥着突出的作用。在亲水环境中,蛋白质的疏水基团或侧链相互靠近并折叠在分子内部,从而形成更为稳定的空间构象。蛋白质溶液中的熵增是产生疏水相互作用的主要动力,与介质水的有序度改变有关,温度和溶剂均会影响疏水相互作用;此外,一些非极性溶剂及去污剂(如尿素和盐酸胍)能破坏疏水相互作用,进而导致蛋白质变性。静电相互作用通常发生于蛋白质中带负电的酸性氨基酸与带正电的碱性氨基酸之间,pH值可以影响氨基酸基团的电离而改变氨基酸带电情况,因此,通过调节pH值可以实现对蛋白质亚基间静电相互作用的调控。除了上述非共价作用,金属配位作用也广泛存在于蛋白质亚基间。自然界中5%~10%的蛋白寡聚体在金属离子驱动下形成稳定的四级结构,这些金属离子往往还充当催化中心,参与关键的生物催化过程。尽管上述非共价作用具有可逆性和动态调控的特点,但其作用力强度较弱,在复杂的溶液条件下不稳定。相比之下,共价作用通过形成稳固的化学键为蛋白质自组装提供稳定性和可控性。其中,半胱氨酸介导的二硫键是最常见的共价作用,其键能高达60 kcal/mol,相比非共价作用高出一个数量级,其更加稳固。
2.2 蛋白质分子间自组装作用力
基于分子间相互作用,多个蛋白质分子能够进一步进行组装,从而形成不同维度的超分子组装体。在蛋白质分子间作用力的设计中,作用力的引入通常只需在蛋白质界面的特定位置对一个或多个氨基酸进行定点突变即可实现:如带电氨基酸(如谷氨酸、天冬氨酸等)间的静电相互作用;疏水氨基酸(如亮氨酸、缬氨酸等)驱动的疏水相互作用;芳香族氨基酸(如苯丙氨酸、酪氨酸等)发生的π-π相互作用。从蛋白质组装设计的角度来看,金属配位键有独特的优势,其配位作用强度高于其他非共价相互作用,并具有可逆性,通过设计氨基酸-金属离子配位作用,可以实现蛋白质分子间的有序组装。除了上述由氨基酸突变直接介导的非共价作用之外,基于特异性分子识别的主客体作用也为蛋白质组装提供了另一条高效途径,具有高选择性和刺激响应性的特点。在主客体作用中,主体为蛋白质分子,客体通常为能够被蛋白质特异性识别和结合的小分子或辅因子,其可被用于诱导蛋白质分子间自组装,构建动态、刺激响应型的组装体,常见用于蛋白质组装的主客体包括链霉亲和素-生物素和细胞色素/肌红蛋白-血红素等。
虽然上述非共价作用为蛋白质组装提供了重要的驱动力,但其相对较弱的结合强度在一定程度上限制了组装体的稳定性。为了克服这一局限,研究者常常引入更强、更稳定的共价作用以实现蛋白质分子间自组装结构的精确调控。通过引入合适距离和角度的半胱氨酸以生成二硫键,并可以通过改变环境氧化还原条件实现可逆反应。除了二硫键,酪氨酸氧化等共价作用也常作为蛋白质组装设计策略,用于指导蛋白质超分子结构的精确调控。
值得注意的是,蛋白质组装并非由单一作用力驱动,而是非共价与共价相互作用协同的结果,因此,合理设计蛋白质自组装作用力、精确调控蛋白质自组装仍具有较大挑战。

03
蛋白质单分子及超分子自组装研究进展
3.1 基于亚基间作用力调控的蛋白质单分子自组装研究进展
蛋白质纳米笼作为一类重要的零维组装体,其独特的区室化结构在生物医学领域展现出显著优势。这类结构不仅能够为生物化学反应提供空间限域环境,有效保护敏感物质免受外界环境干扰和中间产物的毒性作用,还能通过精准的分子设计实现载运效率和功能多样性的显著提升。目前,研究者已成功通过共价和非共价相互作用的协同调控,构建了多种功能各异的蛋白质零维组装体。
在共价作用调控方面,二硫键的设计展现出独特的优势。本团队基于八聚体碗状铁蛋白构建模块,通过引入二硫键实现了纳米笼尺寸和形貌的可控转换,在亚基间插入二硫键会使其转化为十六聚体椭球纳米笼,而删除亚基内二硫键的同时插入亚基间二硫键则蛋白在溶液中形成四十八聚体的蛋白质笼,这一研究能够基于同一构建模块构建出尺寸各异的笼状结构,为纳米笼的精准设计提供了新思路。Gu Chunkai等进一步拓展了该策略的应用价值,他们通过计算机辅助设计在铁蛋白界面精确引入二硫键,显著提升了其耐酸性,使其在强酸条件下仍能保持结构完整性,这一突破为开发消化道稳定递送系统奠定了基础。值得注意的是,二硫键的稳定作用在多种病毒衣壳(如人乳头瘤病毒、石斑鱼神经坏死病毒和猿猴病毒)的笼状结构维持中也发挥着关键作用。
相较于共价作用,非共价相互作用在蛋白质零维组装中的应用更为广泛。上述的对称融合表达和计算机从头设计策略大多依赖于蛋白质亚基间的非共价相互作用。以铁蛋白为例,其组装行为对环境条件表现出高度敏感性:海栖热袍菌铁蛋白和火焰色古生球菌铁蛋白在生理条件下以二聚体形式存在,但在高离子强度(Ca2+、Mg2+、Na+)下可组装为二十四聚体纳米笼,这主要归因于阳离子对C3~C4界面静电斥力的屏蔽效应。通过分子设计可进一步优化纳米笼的功能特性,如将火焰色古生球菌铁蛋白改造为K150A/R151A突变体后,其结构从开放的四面体转变为封闭的八面体,显著提高了活性物质的包封效率。对来自大肠杆菌的细菌铁蛋白进行零维组装调控研究,为理解蛋白质自组装机制提供了重要启示,该蛋白在天然状态下存在二聚体和二十四聚体的动态平衡,而其铁储存功能严格依赖于二十四聚体形式。Ardejani等通过计算机辅助设计,在C3界面引入芳香氨基酸(酪氨酸、苯丙氨酸和色氨酸),利用π-π相互作用成功稳定了二十四聚体组装形式。进一步的丙氨酸扫描结果显示,C3界面的E128、R61、Y114和C2界面的R30是维持二十四聚体结构的关键残基。最近的研究表明,在温和条件(pH<8.5、NaCl浓度<2 mmol/L)下诱导的细菌铁蛋白组装更有利于保持包埋物质的生物活性,这为开发生理相容性递送系统提供了新策略。
3.2 基于蛋白质分子间作用力调控的超分子多维自组装研究进展
蛋白质分子间作用力的精准调控,包括共价键与非共价相互作用,已成为实现其高维度自组装的关键手段。蛋白质可通过共价交联作用、静电相互作用、配位作用、π-π堆积、疏水相互作用等多种相互作用驱动自组装,形成从一维纤维、二维阵列到三维晶格的多样化结构,不仅模拟了天然蛋白质组装体的复杂结构与动态响应行为,也为新型生物功能材料的开发提供了强大平台。本节聚焦于蛋白质超分子自组装中的维度控制策略,分别从一维、二维及三维组装体系总结近年来基于作用力调控的设计策略、结构特征与功能应用,以期为未来精准构建蛋白质材料提供设计思路与理论参考。
3.2.1 蛋白质的一维组装
一维线性组装是蛋白质沿一个方向延伸形成的一维结构。胶原蛋白和肌动蛋白是自然界中存在的天然线性组装蛋白质。近年来,研究学者基于共价作用和非共价作用设计了多种一维自组装蛋白质纳米结构。
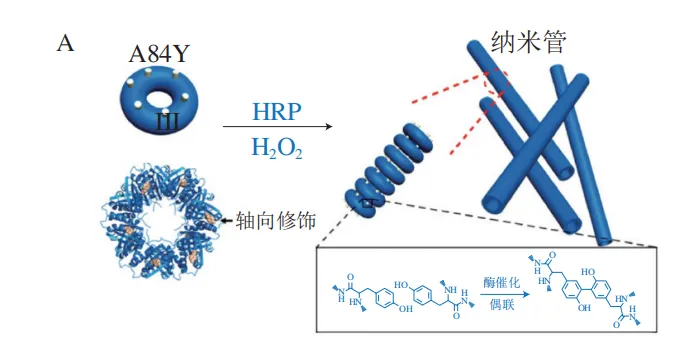
在共价作用方面,Ballister等将位于六聚体环状血红素载体蛋白环两侧的G90和R157突变为半胱氨酸,氧化形成二硫键后可以形成一维纳米管。通过对体外组装条件的pH值和离子强度进行优化可以使纳米管长达100 nm。Zhao Linlu等以稳定蛋白1(SP1)为构建模块设计出了酶触发的一维组装结构,该蛋白是一种天然十二聚体,12 个相同的亚基通过疏水相互作用结合形成一个双层六元环。如图3A所示,通过对Ala84氨基酸定点突变获得SP1A84Y变体,在过氧化氢和辣根过氧化物酶(HRP)存在时,SP1突变体的轴向Tyr残基与相邻突变体的Tyr残基发生共价交联,并沿C6对称轴形成线性蛋白质纳米管。
 |  |
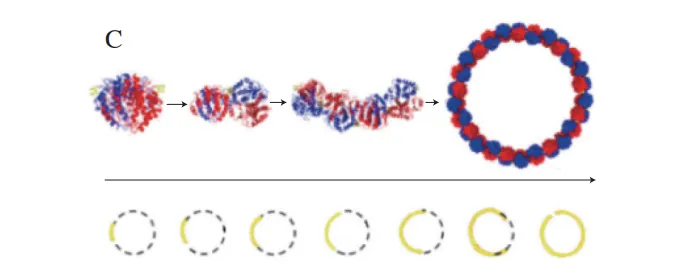 |  |

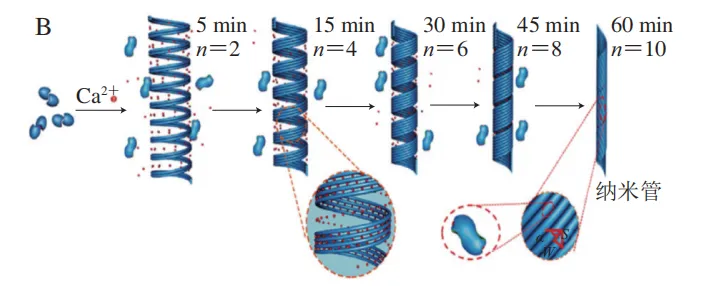
非共价相互作用因其可逆性和环境响应性,在一维组装中展现出独特优势。基于Rubisco能够在羧酶体中组装,Zeng Ruiqi等利用π-π相互作用构建了受NaCl调控的Rubisco一维组装体,将酶催化效率提升了40%,能显著提高羧化酶活性。Zhang Jipeng等利用酶解α-乳清蛋白作为自组装模块,在Ca2+的诱导下可形成β-折叠结构,并进一步自组装形成中空一维纳米管。通过对α-乳清蛋白一维组装过程分析,该团队揭示了其自组装的机制如下:1)酶解α-乳清蛋白在疏水相互作用下形成二聚体;2)Ca2+进一步诱导蛋白构象变化,β-折叠含量增加;3)在Ca2+配位作用下,蛋白构象由β-折叠向细丝转变,这些细丝通过静电排斥作用形成螺旋带,并逐渐沿着纵向伸长和横向聚集形成纳米管(图3B)。除了在一个方向上延伸形成纳米线外,蛋白质构建单元还可以一定的曲率弯曲形成闭合环。具有C2对称性的谷胱甘肽S-转移酶表面具有“V”形金属结合基序,在Ni2+配位以及非共价相互作用下其能够以固定曲率自组装,形成高度有序的蛋白质纳米环(图3C)。纳米环的直径可以通过改变溶液的离子强度调控,在高盐浓度下蛋白质界面上的静电相互作用被减弱,可以将蛋白质纳米环的直径从367 nm减小到96 nm。
主客体作用也可诱导蛋白质自组装,其中“主体”为蛋白质,可以通过非共价相互作用识别“客体”小分子,其高特异性和可逆性使自组装保真度高,并具有刺激响应的特性。Kitagishi等设计了cyt b562蛋白突变体,在其表面引入半胱氨酸残基,使其具有结合血红素的功能,在经过变性-复性循环后,蛋白间利用蛋白-血红素的相互作用驱动形成一维线性结构,并能进一步组装形成高度均匀的单层多维蛋白质网络。凝集素和糖的特异性识别已被证明可用于蛋白一维组装体的调控与设计中,Sicard等以多价半乳糖修饰的1,3-交替杯[4]芳烃作为配体,与来源于绿脓杆菌的凝集素A组装形成规则的蛋白质纳米细丝。
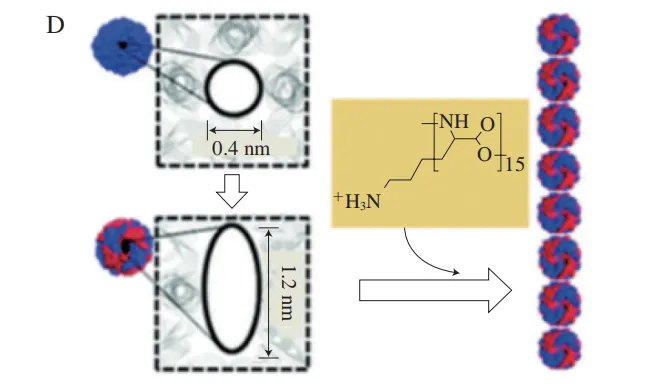
Yang等在铁蛋白多维度组装方面的研究也取得了进展,通过引入非共价作用铁蛋白可以被设计形成一维纳米线性结构。在前期研究中,本团队以来源于大豆种子的铁蛋白作为研究对象,发现在聚合度为15的α-多聚赖氨酸存在条件下可诱导铁蛋白形成线性纳米结构(图3D),在此过程中静电相互作用是主要的作用力,形成的线性材料长度可以通过多聚赖氨酸与铁蛋白的比例或孵育时间调节。近期,Zhang Xiaorong等利用Rossetta对海栖热袍菌铁蛋白的蛋白界面作用进行分析,将“头并肩”二聚体铁蛋白改造成“肩并肩”方式排列,在新的蛋白质相互作用界面设计π-π相互作用和疏水相互作用后,其能够响应Ca2+自组装形成微米级的一维纳米细丝。Chen Xuemin等将人铁蛋白C3界面的D123突变为苯丙氨酸,在pH 9.5、200 mmol/L NaCl溶液条件下可自组装成一维棒状结晶蛋白质阵列,该组装体的形成是通过苯丙氨酸形成的π-π相互作用介导。
基于共价作用与非共价作用,众多一维蛋白组装材料(纳米管、纳米线、纳米环)已成功被构建,并展现出环境响应(如pH值、离子强度、酶、Ca2+)和功能增强(如提升酶活性)的特性。铁蛋白作为模型蛋白,其多种一维组装方式尤为引人注目。总之,通过精巧的分子设计操控蛋白质间相互作用,能够实现构建结构可控、功能多样的一维蛋白质组装体。
3.2.2 蛋白质的二维自组装
二维蛋白组装体的形成需要构建模块存在2 个以上的对称轴,以满足2 个维度的面内生长方向。通常,对称轴所在的平面是形成组装的平面。受自然界中细菌S层结构的启发,二维蛋白纳米组装材料已成为极具潜力的结构平台。细菌S层作为自然界中最经典的二维蛋白组装体之一,由特定蛋白或糖蛋白高度有序排列形成,其自组装能力可通过基因工程技术进行改造,使其作为生物载体在纳米领域和仿生学中发挥重要作用。二维蛋白质组装体因其蛋白质能密集填充至平面层中的特性,在传感、诊断和疫苗开发等领域展现出重要应用。
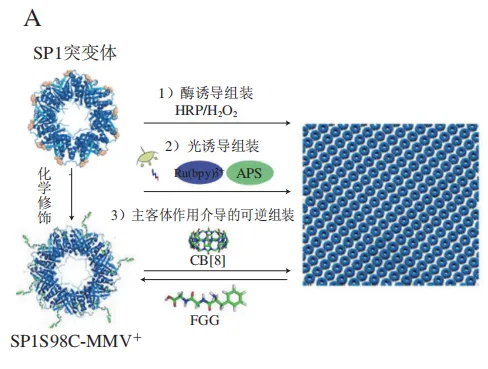
共价交联是构建蛋白质二维组装的常见策略,利用蛋白质表面功能性氨基酸残基设计共价键是实现蛋白质稳定组装的实用方法。如上所述,Zhao Linlu等在调控SP1形成蛋白纳米管的同时,在SP1环外所设计的S98Y突变体可以利用酪氨酸残基氧化偶联的性质形成二维蛋白阵列,此组装过程可以受不同条件调控(图4A):1)基于辣根过氧化物和H2O2或葡萄糖、HRP和葡萄糖氧化酶触发的酪氨酸氧化反应;2)基于三氯联吡啶钌(Ru(bpy)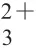 )和过硫酸铵触发的光诱导氧化反应。在后续对SP1的研究中,Li Yijia等在SP1中引入半胱氨酸制备了SP1S98C突变体,并利用主客体相互作用成功构建了具有可逆性的蛋白质二维阵列。SP1S98C与甲基紫精进行共价交联后,通过控制葫芦脲的浓度可诱导组装体尺寸的精确调节。当引入亲和力更强的客体分子Phe-Gly-Gly肽(FGG)时,葫芦脲脱离SP1S98C而选择性与FGG结合,并触发蛋白质二维结构的分解,基于客体分子竞争机制的主客体相互作用为可调节蛋白质自组装提供了新的灵感(图4A)。
)和过硫酸铵触发的光诱导氧化反应。在后续对SP1的研究中,Li Yijia等在SP1中引入半胱氨酸制备了SP1S98C突变体,并利用主客体相互作用成功构建了具有可逆性的蛋白质二维阵列。SP1S98C与甲基紫精进行共价交联后,通过控制葫芦脲的浓度可诱导组装体尺寸的精确调节。当引入亲和力更强的客体分子Phe-Gly-Gly肽(FGG)时,葫芦脲脱离SP1S98C而选择性与FGG结合,并触发蛋白质二维结构的分解,基于客体分子竞争机制的主客体相互作用为可调节蛋白质自组装提供了新的灵感(图4A)。
 |  |
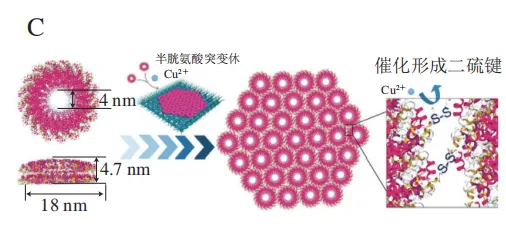 |  |

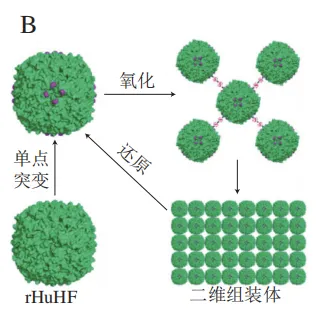
半胱氨酸(Cys)形成二硫键的过程也被应用于设计蛋白质二维组装体。如图4B所示,Zhou等将铁蛋白C4界面第162位的谷氨酸定点突变为半胱氨酸,通过控制还原剂含量、pH值以及蛋白浓度调控铁蛋白的组装,结果显示50~75 mmol/L β-巯基乙醇可通过缓慢形成二硫键而形成有序的二维组装。Zhang Shenxiang等将2 个Cys引入烟草花叶病毒外壳蛋白中,Cu2+在相邻的蛋白之间引发二硫键反应,以诱导定向二维自组装(图4C)。通过引入二硫键成功设计出具有4 nm孔径且宽度约10 μm的超大单层蛋白纳米片,并将其制备成了约40 nm的超薄超滤膜。此外,Tezcan团队利用计算机辅助模拟技术,成功构建了基于二硫键形成的二维蛋白质阵列,他们利用具有C4对称性的L-鼠李糖-1-磷酸醛缩酶(RhuA)作为构建模块,将RhuA 4 个角的氨基酸突变为Cys得到C98RhuA突变体。在氧化条件下,RhuA突变体四角处的Cys之间形成连接,驱动蛋白质二维阵列的形成。值得注意的是,由于单二硫键的灵活性,这些二维组装体在4 ℃条件下能够在1~3 d内转变为紧密排列的晶格。近期,Tezcan团队在此基础上继续探究了C98RhuA作为传感检测器的应用,可用于检测HCN气体。
共价交联在蛋白质组装体的构建方面已经广泛应用,然而天然蛋白质中可用于精确可控共价交联的氨基酸相对较少,引入非天然氨基酸是解决这个问题的有效方法之一。Yang等创新性地引入了非天然螯合氨基酸(联吡啶-丙氨酸)与Ni2+配位,成功驱动蛋白质自组装形成二维结构。该研究以来自炭疽杆菌乙酰转移酶作为构建模块,因其同源六聚体的对称性适合多向组装。联吡啶整合基团与Ni2+的高亲和力和选择性形成[Ni(bipy)2]2+配合物,通过优化Ni2+条件,实现了有序二维组装。
除共价相互作用外,赵广华研究团队基于非共价作用设计了多种二维铁蛋白阵列,所涉及的作用力包括静电相互作用、π-π相互作用、疏水相互作用、配位作用等。早在2014年,该课题组利用多聚赖氨酸的静电相互作用构建了铁蛋白二维组装阵列,在尿素扩大铁蛋白孔径的作用下,每个铁蛋白分子沿着四重轴通道有序组装形成二维平面。该研究团队进一步改造了铁蛋白的关键界面,在铁蛋白四重轴界面通过引入疏水基序(图4D)、苯丙氨酸、半胱氨酸设计出了疏水相互作用、π-π相互作用、二硫键诱导的二维组装。此外,该团队还对蛋白-蛋白界面进行了理性改造,设计疏水相互作用将海栖热袍菌铁蛋白以部分“肩并肩”的方式排列,使其由零维纳米笼转变为二维蛋白质纳米材料。
二维蛋白质组装体是受细菌S层启发、具有巨大应用潜力的纳米结构平台,其形成依赖于具有多重对称轴的蛋白质构建模块。铁蛋白、SP1蛋白、烟草花叶病毒外壳蛋白等高度对称蛋白是构建二维材料的良好模块。这些蛋白质通常具备C4对称性或多重对称轴,能够通过基因工程在其界面精准引入功能性氨基酸残基(如酪氨酸、半胱氨酸),或通过理性设计调控其相互作用界面,从而为实现有序的二维自组装提供结构基础。这些特性使它们成为制备功能化二维纳米材料的理想构建单元。
3.2.3 蛋白质的三维自组装
自然界中存在大量的三维蛋白质组装现象,构成各种细胞机器的材料。如胰腺β细胞中的胰岛素晶体,质型多角体蛋白和过氧化物酶体醇氧化酶蛋白质晶格可作为储存、搭建和催化的稳定平台。根据蛋白质三维组装体的组成不同,其可分为蛋白质-蛋白质三维组装体和蛋白质-纳米颗粒共组装体。
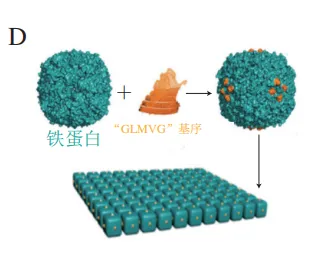
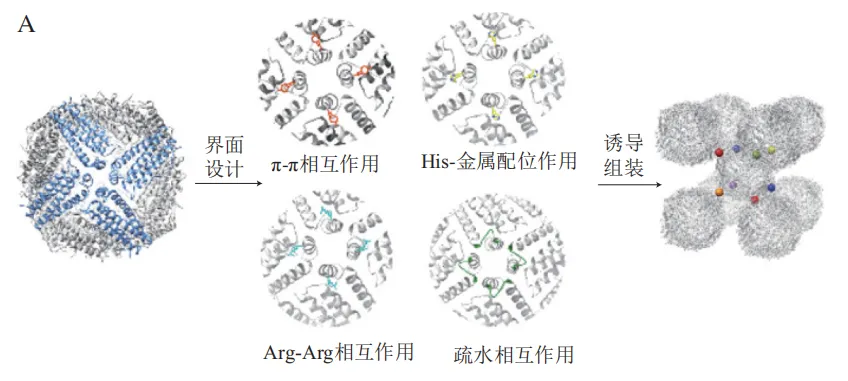
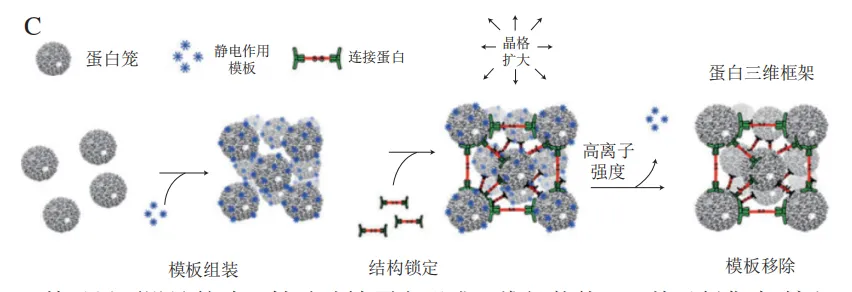
蛋白质-蛋白质三维组装体可以通过设计蛋白质间作用力而形成晶格。如图5A所示,本研究团队以铁蛋白为模板,基于关键界面重新设计策略对铁蛋白四重轴通道处进行改造,在四重轴通道界面引入酪氨酸、精氨酸和β-淀粉样蛋白的“GLMVG”基序,分别以π-π相互作用、金属配位作用、精氨酸-精氨酸相互作用和疏水相互作用成功构建了三维铁蛋白超分子结构。利用组氨酸对Ni2+的响应特性,Ni2+可诱导四重轴突变为组氨酸的铁蛋白形成三维组装体,该蛋白突变体的组装和解聚过程可由Ni2+和乙二胺四乙酸(EDTA)实现可逆调控。此外,静电相互作用也被用于诱导铁蛋白-铁蛋白间相互作用。Mikkilä等利用阳离子络合物构建了三维面心立方堆积的铁蛋白超分子材料,此结构可以发射荧光并产生单线态氧,在作为水处理剂或光催化方面具有重要意义。
 | 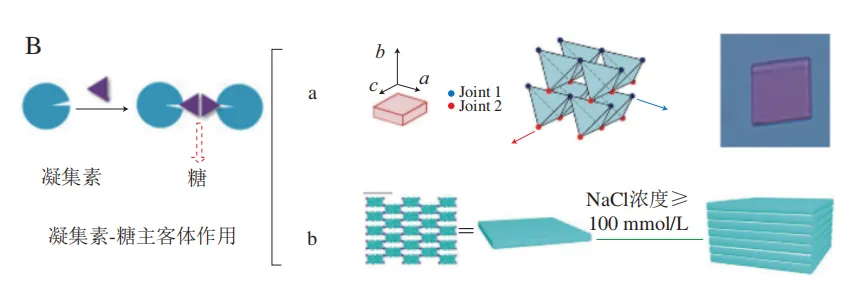 |  |

主客体作用在蛋白三维组装形成的过程中也发挥着重要的作用。Sakai等以刀豆球蛋白A作为构建单元,利用凝集素-糖相互作用和π-π堆积作用,在加入小分子配体RhB3Man后,通过调控溶液条件可形成微米级的正方形片状晶体(图5B-a)。此外,在后续研究中该研究团队以来自铜绿假单胞菌的凝集素A为自组装单元,通过引入合成的半乳糖-罗丹明B复合物,调控NaCl浓度至100 mmol/L以上时蛋白质形成了三维层状结构,这可能是由于蛋白质通过凝集素和糖之间的分子识别以及相邻配体之间罗丹明B的π-π相互作用堆积而形成(图5B-b)。
除了同种蛋白间的相互作用,不同蛋白间也可以设计蛋白质-蛋白质相互作用形成三维组装体。Liljeström等将2 种带相反电荷的蛋白通过静电相互作用形成了共组装,豇豆褪绿斑驳病毒(CCMV)颗粒是直径为28 nm的二十面体笼状蛋白,等电点为3.8,而亲和素等电点约为10.5,亲和素的大小和电荷协同作用促进了其与CCMV笼共组装形成二元三维晶格。如图5C所示,Mccoy等以同源三聚体衣壳装饰蛋白(Dec)通过位点特异性结合病毒衣壳P22(二十面体笼状蛋白),在阳离子树枝状大分子介导下Dec蛋白与P22孵育后形成三维晶格模板,且产生了有助于衣壳稳定高度交联的蛋白质材料。
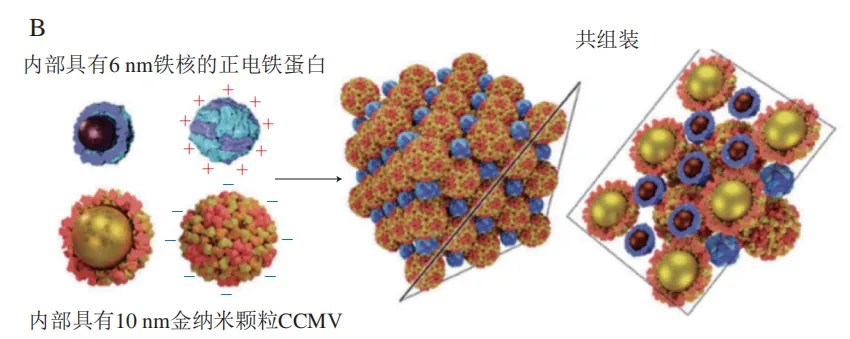
纳米颗粒与蛋白共组装已被开发为蛋白质纳米笼三维自组装的模板。Kostiainen等利用铁蛋白和CCMV形成三维二元超晶格,其中超晶格是由带正电荷的金纳米颗粒与蛋白间的静电相互作用驱动形成;金纳米颗粒和CCMV形成面心立方晶体结构,而金纳米颗粒和铁蛋白笼则形成一种交错的简单立方结构。类似地,图6A展示了基于铁蛋白笼和柱[5]芳烃的自组装成功构建具有规则晶体结构的蛋白质笼-环状分子框架,柱[5]芳烃作为分子胶水能够有效地与蛋白质笼进行电荷驱动的自组装,形成稳定的面心立方框架结构。在该研究中,铁蛋白内部空腔可进一步合成无机铁核或金属纳米颗粒,从而实现有机分子-无机纳米颗粒主客体反应。在最近的一项研究中,该团队选择了2 种尺寸和电荷不同的蛋白质笼,一种是带负电荷的CCMV,另一种是经过工程化处理后带正电荷的铁蛋白,随后将金纳米颗粒加载到CCMV空腔内、铁纳米颗粒加载到铁蛋白空腔内,成功形成了二元金属纳米颗粒超晶格;通过精确调控蛋白质笼之间的静电吸引力,成功促进了这两种蛋白质笼的自组装,形成了具有较大尺寸三维二元超晶格(图6B),其大小可达到20 μm。该研究揭示了不同蛋白质笼与纳米颗粒之间的协同作用对超晶格结构的影响,以及这些结构对纳米颗粒光学特性和磁性特性的进一步影响。
 |  | 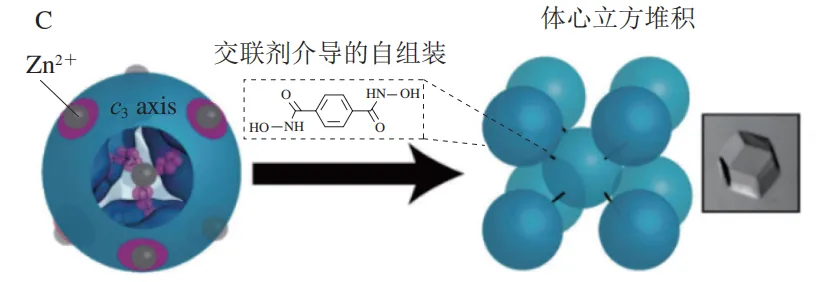 |

作为纳米材料科学的重要组成部分,金属有机框架的晶格结构由金属和有机配体通过配位作用自组装形成。Tezcan团队首次提出蛋白质-金属-有机晶体框架的概念,即利用蛋白质作为金属节点,结合有机配体作为连接,通过金属和有机配体的协调作用,构建三维有序的晶体结构。在这项研究中,铁蛋白的三重轴界面孔隙中引入了三叉形的锌配位位点,并与有机配体(含有羟肟酸官能团)配位驱动蛋白质节点之间的组装。通过调整配体与蛋白质节点之间的相互作用,成功构建了体心立方型晶体。在随后的研究中,研究人员系统地改变了铁蛋白节点上的金属离子(Zn(II)、Ni(II)、Co(II)),并与合成的不同双羟肟酸配体结合,制备了15 种不同的蛋白质-金属-有机晶体框架。该研究也表明,金属离子和配体的选择不仅影响框架的晶格结构,还会对框架的尺寸和形态产生重要影响。在对不同温度下蛋白质-金属-有机晶体框架的热力学研究中,通过调整蛋白质-金属-有机框架中的金属离子和有机配体,可以调节框架的热力学、力学以及动态响应特性。这种灵活的调节能力使得蛋白质-金属-有机框架在材料科学中具有巨大的应用潜力,特别是在开发具有可调性能的智能材料方面。
综上所述,自然界中广泛存在三维蛋白质组装体,它们作为重要的生物材料,为人工构建功能化超结构提供了灵感。三维蛋白质组装主要可分为两种策略:一是通过理性设计蛋白质界面,引入特定氨基酸或基序,利用π-π堆积、金属配位、静电、疏水及主客体识别等多种分子间作用力,构建以铁蛋白、病毒衣壳蛋白等为模块的蛋白质-蛋白质三维晶格;二是借助静电相互作用驱动蛋白质笼(如CCMV、铁蛋白)与纳米颗粒共组装,形成面心立方、简单立方等超晶格,实现有机-无机杂化材料的可控构筑。这些策略所形成的三维蛋白质材料在催化、传感、光功能和智能材料等领域展示出广阔的应用前景。

04
蛋白质多维度组装体的应用
4.1 活性物质包埋与递送
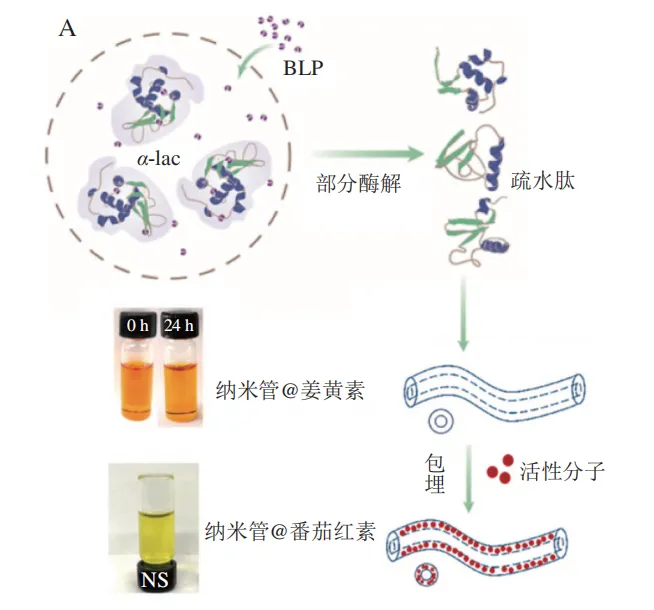
蛋白质及其组装体由于其良好的生物安全性、生物相容性和可降解性,已被广泛应用于活性物质的包埋,并递送至不同生理场景中发挥功效。相比于其他组装体,蛋白质一维纳米管作为营养物质载体具有诸多的优势:其大小、形状和刚度使其很容易被靶细胞吸收,可作为口服药物递送系统靶向黏膜被细胞摄取;纳米管的疏水空腔可以负载脂溶性化合物,例如番茄红素、姜黄素和辣椒素,以提高这些化合物的溶解度、稳定性和生物利用度(图7A)。
Bao Cheng等使用α-乳白蛋白(α-lac)肽构建了自组装纳米管,并通过疏水相互作用将脂溶性姜黄素加载到纳米管的疏水内核中,能够在葡聚糖硫酸钠诱导的结肠炎动物模型中发挥良好的抗炎功效。在食品体系中,番茄红素经过α-lac纳米管负载后大大提高了光热稳定性和抗氧化性,良好的胶体稳定性也使得经α-lac纳米管包埋的番茄红素成功应用于乳饮料中,并展现出更高的黏度和长期稳定性。共价修饰部花青素的桶形伴侣蛋白GroEL可以在疏水内核中负载超顺磁性氧化铁纳米颗粒,在加入Mg2+后蛋白之间通过配位作用组装成纳米线结构,并展现出受磁场调控的组装特性。同样以GroEL作为组装载体,Biswas等利用金属配位作用设计成蛋白纳米管结构,当ATP水解成ADP时会诱导结构的解体,由于GroEL本身可以识别不可逆变性蛋白,将药物分子连接到变性蛋白上可以使其包埋于蛋白纳米管内,通过ATP的拆解作用可以实现药物在细胞内的递送。
 | 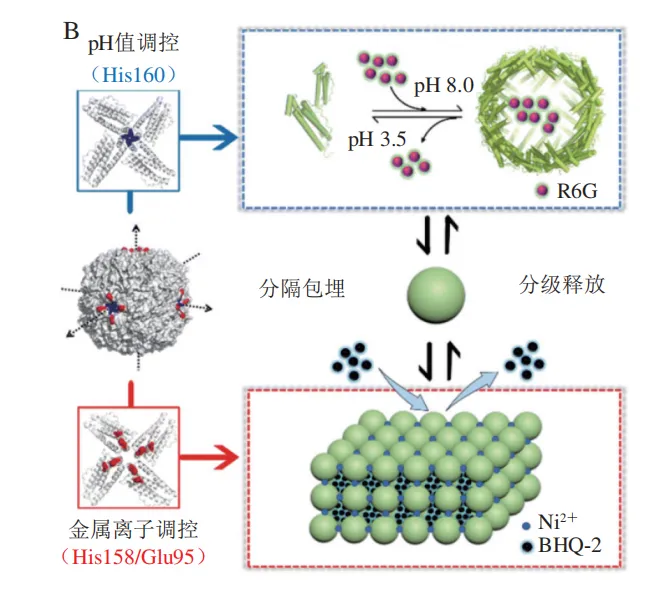 |

由于蛋白分子间在组装过程中存在着空隙,蛋白质三维组装体也可用于分级包埋活性分子物质。如图7B所示,本研究团队基于三维铁蛋白纳米笼超晶格构建了一个双室系统,铁蛋白内部空腔和外部组装间隙可分别包埋不同活性分子,其自组装行为可以通过调控pH值和金属离子实现分级释放。首先,通过调节pH值诱导铁蛋白纳米笼发生可逆自组装,从而将罗丹明6G(R6G)封装在其空腔内。其次,在Ni2+诱导下,含有R6G的铁蛋白纳米笼自组装成三维超晶格,在此过程中,另一个分子BHQ-2(R6G的淬灭剂)可以被包埋在超晶格的组装间隙内。在释放过程中,通过用EDTA及调节pH值使这2 个分子可以逐步被释放出来。
4.2 人工光捕获及光催化系统
受大自然启发,研究者们建立了诸多蛋白质-色素分子相互作用体系模拟天然光捕获系统,以更深入地了解光合作用机制并进一步对太阳能进行高效利用。目前,一维、二维、三维蛋白组装体由于其良好的结构特性已被建立为高效光捕获系统或光催化平台。
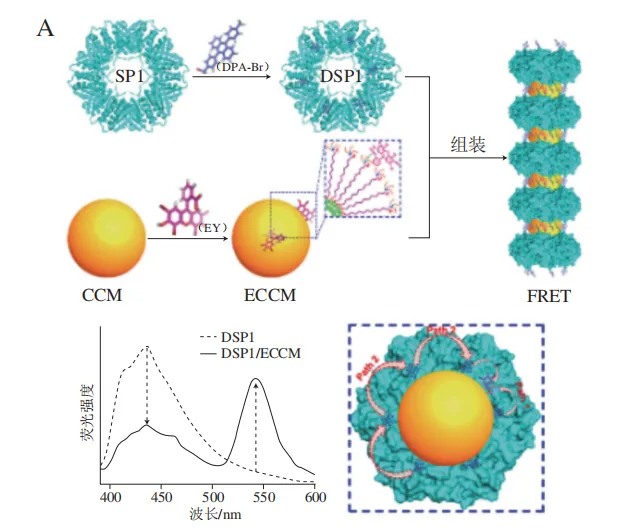
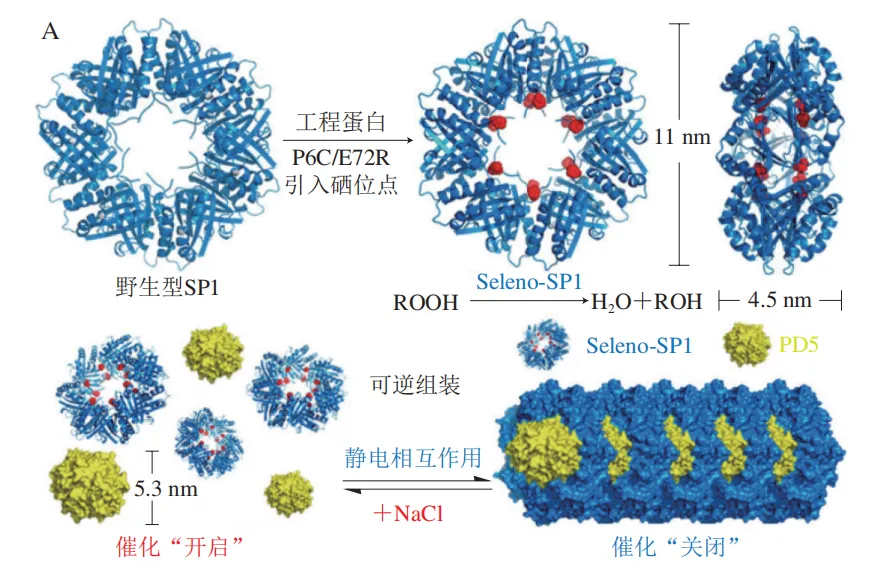
一维蛋白纳米线可以充当光捕获“天线”,仿生模拟光合细菌的能量转移过程。Sun Hongcheng等利用阳离子表面活性剂胶束诱导环状SP1蛋白在静电相互作用下自组装成纳米线(图8A),能量供体DPA-Br以共价交联的方式结合在SP1蛋白轴向表面,而能量受体EY通过静电相互作用修饰到胶束上,形成SP1-色素一维组装体后能量可以在SP1环周围的相邻供体内转移,并传递到附近的受体发色团。
 | 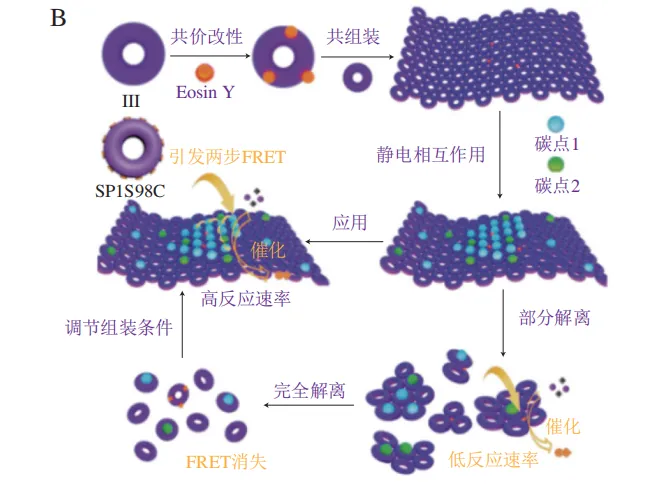 |  |

然而,一维纳米线作为光捕获系统存在能量传递的限制,能量在纳米线中的传递是单向的,一旦能量供体/受体失效,整个能量转移过程将会中断。这种单向能量传递的特性显著降低了系统的稳定性和实际应用的可行性,而二维纳米片则能显著克服这些缺点,实现稳定的能量转移。Li Xiumei等利用蓝色荧光蛋白和绿色荧光蛋白共价组装构建了一个高度有序的二维光捕获系统,通过改变诱导连接剂的长度,可以优化相邻色素之间的距离和组装体的整体尺寸,从而提高能量转移效率。Zhao Linlu等以SP1组成的二维纳米片作为光捕获平台,将2 种合成的不同尺寸量子点(QD)以静电相互作用排列在纳米片表面。该系统具有有效实现光捕获能力的能力,QD在纳米片上的有序排列表现出从多个连续供体(QD1)到相邻受体(QD2)的明显共振能量转移现象,这与植物叶绿体类囊体薄膜上捕获光能并进行能量传递的现象极其类似。在后续研究中,该团队将碳点等荧光发色团通过静电相互作用固定在蛋白质纳米片表面,不仅实现了2 种荧光发色团间的单步能量传递,还在3 个荧光发色团间构建了多步逐级能量传递人工光捕获系统(图8B)。
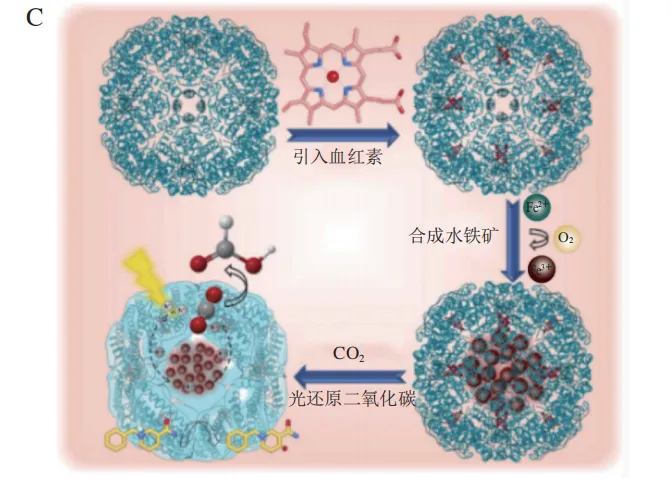
在光捕获系统的基础上,将催化剂引入蛋白质组装体可进一步对光进行催化转化,产生析氢反应或将二氧化碳还原为有机分子。在SP1二维组装的基础上,Li Yijia等在SP1的腔体内N端融合金属结合肽用于合成硫化镉QD,并进一步装载Pt纳米颗粒以实现高效的光催化H2生产。此外,来自大肠杆菌的细菌铁蛋白具有天然结合血红素的特性,利用大肠杆菌铁储藏蛋白的二重轴界面可以结合血红素的特点将其作为纳米反应器,以其自身结合的血红素作为光敏剂,内部空腔中形成的纳米铁核为光催化剂将CO2高效地转化为甲酸,同时利用关键界面设计策略构建了大肠杆菌铁储藏蛋白的三维晶体框架,提高了铁储藏蛋白作为纳米反应器的循环使用能力(图8C)。
4.3 生物催化
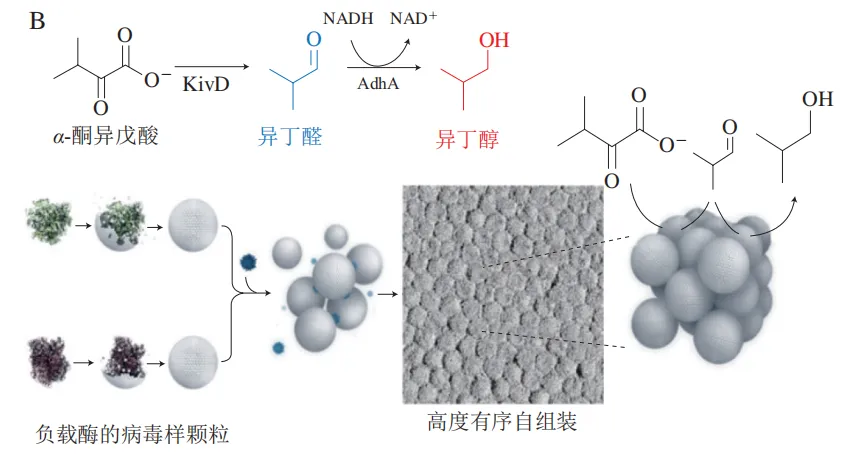
将酶进行自组装或将其封装在蛋白质组装体中是高值化利用酶的有效策略之一,可以提高其稳定性和催化效率,并赋予酶多样性的功能。Liu Junqiu团队利用烟草花叶病毒衣壳蛋白的pH值响应自组装特性,将其表面引入硒酶催化位点,从而构建出具有谷胱甘肽还原酶活性的蛋白纳米线。与其他人工硒酶相比,该组装体展现出良好的生物相容性和优异的抗氧化能力,能有效保护线粒体免受氧化损伤。该团队同样将硒酶催化位点引入SP1蛋白外表面中,并在聚酰胺树枝状分子PAMAM上修饰了锰卟啉,当PAMAM在静电相互作用下触发SP1蛋白组装成纳米线后,该蛋白纳米线同时具备谷胱甘肽还原酶以及超氧化物歧化酶活性,这种多酶协同抗氧化组装体表现出优异的生物学效应和低细胞毒性。此外,如图9A所示,在SP1内表面引入硒酶催化位点构建了一个由蛋白质组装控制的可控含硒抗氧化系统,当SP1组装为纳米线时,酶由于催化位点被隐蔽而丧失了95.5%的酶活性,而通过调控盐离子浓度促进纳米线解离后,催化位点暴露出来而使酶的活性恢复至98.7%,为构建“智能”酶提供了一种有效的方法。Gao Xin等将八聚体亮氨酸脱氢酶和二聚体甲酸脱氢酶分别与PDZ结构域及其配体融合表达,利用主客体相互作用在体外和体内实现了2 种酶的二维层状超分子组装,相比于未组装的酶表现出更高的催化效率与结构稳定性。Pan Tiezheng等通过在细胞内共结晶的方法,将外源性酶甲酸脱氢酶和有机光催化剂曙红Y同时固定在蛋白质晶体中。相比于游离的酶,固定在蛋白质晶体内的酶具备了基于级联反应的二氧化碳-甲酸盐转换能力,并展现出热稳定且可回收的特性。Douglas团队分别将2 种酶包裹在病毒衣壳蛋白当中,通过聚酰胺树枝状分子PAMAM调节蛋白表面的外部结构,将多个病毒样颗粒组装成具有面心立方晶格的有序超晶格材料(图9B);组装后的超晶格材料能够发生级联反应并协同催化作用,表现出合成异丁醇的催化活性。此外,封装β-葡萄糖苷酶的P22组装体提高了酶的局部浓度,从而提高了催化效率,包封的酶在加热、冷却和冻干后重复使用仍保持活性,进一步证明了该材料的稳定性。
 |  |


05
结 语
蛋白质组装体在生物材料领域的应用中逐渐显现出巨大的潜力。研究人员通过高度有序的蛋白质组装,设计了众多具有较好稳定性、多样性和兼容性的生物材料,包括零维纳米笼、一维纳米线/管、二维阵列和三维超晶格等。从零维单分子设计到多维度蛋白质组装体的设计和调控,不仅加深了对生物大分子结构与功能关系的理解,还推动了蛋白质作为新型材料在医学、化学和环境等领域的应用发展。在食品科学与营养领域,蛋白质自组装技术也正展现出巨大的应用潜力。通过合理设计蛋白质的多维度组装结构,可以显著改善食品功能成分的包埋、保护和递送效率。例如,基于α-乳清蛋白自组装形成的纳米管已被成功用于包埋姜黄素、番茄红素等脂溶性活性成分,不仅显著提高了这些成分的稳定性和生物利用度,还成功应用于乳饮料体系,表现出优异的胶体稳定性和长期储存性。蛋白质三维组装体形成的双室系统为实现活性成分的分级包埋和控释提供了新思路,这在功能性食品开发中具有重要意义。此外,酶-蛋白质组装体展现出的增强稳定性和催化效率,为开发新型食品酶制剂和生物催化平台提供了技术支撑。随着对蛋白质组装机制的深入理解和精准调控能力的提升,蛋白质自组装技术有望在食品质构改良、营养素递送系统、智能包装材料和食品安全检测等领域发挥更为重要的作用,为食品工业的创新发展提供新的技术路径。
然而,蛋白质组装体在一维、二维、三维结构上的发展仍面临诸多挑战。如何精确调控蛋白质自组装过程、优化结构的稳定性与可控性,以及如何实现更高效的生物医药和环境应用,依然是当前的研究重点。随着蛋白质组装技术和理解的不断深入,未来有望开发出更加高效、智能和多功能的蛋白质组装体,为生物技术、纳米技术和食品营养领域带来更为广泛的应用前景。
通信作者:

吕晨艳 教授
中国农业大学食品科学与营养工程学院
食品营养系 党支部书记
吕晨艳,中国农业大学食品学院教授/博导,食品营养系党支部书记/副主任,中国农业大学杰出人才并获青年新星A类支持,入选国家级高层次青年人才支持计划。任十四五重点研发计划指南专家组成员,中国营养学会蛋白质分会委员,北京市千人进千企产业特派员等。15 年来一直从事蛋白质资源开发利用、蛋白质载体设计与改造、营养递送及应用方面的研究工作。主持承担国家自然科学基金面上项目、青年项目、十四五重点研发计划青年科学家项目课题等10余项,在Chemical Society Reviews、Advanced Science、Chemical Engineering Journal等高水平期刊发表论文50余篇,授权发明专利7 项。
第一作者:

孙明炀 博士研究生
中国农业大学食品科学与营养工程学院
孙明炀,中国农业大学食品学院博士研究生,研究方向为蛋白质化学与营养。
引文格式:
孙明炀, 臧佳辰, 张拓, 等. 蛋白质自组装:从单分子设计到多维度超分子组装[J]. 食品科学, 2025, 46(24):321-334. DOI:10.7506/spkx1002-6630-20250710-081.
SUN Mingyang, ZANG Jiachen, ZHANG Tuo, et al. Protein self-assembly: from single-molecule design to multidimensional supramolecular assembly[J]. Food Science, 2025, 46(24):321-334. (in Chinese with English abstract) DOI:10.7506/spkx1002-6630-20250710-081.
点击下方阅读原文即可查看文章相关信息。
实习编辑:李雄;责任编辑:张睿梅。点击下方阅读原文即可查看全文。图片来源于文章原文及摄图网
近期研究热点




长按或微信扫码进行注册
为系统提升我国食品营养与安全的科技创新策源能力,加速科技成果向现实生产力转化,推动食品产业向绿色化、智能化、高端化转型升级,由北京食品科学研究院、中国食品杂志社《食品科学》杂志(EI收录)、中国食品杂志社《Food Science and Human Wellness》杂志(SCI收录)、中国食品杂志社《Journal of Future Foods》杂志(ESCI收录)主办,合肥工业大学、安徽农业大学、安徽省食品行业协会、安徽大学、合肥大学、合肥师范学院、北京工商大学、中国科技大学附属第一医院临床营养科、安徽粮食工程职业学院、安徽省农科院农产品加工研究所、安徽科技学院、皖西学院、黄山学院、滁州学院、蚌埠学院共同主办的“第六届食品科学与人类健康国际研讨会”,将于 2026年8月15-16日(8月14日全天报到)在中国 安徽 合肥召开。

长按或微信扫码进行注册
会议招商招展
联系人:杨红;电话:010-83152138;手机:13522179918(微信同号)

