 提示:欢迎点击上方「PaperRss」↑关注我们!
提示:欢迎点击上方「PaperRss」↑关注我们!

2026年3月27日,国际顶尖学术期刊《Science》在线刊登了一项由中国科研团队独立完成的里程碑式研究。这项研究由江西农业大学猪遗传改良与种质创新全国重点实验室的黄路生院士团队主导,是《Science》创刊以来,中国在猪遗传育种领域首篇以国内单位为唯一完成单位发表的长篇研究论文,标志着我国在该基础研究领域取得了历史性突破。
研究团队历经数年攻关,成功构建了全球首个哺乳动物“同一个体全身组织”单细胞/单核转录组全景图谱。他们在单一妊娠母猪及其单个胎猪个体上,于16小时内同步采集并分析了涵盖胚胎全身115个组织及母体119个组织的样本,系统鉴定了890种细胞类型及其特异性表达的转录因子。这项被国际学界视为“标志性目标”的工作,此前仅由美国联盟在单个个体17个组织上实现,此次突破极大克服了以往研究因样本来源于不同个体而带来的遗传背景“噪音”干扰。
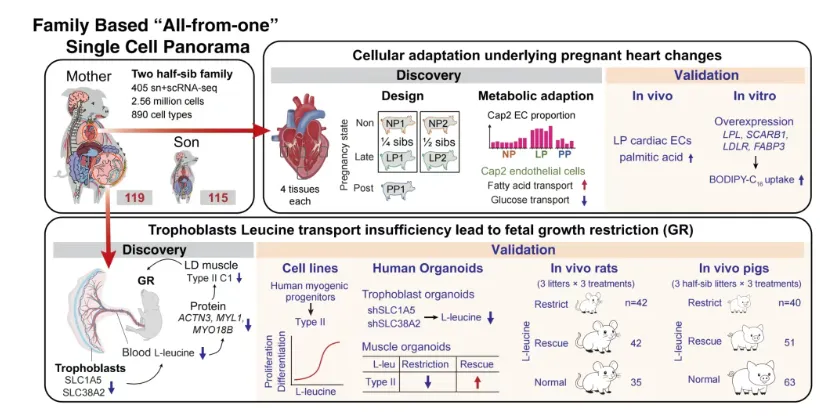
重大突破一:揭示胎儿生长受限的细胞“元凶”
在我国生猪养殖中,胎儿生长受限(FGR)发生率高达5-20%,每年导致至少3500万头仔猪发育不良,不仅造成巨大经济损失,也关乎人类类似妊娠并发症的研究。团队利用猪一胎多仔的优势,对比分析了正常与生长受限的全同胞胎猪。
研究发现,生长受限胎儿的胎盘尿囊绒毛膜中,一种名为滋养层的细胞出现了功能异常。其细胞膜上负责转运亮氨酸(一种必需氨基酸)的转运蛋白SLC1A5和SLC38A2表达显著下调,导致胎儿血液中亮氨酸浓度降低。 这种氨基酸是肌肉蛋白合成的关键“原料”。后续研究证实,亮氨酸不足会直接导致胎儿肌肉中负责高表达的II型肌纤维(TypeIIC1)比例下降,肌动蛋白和肌球蛋白合成受阻,最终致使胎儿体重减轻。该机制在人类细胞、类器官及大鼠模型中得到多途径验证,为通过遗传育种和营养调控解决生猪产业这一瓶颈问题,以及为人类临床干预胎儿生长受限提供了全新的细胞分子靶点。
重大突破二:破解妊娠期母体心脏的“能量密码”
妊娠期间,母体心脏负荷剧增,输出量需增加30-50%,其生理适应机制一直是科学盲区。团队通过对妊娠不同阶段母猪心脏的分析,首次揭示了心脏安全度过此阶段的奥秘。
研究发现,妊娠期心脏会发生可逆的生理性肥大,这由心肌细胞中的FOXO3–FBXO32保护性通路维持,它能抑制可能导致病理性心脏问题的信号。更关键的是,心脏在孕期发生了能量代谢的“战略切换”:从主要利用其他能量转为更多依赖脂肪酸供能。 研究鉴定出一种在妊娠期显著增多的特殊心脏毛细血管内皮细胞(Cap2亚群),它像“加油枪”一样,高表达LPL、FABP3等脂肪酸转运基因,功能实验证实其能显著提升心肌对脂肪酸的摄取能力。这解释了孕期心脏如何获得额外能量以支持巨大负荷。这一发现为理解人类妊娠期心脏健康、预防围产期心力衰竭提供了全新的理论依据。
深远意义:一张图谱,多重价值
这项研究构建的“全身细胞地图”价值深远。首先,它首次在同一健康个体背景下,精准绘制了1368个转录因子在全身细胞中的“工作地点图”,为解析影响猪产仔数、体长、体重等重大经济性状的基因如何通过特定细胞发挥作用提供了“导航仪”。
其次,通过跨物种比对,研究证实猪与人类在心脏、胎盘、肌肉等关键细胞类型的转录特征上高度保守。例如,人类心脏中同样存在类似的脂肪酸转运内皮细胞亚群。这强力夯实了猪作为研究人类妊娠疾病、心血管代谢疾病的理想动物模型的理论基础。
网友观点认为,这项研究不仅是基础科学的重大突破,更具有极强的现实意义。一方面,它直指我国生猪产业中胎儿生长受限这一每年造成数百亿损失的核心痛点,为从遗传根源上培育“壮仔”品种提供了精准方案。 另一方面,其揭示的妊娠期心脏适应和胎盘营养转运机制,为人类母婴健康研究打开了新窗口,是农业科学与医学交叉融合的典范。这项百分之百国产的原创成果,展现了中国科学家解决世界级科学难题的能力与决心。
- THE END -
 【免责声明】图文来自网络,版权属于原作者,如有侵权或非授权发布之嫌,请联系我们,我们将及时更正、删除。转载目的在于促进信息交流,并不代表本公众号赞同其观点或对其内容真实性负责。欢迎关注PaperRSS公众号,每天都在更新。
【免责声明】图文来自网络,版权属于原作者,如有侵权或非授权发布之嫌,请联系我们,我们将及时更正、删除。转载目的在于促进信息交流,并不代表本公众号赞同其观点或对其内容真实性负责。欢迎关注PaperRSS公众号,每天都在更新。

PaperRSS,知名教育公众号。投稿、合作、转载授权事宜请联系本号。微信ID:PaperRSS001 或邮箱:PaperRSS001@qq.com。此外,本公众号为国内实验室招聘人员、科研成果展示提供服务,欢迎垂询。