中国农业科学院赵东明、盛相鹏、步志高Nature Communications!!揭示非洲猪瘟病毒复制新机制:宿主CypA稳定衣壳蛋白的关键作用
- 2026-05-28 11:21:48
医学研究前沿——聚焦医学前沿研究进展。100多万医学领域硕博医生们订阅的微信公众号。点击标题下蓝字“医学研究前沿”关注,我们将为您提供最有价值、最前沿的医学前沿资讯。

非洲猪瘟病毒(ASFV)作为一种大型双链DNA病毒,对全球养猪业构成严重威胁,其特征是高发病率和高死亡率,目前尚无安全有效的疫苗或抗病毒药物。该病毒粒子结构复杂,由多层组成,其中主要衣壳蛋白p72占比高达病毒总质量的三分之一,在病毒组装和衣壳形成中扮演核心角色。然而,p72蛋白的稳定性调控机制长期未知,这限制了针对ASFV的防控策略开发。先前研究表明,病毒编码的分子伴侣pB602L可辅助p72正确折叠,但宿主因子是否参与p72的时序性调控仍不明确。尤其是在病毒感染后期,p72需要保持稳定以促进病毒粒子组装,而早期则需降解以释放病毒基因组,这种精细平衡提示宿主因素可能发挥关键作用。中国农业科学院赵东明、盛相鹏、步志高团队的最新研究致力于填补这一空白,旨在揭示宿主蛋白如何调控p72稳定性,从而影响ASFV复制效率。该研究不仅深化了对病毒-宿主相互作用的理解,也为开发新型抗病毒手段提供了理论基础。
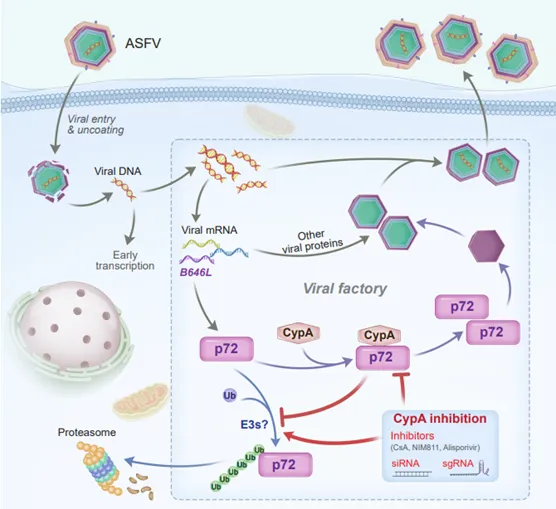
研究团队通过免疫共沉淀结合质谱分析技术,系统筛选了与p72相互作用的宿主蛋白,并鉴定出亲环蛋白A(CypA)为关键结合伴侣。CypA是一种高丰度宿主蛋白,具有脯氨酰顺反异构酶活性和分子伴侣功能,参与多种细胞过程。实验证实,CypA在体内和体外均能与p72直接结合,且利用AlphaFold3结构模拟和定点突变验证了相互作用特异性,表明CypA通过其疏水空腔结合p72的暴露区域。进一步机制研究表明,CypA结合可显著减少p72的K63位泛素化修饰,从而抑制蛋白酶体介导的降解途径,提升p72蛋白稳定性。相反,使用环孢素类CypA抑制剂或基因敲除技术破坏这一相互作用后,p72泛素化水平增加,蛋白降解加速,导致病毒复制受阻。这些发现明确了CypA在维持p72稳定性中的必要性,并通过细胞模型证明,抑制CypA会降低p72蛋白水平(不影响其转录),进而破坏病毒工厂的形成和病毒粒子组装,显著抑制ASFV复制。
本研究的机制解析显示,CypA-p72相互作用是ASFV高效复制的关键环节,为病毒生命周期提供了宿主依赖的稳定性调控模块。这一发现不仅揭示了衣壳蛋白稳定性调控的新途径,还提示靶向CypA可能成为抗ASFV的潜在策略。例如,小分子抑制剂干扰CypA-p72结合或可阻断病毒复制,为药物研发提供新方向。该研究发表于《Nature Communications》,强调了宿主因子在病毒感染中的重要作用,推动了ASFV病理机制的深入理解,对未来疫病防控具有重要参考价值。



说明:
🔹本文仅作科研人员学术交流。
🔹本文内容若存在版权问题,请联系我们及时处理。
🔹欢迎广大读者对本文进行转发宣传。
🔹《医学研究前沿》会不断提升自身水平,为读者分享更加优质的材料研究成果解读,欢迎关注我们。
欢迎广大科研工作者投稿最新研究成果。
