本文获国家自然科学基金(22378419);中国农业大学 2115 人才工程。
咖啡渣是速溶咖啡生产过程中产生的主要副产物,含有丰富的半乳甘露聚糖,利用甘露聚糖酶能够将其水解为具有多种功能活性的甘露糖和甘露寡糖,有效提高产品附加值。本研究将黑曲霉(Aspergillus niger)来源的β-甘露聚糖酶基因(AnMan26)在黑曲霉工程菌(FBL-B)中进行重组表达,表征了该酶的酶学性质,进而将其用于水解咖啡渣制备甘露糖和甘露寡糖。结果表明:重组黑曲霉经 168 h 高密度发酵后,甘露聚糖酶产酶水平达1830 U/mL。该酶的最适 pH 为 5.0,最适温度为 45 ℃,在 pH3.0~7.0 和 45 ℃ 以下保持稳定。将 AnMan26 和 α-半乳糖苷酶复配水解微波处理后的咖啡渣,水解 8 h 后咖啡渣中甘露聚糖的水解率为 42.3%,水解产物得率为20.3%,主要成分为甘露糖(44.1%)、甘露二糖(2.5%)、甘露三糖(10.9%)和甘露六糖(1.5%)。该酶具有优良的酶学性质,能够有效水解咖啡渣制备甘露糖和甘露寡糖,为咖啡渣的高值化利用提供了理论和实践基础。
作为最古老且有效的食品保鲜技术,低温贮藏在维持肌肉食品、水果和蔬菜的安全及质量方面发挥着关键作用,根据贮藏环境温度的不同,现代工业中通常以冷藏(0~4 ℃)和冷冻(低于−18 ℃)两种方式来提高产品的品质稳定性。近年来,与传统肉制品相比,调理牛排因其食用方便、营养均衡等优势,越来越受到消费者的青睐。调理牛排产品通常采用冷藏或者冷冻方式进行贮运销售。传统的冷藏技术货架期较短,难以进行长线的冷链运输;此外,尽管冷冻技术可以大幅度延长货架期,但是贮藏过程中冰晶的生长/再结晶会对肌肉组织造成剧烈的机械损伤,解冻后过多的汁液损失会直接损害行业的经济效益和消费者的健康需求。因此,有必要开发新型的低温保存技术以维持食品原有的品质。咖啡渣是速溶咖啡生产过程中产生的主要副产物,每吨咖啡豆会产生 650 公斤咖啡渣。目前,大部分咖啡渣通过填埋方式处理,造成严重的资源浪费和环境负担。咖啡渣中含有丰富的半乳甘露聚糖,含量可达 40% 以上(以干基计)。这些半乳甘露聚糖主要由通过 β-1,4 糖苷键连接的甘露聚糖主链和通过 α-1,6 糖苷键连接的半乳糖侧链组成,半乳糖侧链的取代度为 1% 左右。因此,咖啡渣是制备甘露糖和甘露寡糖的优良原料之一。将咖啡渣中的半乳甘露聚糖转化为高附加值的甘露糖和甘露寡糖一直是食品领域研究热点之一。β-甘露聚糖酶是一种可以水解甘露聚糖主链中β-1,4 糖苷键的糖苷水解酶,是降解甘露聚糖制备甘露糖和甘露寡糖过程中最重要的酶。甘露聚糖酶广泛存在于植物、动物和微生物中,其中微生物是 β-甘露聚糖酶的最主要来源。在芽孢杆菌属(Bacillus)、双歧杆菌属(Bifidobacterium)、脂环酸芽孢杆菌属(Alicyclobacillus)和类芽孢杆菌属(Paenibacillus)等细菌和青霉属(Penicillium)、毛壳菌属(Penicillium)、曲霉属(Aspergillus)等真菌中均发现 β-甘露聚糖酶存在。利用 β-甘露聚糖酶水解富含甘露聚糖的底物生产甘露糖和甘露寡糖已成为 β-甘露聚糖酶的一个重要应用领域。与物理和化学降解方法相比,酶法降解更加绿色环保,作用条件更温和,操作更方便。目前,已有一些研究利用 β-甘露聚糖酶水解甘露聚糖底物制备甘露糖和甘露寡糖。例如,米曲霉(A. oryzae)来源的 β-甘露聚糖酶可以水解槐豆胶产生甘露糖、甘露三糖和聚合度(degree of polymerization,DP)更高的甘露寡糖;枯草芽孢杆菌(B. subtilis)来源的 β-甘露聚糖酶酶解角豆胶可以产生 DP 2~5 的甘露寡糖。但是,利用β-甘露聚糖酶水解咖啡渣制备甘露糖和甘露寡糖的研究相对较少。因此,发掘一种能够有效水解咖啡渣的 β-甘露聚糖酶,对咖啡渣的高值化利用至关重要。黑曲霉具有分泌蛋白能力强和培养简单的优点,是重要的蛋白质表达系统之一。美国食品药品监督管理局将其列为公认安全的(Generally Regarded As Safe,GRAS)菌种,可用于表达多种食品酶制剂。目前,利用黑曲霉表达系统表达甘露聚糖酶的研究很少,且表达水平较低,难以满足甘露聚糖酶的工业应用需求。例如,葡萄穗霉(Stachybotrys chartarum)来源的两种 β-甘露聚糖酶在黑曲霉中异源表达,产酶水平分别仅为 521 和 84 U/mL;棘孢曲霉(A. aculeatus)来源的 β-甘露聚糖酶(man1)在黑曲霉中表达,表达水平仅 995 U/mL。因此,实现β-甘露聚糖酶在黑曲霉表达系统中高效表达具有重要意义。在前期研究中,发现黑曲霉来源的甘露聚糖酶AnMan26 具有优良的水解特性,能够水解多种甘露聚糖底物(槐豆胶、香豆胶等)制备甘露寡糖。因此,本研究以该酶为研究对象,将其导入黑曲霉工程菌 FBL-B 中进行高效表达,进而研究了该酶的酶学性质,并与 α-半乳糖苷酶复配水解咖啡渣制备甘露糖和甘露寡糖,以期为咖啡渣高值化利用提供理论依据。2.1 β-甘露聚糖酶(AnMan26)在黑曲霉中高效表达
以重组质粒 pPIC9K-AnMan26 为模板,PCR 扩增目的基因,得到长度为 954 bp 的目的片段,经NotI 和 XhoI 双酶切后,与同样经过双酶切的载体Blunt-pyrG 连接,得到重组表达载体 Blunt-pyrGAnMan26。将 Blunt-pyrG-AnMan26 转化至黑曲霉工程菌 FBL-B 中,成功实现 AnMan26 的表达,随后对转化子进行筛选,选取摇瓶发酵酶活力最高(630 U/mL)的转化子在 5 L 发酵罐中进行高密度发酵。随着发酵进行,发酵液中 β-甘露聚糖酶的酶活力和蛋白含量均逐渐增加。发酵 168 h 后,β-甘露聚糖酶的酶活力达 1830 U/mL,蛋白浓度达 3.44 mg/mL(图 1a)。SDS-PAGE 分析表明,发酵开始后在66 kDa 附近检测到弥散的蛋白条带,即为 β-甘露聚糖酶蛋白条带,且蛋白条带逐渐变粗(图 1b)。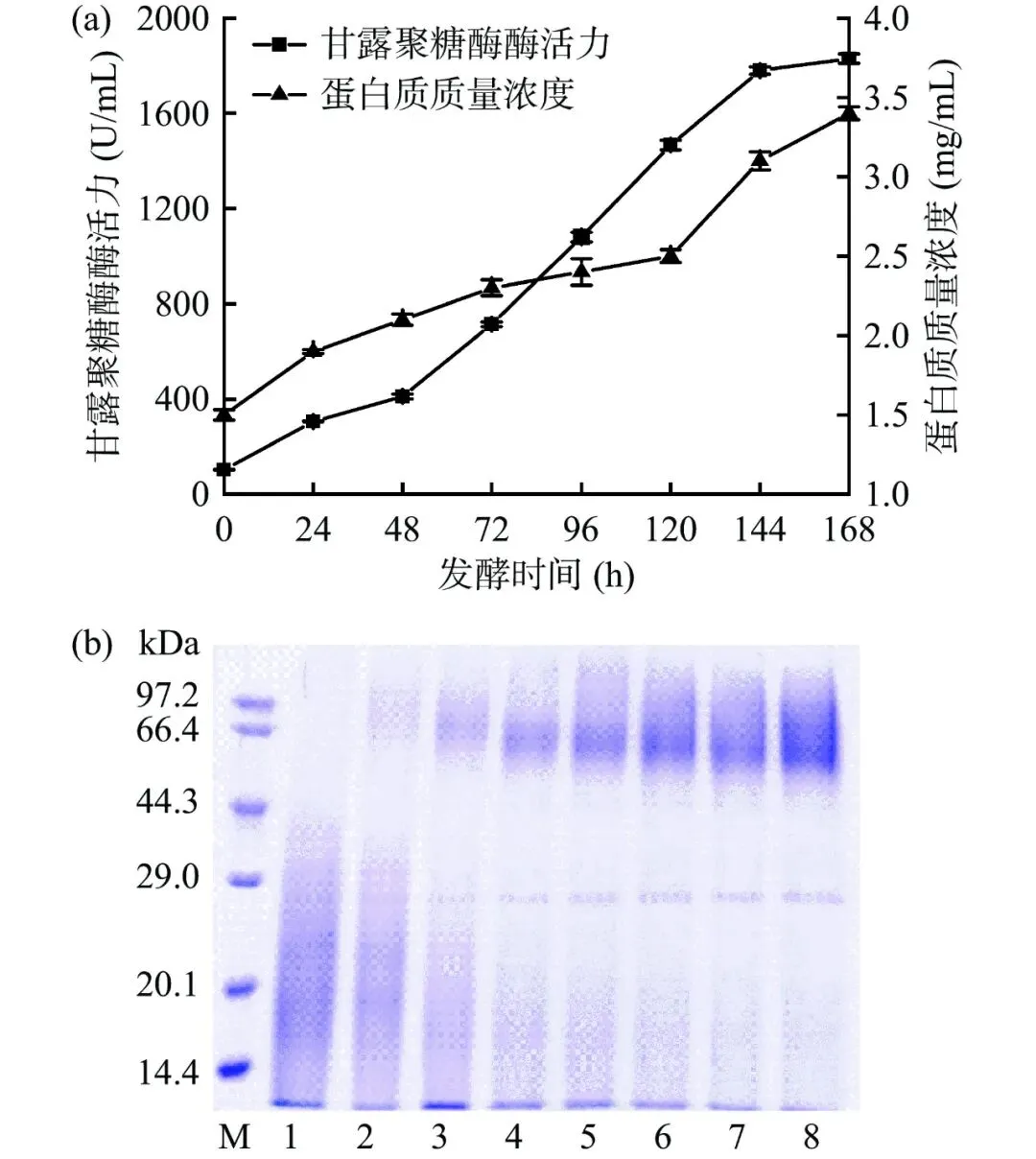
图 1 β-甘露聚糖酶(AnMan26)高密度发酵历程(a)及 SDS PAGE 分析(b)Fig.1 High density fermentation of β-mannanase (AnMan26) (a) and SDS-PAGE analysis (b)注:M:低相对分子质量标准蛋白质;泳道 1~8 分别为 0、24、48、72、96、120、144、168 h 的发酵上清液。目前仅有少数 β-甘露聚糖酶在黑曲霉中成功表达,但这些甘露聚糖酶的产酶水平较低。例如,里氏木霉(Trichodermareesei)来源的 β-甘露聚糖酶在黑曲霉中的产酶水平仅为 20 U/mL,葡萄穗霉来源的两种 β-甘露聚糖酶在黑曲霉中的产酶水平分别仅为 521 和 84 U/mL。本研究将黑曲霉来源的 β-甘露聚糖酶(AnMan26)在黑曲霉工程菌中表达后产酶水平达 1830 U/mL,明显高于其他已报道 β-甘露聚糖酶在黑曲霉中的产酶水平。粗酶液经 Q-Sepharose 阴离子交换层析一步纯化得到电泳级纯酶,纯化倍数为 1.4,纯酶比酶活力 218.5±23.8 U/mg,回收率 32.6%(表 1)。经 SDSPAGE 分析,该酶在 66 kDa 附近呈弥散条带(图 2),可能是该酶在黑曲霉表达过程中出现糖基化修饰所导致。经去糖基化酶 PNGase-F 处理后,弥散条带变为单一条带,分子量为 40 kDa,与预测的分子量一致。用 NetNGlyc 1.0 Server 软件在线分析 β-甘露聚糖酶 AnMan26 中的 N-糖基化修饰位点。发现AnMan26 存在 4 个天然 N-糖基化位点,分别是Asn3-Gln4-Thr5、 Asn124-Val125-Ser126、 Asn134-Gly135-Thr136、Asn305-Asp306-Thr307,其中第 305 位的 NDT 发生糖基化修饰的可能性较小,而第 3 位 NQT、第 124位 NVS 和第 134 位 NGT 发生糖基化修饰的可能性较大。在之前研究中,发现该酶在毕赤酵母表达中也发生糖基化现象。通常,真核表达的蛋白质都会有不同程度的糖基化修饰。例如,喜热梭孢壳来源的β-甘露聚糖酶 MtMan1 存在 1 个 N-糖基化位点,嗜热毛壳菌来源的 β-甘露聚糖酶 CtMan26 存在1 个 N-糖基化位点,它们在毕赤酵母中表达后分子量分别为 60 和 55 kDa,但经去糖基化酶处理后分子量均降低至 50 kDa,与预测分子量一致。Table 1 Purification of β-mannanase (AnMan26)
注:总酶活力(U)=酶液酶活力(U/mL)×酶液体积(mL);总蛋白含量(mg)=酶液蛋白浓度(mg/mL)×酶液体积(mL);比酶活力(U/mg)=总酶活力(U)/总蛋白含量(mg);纯化倍数=纯酶比酶活力(U/mg)/粗酶比酶活力(U/mg);回收率(%)=纯酶总酶活力(U)/粗酶总酶活力(U)×100。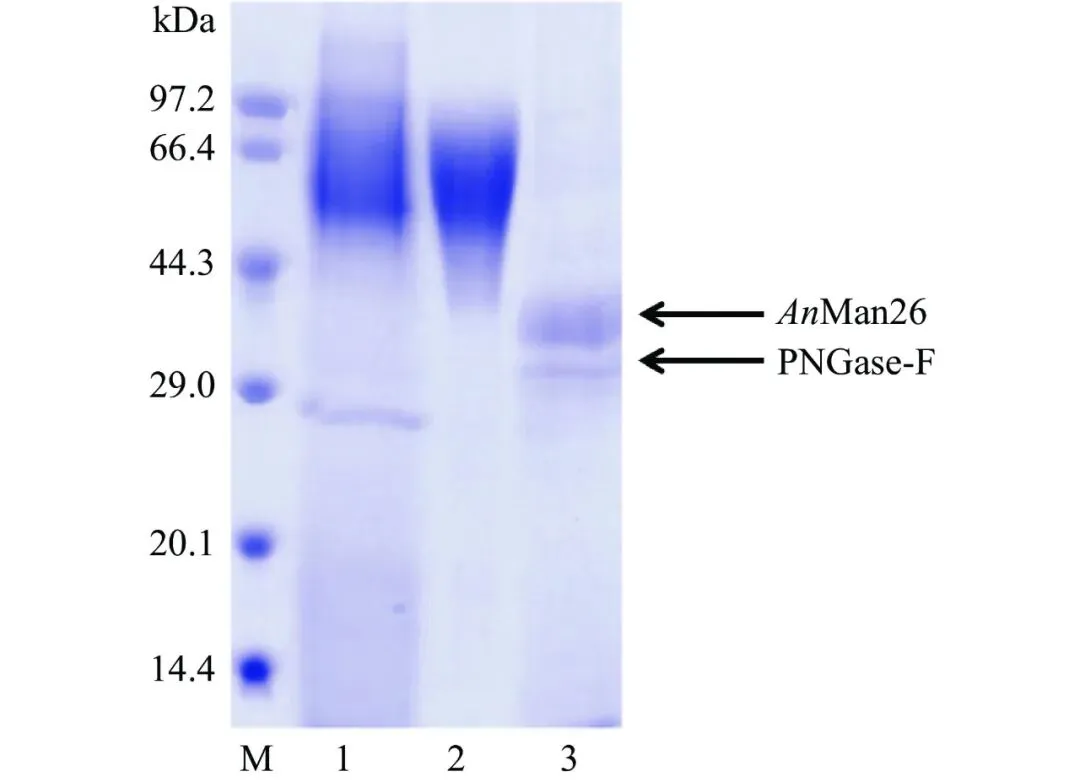
图 2 β-甘露聚糖酶(AnMan26)的纯化电泳图Fig.2 SDS-PAGE analysis of the purification of β-mannanase (AnMan26)注:M:低相对分子质量标准蛋白质;泳道 1:粗酶液;泳道 2:纯酶液;泳道 3:AnMan26 去糖基化。AnMan26 的最适 pH 为 5.0(图 3a),在 pH3.0~7.0 下具有良好的稳定性,处理 30 min 后,仍保留70% 以上的残余酶活力(图 3b)。该酶的最适温度为 45 ℃(图 3c),在 45 ℃ 以下具有良好的稳定性,处理 30 min 后仍有 80% 以上的残余酶活力(图 3d)。与在毕赤酵母中表达相比,AnMan26 在黑曲霉中的最适 pH 没有发生变化。AnMan26 能够在pH3.0 下仍保持 70% 以上的残余酶活力,说明该酶具有良好的耐酸性,明显优于枯草芽孢杆菌 YZ-21来源的 β-甘露聚糖酶 ManA(pH3.0 下残余酶活力为 15%)和多粘类芽孢杆菌(P. polymyxa)来源的 PpMan26A(pH3.0 下残余酶活力几乎为 0)。
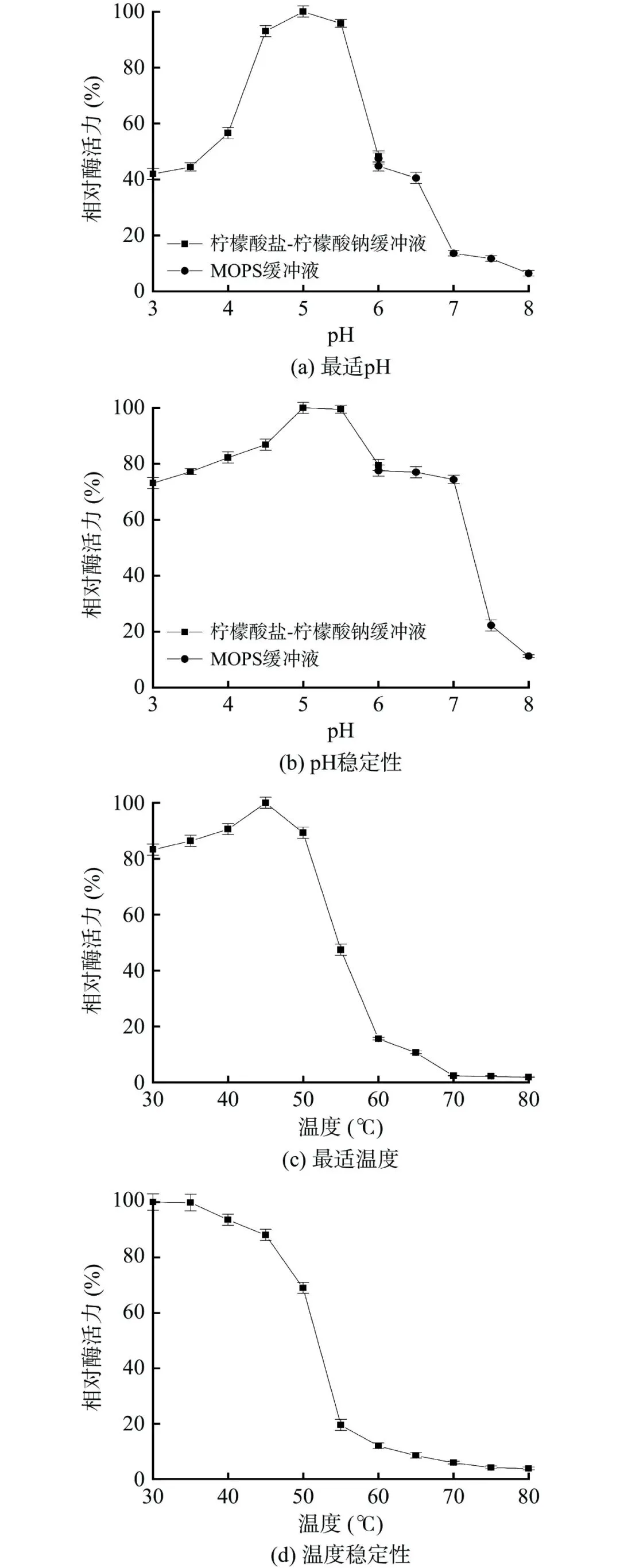
图 3 AnMan26 的最适 pH(a)及 pH 稳定性(b)、最适温度(c)及温度稳定性(d)Fig.3 AnMan26 optimum pH (a) and pH stability (b), optimal temperature (c) and temperature stability (d)为提高 β-甘露聚糖酶对咖啡渣的水解效率,对咖啡渣进行微波预处理。经单因素条件优化,预处理最佳条件为微波功率 350 W、处理时间 5 min(图 4)。在此条件下,利用 AnMan26 和 α-半乳糖苷酶复配水解咖啡渣 8 h,水解产物的得率为 20.3%,咖啡渣中半乳甘露聚糖的水解率达 42.3%。高效阴离子交换色谱分析表明,所得水解产物由甘露糖、甘露二糖、甘露三糖和少量的甘露四糖和甘露六糖组成,其中甘露糖含量为 44.1%(w/w),甘露二糖、甘露三糖、甘露四糖和甘露六糖的含量分别为 2.5%、10.9%、0.5%和 1.5%(表 2)。
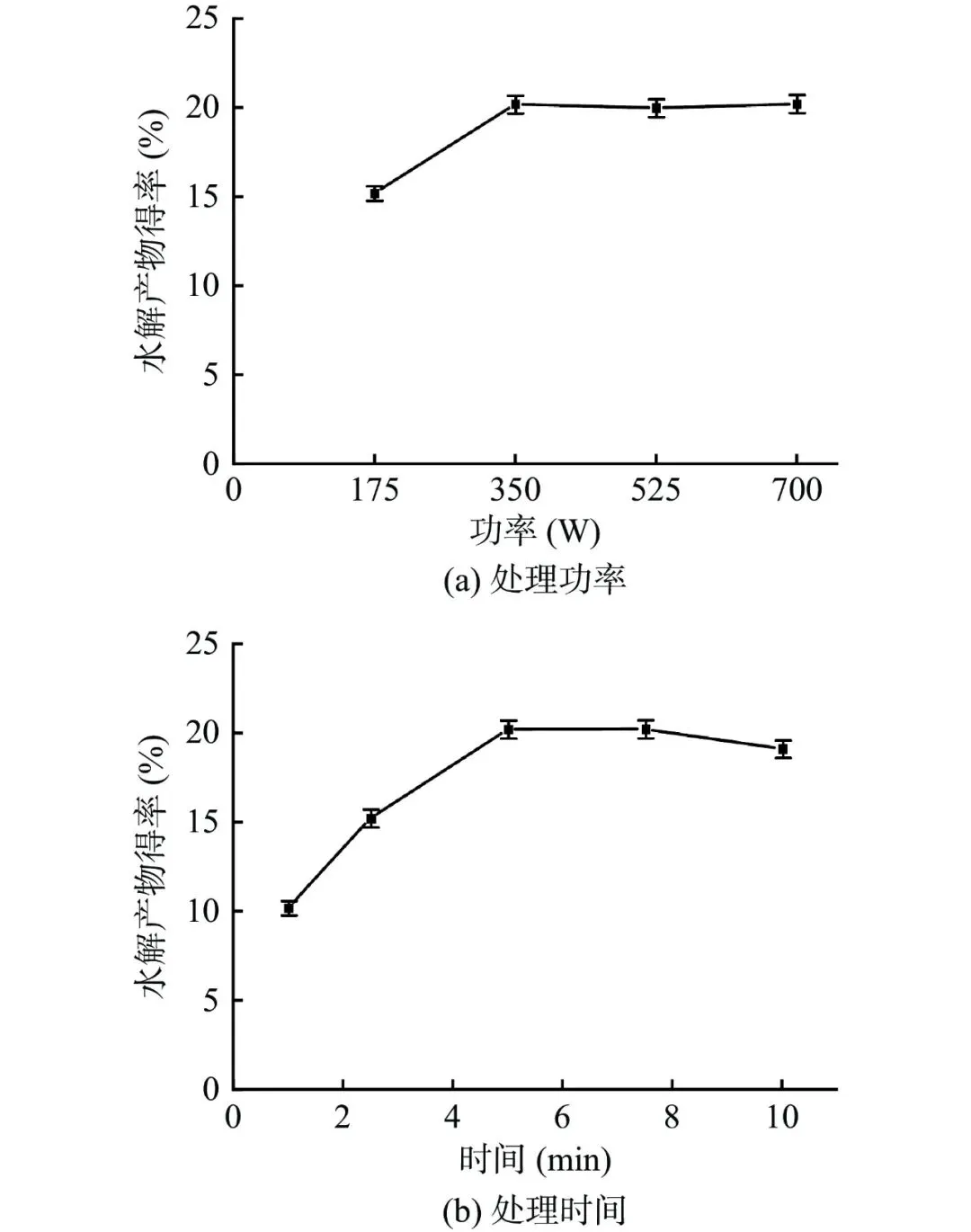
Fig.4 Effect of treatment power and time on hydrolysate yield处理功率和处理时间是微波处理效果的两大影响因素。经微波处理后的咖啡渣内部结构更松散,增加甘露聚糖酶与底物的接触面积。微波处理方法相比于蒸汽爆破等其他物理化学方法,具有装备复杂性低、能耗低的优点。在最佳微波处理条件下(350 W,5 min),咖啡渣的水解率达 42.3%,水解产物得率达 20.3%,效果优于已报道的大部分 β-甘露聚糖酶。Yoo 等利用链霉菌(Streptomycetaceae sp.)来源的 β-甘露聚糖酶 Man147 水解咖啡渣,咖啡渣中的甘露聚糖水解率仅为 18%。Chiyanzu 等用棘孢曲霉来源的 β-甘露聚糖酶和纤维素酶复配水解咖啡渣,甘露寡糖的产量为 14.64%。因此,利用微波处理咖啡渣后进行 AnMan26 和 α-半乳糖苷酶复配水解是一种有效的制备甘露糖和甘露寡糖的方法。
表 2 甘露糖和甘露寡糖(DP≤6)各组分在咖啡渣水解物中含量Table 2 Content of mannose and manno-oligosaccharides (DP≤6) in the hydrolysate of coffee grounds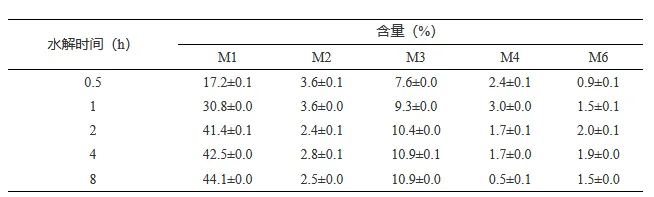
本研究利用黑曲霉工程菌 FBL-B 成功表达黑曲霉来源 β-甘露聚糖酶 AnMan26,经高密度发酵,产酶水平达 1830 U/mL。该酶具有优异的耐酸性(pH3.0 下仍保持 70% 以上活性)和良好的热稳定性(45 ℃ 以下稳定),在食品、饲料等领域具有很好的应用潜力。进一步采用微波预处理(350 W,5 min)结合 AnMan26 与 α-半乳糖苷酶复配水解工艺,咖啡渣水解率达 42.3%,产物得率达 20.3%。AnMan26可以将农业副产物咖啡渣转化为具有多种功能活性的甘露糖和甘露寡糖产品,在咖啡渣高值化利用等方面具有良好的应用前景。引用本文:姚琪,孙丹阳,闫巧娟,等. 黑曲霉β-甘露聚糖酶的高效重组表达、表征及在水解咖啡渣中的应用[J]. 食品工业科技,2026,47(3):156−162. doi: 10.13386/j.issn1002-0306.2024120221.
Citation:YAO Qi, SUN Danyang, YAN Qiaojuan, et al. Efficient Recombinant Expression and Characterization of β-Mannanase from Aspergillus niger and Its Application in the Hydrolysis of Coffee Grounds[J]. Science and Technology of Food Industry, 2026, 47(3): 156−162. (in Chinese with English abstract). doi: 10.13386/j.issn1002-0306.2024120221.
李延啸,男,2018年6月毕业于中国农业大学工学院,获工学博士学位。2020年作为优秀人才引进中国农业大学工学院农业工程系,任副教授。主要研究方向为农产品生物加工,主要包括:①农产品加工相关酶的发掘与表达。②酶的分子改造与高效生产。③农产品及其加工副产物的资源化、高值化加工。④功能性低聚糖、膳食纤维生产与应用。近年来,在甘露聚糖酶、甘露糖异构酶、淀粉酶、甘露糖苷酶等酶的克隆表达、分子改造、高效生产与应用等方面展开了深入研究。在Food Chemistry、Bioresource Technology、Biotechnology for Biofuels等期刊上发表SCI论文13篇,授权发明专利6项。主持国家自然科学基金青年科学基金项目1项,主持“十三五”国家重点研发计划“医药与食品工业酶创制与催化”项目子课题1项,主持中国博士后科学基金面上项目1项,参与国家自然科学基金项目6项。荣获2018年国家科学技术进步奖二等奖1项(第6完成人),2017年中国轻工业联合会科学技术进步奖一等奖1项(第5完成人)。
或登录www.spgykj.com阅览全文。
群聊:食品工业科技作者群
我刊正式组建微信作者群,为作者提供更多的学术与论文资讯,如需进群,请联系刘老师(微信:上方二维码,电话:87244117-8062)。
《食品工业科技》具有以上论文在全世界范围内的复制权、发行权、翻译权、汇编权、广播权、表演权、信息网络传播权、转许可权及以上权利的邻接权,且作者已授权期刊同论文著作权保护期。如需转载,可联系《食品工业科技》编辑部010-87244116,或直接在文末撰写转载来源。