PPB·5.7|南京农业大学徐彬教授团队揭示柳枝稷干旱诱导型启动子PvHVA1pro精准调控靶基因表达的分子机制
- 2026-06-03 04:33:27




文献标题:Characterization of drought-inducible promoter of PvHVA1 for drought-tolerant improvement in switchgrass (Panicum virgatum L.)
文献译名:柳枝稷 PvHVA1 干旱诱导型启动子的鉴定及其在柳枝稷抗旱性改良中的应用期刊名称:Plant Physiology and Biochemistry发表时间:2026 年 03 月 12 日影响因子:5.7论文一作:文武武一作单位:a 南京农业大学草业学院,中国南京卫岗 1 号,210095;b 上海交通大学农业与生物学院,中国上海,200240通讯作者:徐彬 教授通讯邮箱:binxu@njau.edu.cn项目基金:本研究由国家自然科学基金项目(编号:32201447、32441041、32271755)资助完成。研究背景
干旱胁迫严重限制了植物的生长与产量,植物界迫切需要对耐旱基因进行精确的按需调控,以在理想生长条件下的竞争优势与干旱威胁下的生存之间取得平衡。柳枝稷(Panicum virgatum L.)作为一种重要的生物能源和饲料作物,为了在边际土地上获得高生物量而不占用耕地,必须在提高耐旱性和维持高生物量之间实现平衡。目前,已有包括PvPIP2;9、OsDST-SRDX和SHN3等在内的多个耐旱基因被克隆并应用于提升柳枝稷的耐旱性能。
启动子通过招募转录因子来响应环境信号,在基因表达调控中发挥关键作用。组成型启动子驱动的胁迫响应基因过表达虽然能提高植物抗性,但常因能量过度消耗而导致植株矮小、产量下降等不利表型;相比之下,诱导型启动子(如受干旱诱导的晚期胚胎发生丰富蛋白基因HVA1的启动子)仅在特定胁迫下激活基因表达,能在不阻碍正常生长的前提下提升抗性。然而,尽管柳枝稷的转基因研究日益增多,其遗传改良仍主要依赖组成型启动子,至今尚未有原生的干旱诱导型启动子在该物种中得到功能性表征与验证,HVA1等基因的天然启动子在柳枝稷中的活性及应用潜力仍处于研究空白。
实现柳枝稷耐旱性精确工程的核心挑战在于缺乏经过验证的、可灵活部署的诱导型调控元件。对柳枝稷原生干旱诱导型启动子PvHVA1pro进行鉴定与功能验证,跳出单一顺式元件分子机制的局限,重点表征其在驱动干旱响应基因时的诱导性、可逆性及适用性。以PvPIP2;9作为概念验证靶标,证实PvHVA1pro能够实现干旱诱导的基因表达并显著改善植物的干旱表现。这不仅确立了PvHVA1pro作为一种实用的调控工具,也为柳枝稷及其他潜在禾本科作物的转基因精确调控和基因组工程提供了宝贵的启动子资源与关键使能技术。
本研究在柳枝稷中首次鉴定并功能验证了干旱高度诱导且表达可逆的原生启动子PvHVA1pro,证实其能通过“按需”驱动靶基因(PvPIP2;9)的表达,在不产生生长抑制代价的前提下显著提高植株的耐旱性、水分利用效率并优化株型(减小叶夹角),为禾本科作物的抗逆精确工程提供了优良的底层调控工具。
研究方法
2.1 植物材料培养与胁迫处理
为探究基因表达模式及评估植物耐旱性,本研究选用柳枝稷低地生态型品系‘HR8’作为试验材料。在基因表达谱分析中,将4周龄幼苗置于人工气候室中进行水培,并分别施加聚乙二醇(PEG6000)、NaCl、脱落酸(ABA)及低温(4 °C)处理,于不同时间点取样。在转基因植株的耐旱性评估中,将温室土培生长2.5个月的转基因株系与野生型(WT)植株进行为期21天的停水干旱处理,期间持续监测土壤水势变化,并以正常水分条件作为对照,采集顶端完全展开的叶片用于后续生理指标测定。
2.2 基因克隆、载体构建与遗传转化
为验证PvHVA1pro启动子的活性及其在抗旱工程中的应用潜力,首先从柳枝稷基因组中克隆了该启动子序列(−1至−1727 bp)并进行顺式调控元件分析。随后,构建了含有报告基因的pCAMBIA1302-PvHVA1pro::GUS-polyA表达载体;同时,为进行应用验证,将已知具耐旱功能的柳枝稷水通道蛋白基因PvPIP2;9置于该启动子下游,构建了pCAMBIA1302-PvHVA1pro::PvPIP2;9-polyA载体。最终,通过根癌农杆菌(Agrobacterium tumefaciens)介导法将上述载体分别转化至柳枝稷愈伤组织中,经潮霉素筛选及PCR技术对GUS、HptⅡ等标记基因进行扩增,成功鉴定出阳性转基因株系。
2.3 生理生化指标测定与统计学分析
为全面评估启动子活性及转基因植株的生理响应,本研究采用了一系列分析方法。利用qRT-PCR技术并以PvFTSH4为内参基因,测定了不同处理下靶基因的相对表达量(基于2⁻ΔΔCt法);通过组织化学染色法及显微观察评估了GUS报告基因在不同组织的表达活性。在生理生化层面,分别采用称重法、电导率仪及渗透势仪测定了叶片相对含水量、电解质渗透率和渗透势;利用分光光度法定量了叶绿素含量;并借助便携式光合系统监测了气孔导度、光合速率、蒸腾速率及瞬时水分利用效率。所有试验数据均包含至少三次独立重复,采用SPSS软件进行单因素方差分析(ANOVA),并通过Duncan检验比较均值差异,显著性水平设定为p < 0.05。

研究结果
3.1. 不同非生物胁迫下PvHVA1的表达谱分析
序列比对:根据柳枝稷基因组序列信息对PvHVA1的全长CDS序列进行了BLAST比对分析。
表达模式:光暗周期下PvHVA1表达无显著差异,表明其不受昼夜节律调控;PEG诱导的渗透胁迫强烈诱导其表达(处理4小时达5833倍);NaCl和低温处理轻微诱导其表达;ABA处理中度诱导其表达(处理8小时达124倍)。
为探究PvHVA1对不同非生物胁迫的响应,本研究测定了柳枝稷幼苗在光暗周期及PEG、低温、NaCl和ABA处理下的转录水平。结果表明,PvHVA1的表达不受昼夜节律调控,但在渗透胁迫下表现出高度的可诱导性,同时对盐、低温和ABA处理也有不同程度的响应(Fig. 1)。
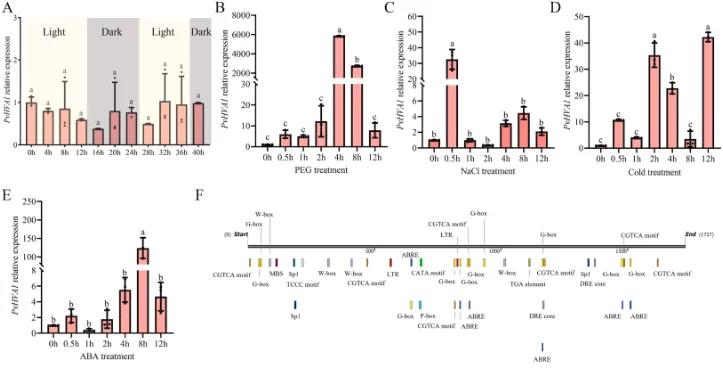
图1. PvHVA1的表达谱和启动子分析。 (A) 光暗周期下PvHVA1的相对表达量。(B-E) qRT-PCR测定PEG (B)、NaCl (C)、低温 (D) 和ABA (E) 处理下PvHVA1的相对表达量。对于每种处理,表达水平以对照(设为1)进行归一化,数据代表三个生物学重复的平均值±SE。每列上方的不同字母表示平均值之间存在显著差异(p < 0.05)。(F) PlantCARE网站预测的PvHVA1启动子中的顺式调控元件。
3.2 柳枝稷干旱诱导型PvHVA1启动子的表征
克隆与预测:从柳枝稷中分离了PvHVA1起始密码子ATG上游1727 bp的序列,并预测出39个潜在的顺式调控元件,涵盖非生物胁迫、光和激素响应元件。
活性验证:通过农杆菌介导法获得了PvHVA1pro::GUS稳定转基因柳枝稷。正常条件下未观察到GUS染色;干旱处理7天和14天后,转基因植株的根、茎、叶中出现逐渐加深的GUS染色,而恢复供水后染色消失;GUS酶活性测定结果与染色表型高度一致。
为评估PvHVA1的启动子活性,本研究克隆了其上游调控序列并进行了顺式元件分析。随后,通过构建PvHVA1pro::GUS转基因柳枝稷植株并结合GUS组织化学染色及酶活性定量测定,证实了该启动子在最适生长条件下基础表达量极低,但在干旱胁迫下被强烈诱导,且在水分恢复后具有表达可逆性(Fig. 2, Fig. 3)。
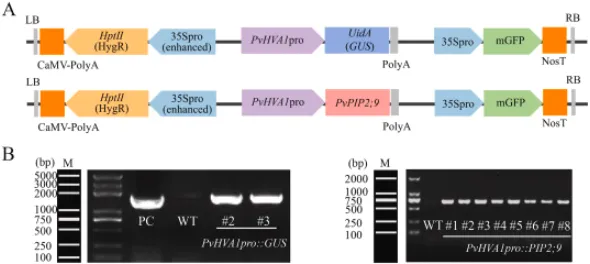
图2. PvHVA1pro::GUS和PvHVA1pro::PIP2;9转基因柳枝稷的鉴定。 (A) 转化入柳枝稷的质粒构建示意图。LB,左边界;RB,右边界;35S pro,CaMV35S启动子;PvHVA1 pro,PvHVA1启动子;HptII,潮霉素磷酸转移酶II基因;HygR,潮霉素抗性;NosT,Nos终止子。(B) PvHVA1pro::GUS和PvHVA1pro::PIP2;9转基因柳枝稷的PCR验证。M,Marker;PC,阳性对照;WT,野生型柳枝稷;#1-#8,转基因株系编号。
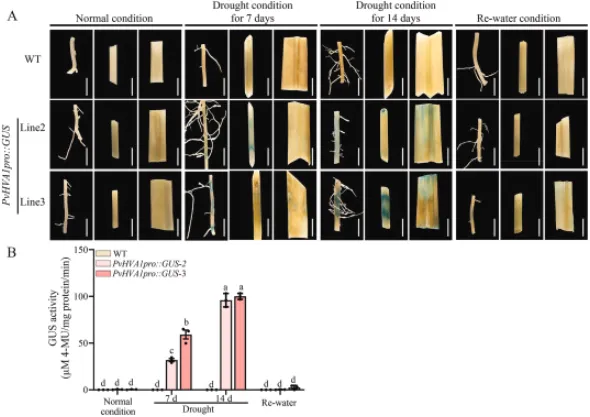
图3. 水分亏缺条件下柳枝稷中PvHVA1启动子的活性分析。 (A) PvHVA1pro::GUS转基因柳枝稷的GUS组织化学染色。取下根、茎和叶,在对照、干旱7天和14天以及水分恢复条件下,在X-gluc溶液中孵育12小时。叶绿素用70%乙醇脱色。比例尺 = 5 mm。(B) PvHVA1pro::GUS转基因柳枝稷的GUS活性。数据代表三个生物学重复的平均值±SE。每列上方的不同字母表示平均值之间存在显著差异(p < 0.05)。
3.3 由干旱诱导型PvHVA1启动子驱动的PvPIP2;9表达提高了柳枝稷的耐旱性
耐旱性评估:干旱21天后,野生型叶片严重枯萎发黄,而PvHVA1pro::PvPIP2;9转基因植株仅轻微卷曲;转基因株系维持了更高的叶片相对含水量和叶绿素含量,且渗透势和电解质渗漏率显著低于野生型。
表型观察:与组成型表达株系相比,诱导型表达株系在复水后恢复更好。此外,转基因植株表现出更小的叶夹角(10°至13°)和更直立的叶片表型,且干旱下叶夹角/叶鞘区域的GUS染色主要集中在茎秆中。
为评估PvHVA1启动子在水分亏缺条件下的应用潜力,本研究利用其驱动水通道蛋白基因PvPIP2;9在柳枝稷中表达。结果表明,干旱诱导的PvPIP2;9表达显著改善了植株的生理状态并提高了耐旱性,且在复水后展现出优于组成型表达的恢复能力。同时,该靶向表达模式还导致了转基因植株叶夹角减小的直立表型特征(Fig. 4, Fig. 5)。
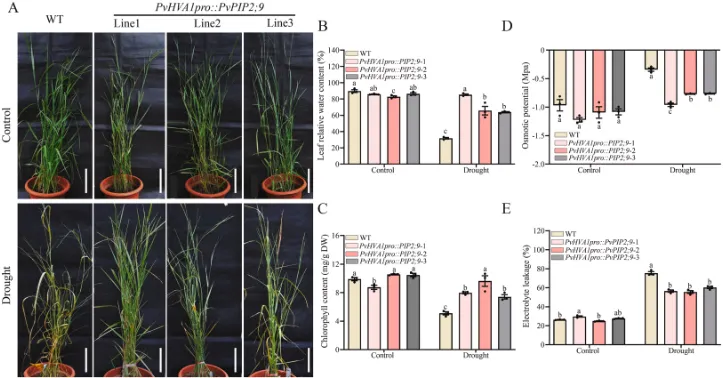
图4. 在PvHVA1启动子控制下表达PvPIP2;9提高了柳枝稷在水分亏缺胁迫下的耐旱性。 (A) PvHVA1pro::PIP2;9转基因柳枝稷和WT植株分别在对照和干旱处理下的表型。2.5个月大的柳枝稷在水分充足和停止浇水21天的条件下生长。比例尺 = 10 cm。(B) 叶片相对含水量。(C) 叶片叶绿素含量。(D) 叶片渗透势。(E) 叶片电解质渗漏。数据代表三个生物学重复的平均值±SE。每列上方的不同字母表示平均值之间存在显著差异(p < 0.05)。
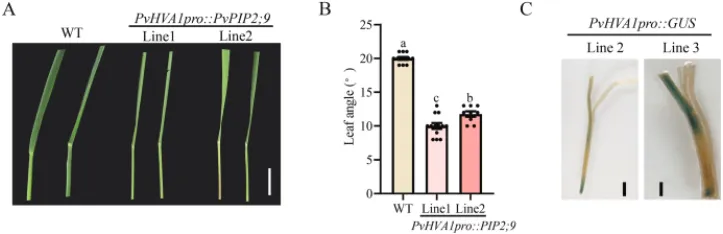
图5. 在PvHVA1启动子控制下表达PvPIP2;9减小了柳枝稷的叶夹角。 (A) 转基因和WT植株的叶夹角表型。比例尺 = 1 cm。(B) PvHVA1pro::PIP2;9转基因和WT植株的叶夹角。数据代表至少九个重复的平均值±SE。每列上方的不同字母表示平均值之间存在显著差异(p < 0.05)。(C) 干旱条件下PvHVA1pro::GUS转基因柳枝稷叶夹角/叶鞘区域的GUS组织化学染色。比例尺 = 3 mm。
3.4 PvHVA1pro::PvPIP2;9的表达提高了水分亏缺条件下的光合效率和水分利用效率
光合特性:转基因与野生型株系的气孔导度无显著差异;但在对照和干旱条件下,转基因株系的光合速率均显著高于野生型。
水分利用:对照条件下转基因株系的蒸腾速率较高,干旱条件下两者相似;干旱处理后,转基因植株表现出更高的水分利用效率。
进一步研究了由PvHVA1pro驱动的PvPIP2;9干旱诱导表达对柳枝稷光合作用和水分利用效率(WUE)的影响。结果证实,该诱导表达模式不仅在正常和干旱条件下均提升了植株的光合速率,还在干旱处理后显著提高了水分利用效率,表明PvHVA1pro可作为一种有效的调控工具应用于柳枝稷耐旱性研究中靶基因的诱导表达(Fig. 6)。
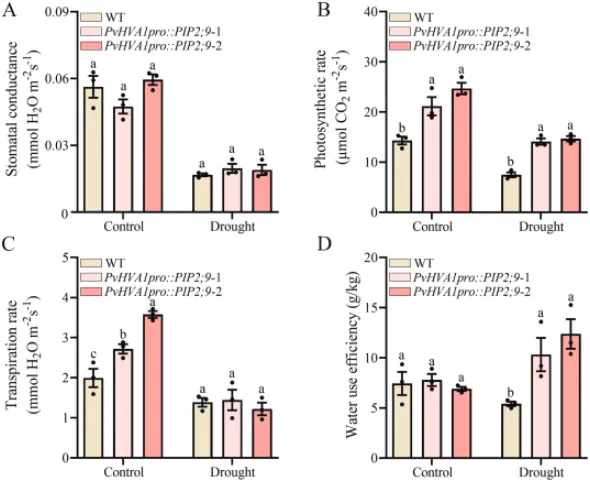
图6. PvHVA1pro::PIP2;9转基因柳枝稷的光合特性。 在对照和水分亏缺条件下测定顶部第三片叶子。(a) 气孔导度。(b) 光合速率。(c) 蒸腾速率。(d) 水分利用效率。数据代表平均值±SE (n = 3)。每列上方的不同字母表示平均值之间存在显著差异(p < 0.05)。
研究创新性
1. 首次在柳枝稷中鉴定并功能验证了原生的干旱诱导型启动子。尽管此前在柳枝稷(一种重要的生物能源和饲料作物)中进行了广泛的转基因研究,但其抗逆遗传改良大多依赖于组成型启动子(如Ubiquitin或CaMV35S)。组成型启动子虽然能提高抗性,但往往会导致正常生长条件下的能量浪费和生长抑制。本研究首次在柳枝稷中克隆、表征并功能验证了干旱诱导型启动子PvHVA1pro,填补了该物种在精确基因调控元件方面的研究空白。
2. 挖掘出具有“低基础表达、高诱导性、强可逆性”的优良调控元件。研究证实,PvHVA1pro在水分充足的最适生长条件下基础表达活性极低(避免了不必要的代谢消耗),但在渗透胁迫(如PEG处理)下能被极其强烈地诱导,基因表达量急剧增加高达5833倍。更为关键的是,在干旱解除(复水)后,其启动子活性能够迅速消失。这种高度敏感且按需启动的时空表达特性,使其成为理想的精确调控工具。
3. 实现了耐旱性的精确工程,克服了组成型过表达的“生长惩罚”。本研究将PvHVA1pro作为概念验证工具,用于驱动水通道蛋白基因PvPIP2;9的表达。结果表明,这种诱导型表达策略不仅显著提高了柳枝稷的耐旱性、光合性能和水分利用效率,而且避免了明显的生长抑制代价。与组成型过表达(Ubipro::PIP2;9)相比,诱导型表达的转基因植株在胁迫解除(复水)后展现出更优异的生长恢复能力,成功实现了“正常条件下保障生长,干旱威胁下集中资源求生”的平衡。
4. 揭示了靶向诱导表达对植物株型(叶夹角)的积极改良作用。研究意外发现,由PvHVA1pro驱动PvPIP2;9表达的转基因植株表现出叶夹角显著减小(从约20°减小至10°~13°)、叶片更加直立的表型特征。这种形态学上的改变(株型结构的优化)可能影响了空气水分沉积并有助于减少水分蒸腾,从而进一步从形态发育层面提升了植物在水分亏缺条件下的适应性。
5. 为禾本科作物的分子育种提供了关键的“使能技术(Enabling Technology)”。本研究没有局限于单个顺式元件分子机制的探讨,而是致力于将PvHVA1pro确立为一种可实际部署的调控工具。该启动子的成功应用,为柳枝稷及其他潜在禾本科作物(尤其是需要在边际土地上平衡高生物量与高抗逆性的作物)的抗逆基因精确表达、功能基因组学研究以及基因组编辑,提供了宝贵的底层调控资源和技术支撑。

审核|林蘖亙
阅读科研文献,荟萃前沿进展
欢迎关注、转发、投稿、点赞
