JIPB|中国农业大学研究团队用Y1H技术揭示OsSPL10的变异通过直接调节水稻中OsNAC2的表达和ROS的产生来赋予耐旱性
干旱是制约水稻(Oryza sativaL.)生产的主要因素。鉴定干旱胁迫相关基因的自然变异是开发遗传改良水稻品种的重要一步。在这里,我们将鳞状启动子结合蛋白样 (SPL) 家族的成员 OsSPL10 作为参与调节水稻耐旱性的转录因子。OsSPL10通过控制 ROS 产生和气孔运动在耐旱性中发挥重要作用。2022年9月,中国农业大学研究团队在JIPB上发表了题为“Variations in OsSPL10 confer drought tolerance by directly regulating OsNAC2 expression and ROS production in rice”的研究论文,揭示OsSPL10的变异通过直接调节水稻中OsNAC2的表达和ROS的产生来赋予耐旱性。
OsSPL10的单倍型和等位基因频率分析表明,大多数旱稻和改良的低地稻品种都含有OsSPL10 Hap1等位基因,而OsSPL10 Hap2 等位基因主要存在于低地和地方稻品种中。重要的是,我们证明了具有OsSPL10 Hap1等位基因的品种表现出低表达水平的OsSPL10及其下游基因OsNAC2,这会降低 OsAP37 的表达并增加OsCOX11的表达,从而防止 ROS 积累和 PCD。此外,OsSPL10的敲低或敲除可诱导气孔快速关闭并防止水分流失,从而提高水稻的耐旱性。基于这些观察,我们提出OsSPL10 通过调节OsNAC2表达来赋予耐旱性,并且OsSPL10 Hap1 可能是水稻耐旱性遗传改良的有价值的单倍型。我们进行了酵母单杂交(Y1H)试验,以评估OsSPL10与候选靶基因启动子的潜在结合。我们观察到OsSPL10仅与OsNAC2启动子结合;OsbZIP23和OsMADS26启动子即使在不存在OsSPL10的情况下也具有活性,表明酵母蛋白的转录激活(图4A,S5A)。RT-qPCR分析表明,在正常和干旱胁迫条件下,OsNAC2表达水平与OsSPL10转基因系中的OsSPL10表达水平一致(图4B)。SPL通过识别5′-GTAC-3′序列来调节其下游靶基因的转录。值得注意的是,我们在OsNAC2的2kb启动子中鉴定了15个结合基序(图4C,E)。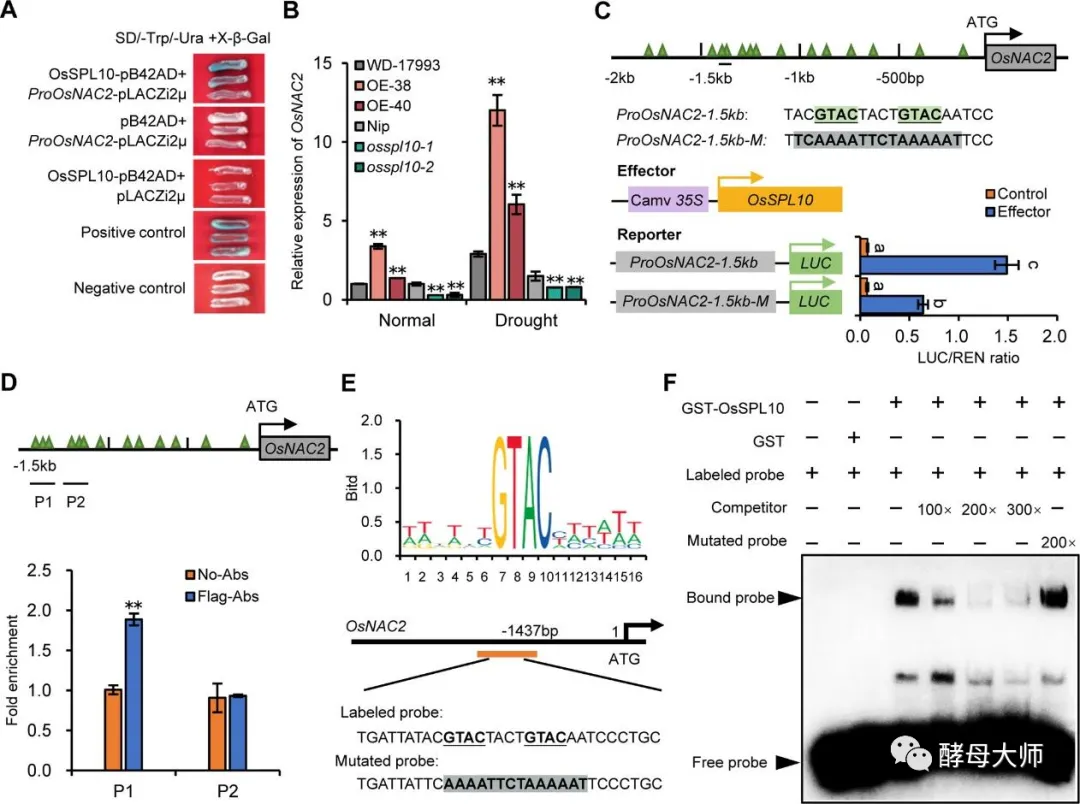
为了确定OsSPL10是否在体内直接与OsNAC2启动子结合,我们对Pro35S:3×FLAG-OsSPL10幼苗进行了ChIP-qPCR检测。我们检测到特定片段的显著富集,染色质用抗FLAG抗体(FLAG Abs)沉淀(图4D)。在体外检测OsSPL10是否特异性结合OsNAC2启动子的GTAC基序,我们进行了电泳迁移率转移使用带有两个GTAC基序的标记探针进行分析(EMSA)OsNAC2启动子(图4E)。我们确定重组OsSPL10-GST(谷胱甘肽S-转移酶)可以与标记的探针,而不是突变的探针(图4E,F)。这些结果提示OsSPL10通过与GTAC结合是一种直接的正调节因子OsNAC2启动子区的基序。总之,OsSPL10似乎通过控制ROS的产生和气孔运动在抗旱性中发挥了重要作用。在干旱胁迫下,具有OsSPL10
Hap1等位基因的品种显示OsSPL10及其下游基因OsNAC2的低表达水平,这降低了OsAP37的表达并增加了OsCOX11的表达,从而防止ROS积累和PCD。相反,OsSPL10的敲除或敲除诱导气孔快速关闭并防止水分流失,从而提高水稻的耐旱性(图7)。相反,在含有OsSPL10 Hap2等位基因的品种中,OsSPL10的高表达促进了OsNAC2的表达,导致ROS积累和PCD,这伴随着气孔缓慢关闭的促进,从而导致水稻对干旱胁迫的更大敏感性。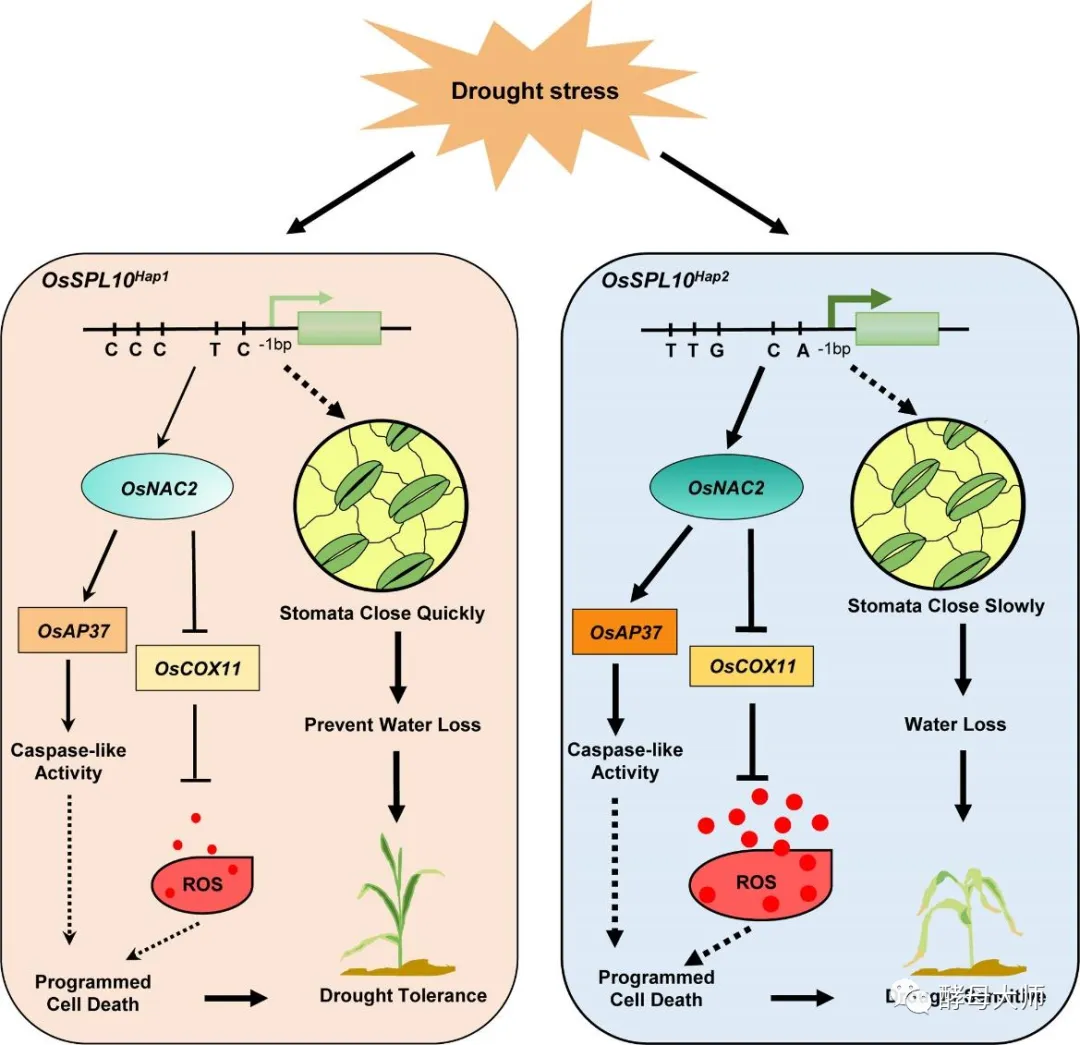
图7.OsSPL10在抗旱性中的作用模型