(一)HvTrh的序列特征与时空表达模式
HvTrh 具有典型的bHLH-PAS结构域,且在鞘翅目昆虫中高度保守。表达分析显示,HvTrh 在蛹期的表达量最高,且在幼虫中肠中的表达显著高于表皮、脂肪体和马氏管。
(二)沉默HvTrh导致致命的蜕皮缺陷
实验通过对1-4龄幼虫注射dsRNA干扰 HvTrh 的表达。结果显示:
高致死率:1-4龄幼虫的死亡率分别高达 70%、70%、100% 和 90% 。
表型特征:1龄幼虫发育停止并死亡;2龄和3龄幼虫表现为蜕皮启动但无法脱去旧表皮,常出现刺分叉倒伏和体节粘连现象;4龄幼虫则无法完成化蛹过程 。
呼吸系统正常:尽管 Trh 在胚胎期负责气管发育,但幼虫期敲降 HvTrh 后,其气管形态和螺旋丝结构保持正常,说明其致死并非由呼吸受阻引起。
图 1. 沉默 HvTrh 对不同幼虫龄期的影响。(A–M):1至4龄幼虫注射 dsHvTrh 后产生的表型变化。(N–Q):1至4龄幼虫的存活率曲线 。
(三)HvTrh通过20E信号通路调控蜕皮
基因下调:沉默 HvTrh 后,20E合成基因 (Hvshd, Hvphm, Hvsad) 和信号基因 (HvEcR, HvUSP, HvE75) 显著下调,而 HvHR3 表达上调。
滴度下降:4龄幼虫血淋巴中的20E滴度明显降低。
不可挽救性:外源补充20E无法挽救 HvTrh 沉默导致的死亡或蜕皮失败,表明组织对20E信号的解读能力受损。
图 3. 沉默 HvTrh 对 20E 通路的影响。(A):20E 相关基因的表达水平。基因缩写说明:shd (shade)、phm (Phantom)、sad (shadow)、EcR (蜕皮激素受体)、USP (Ultraspiracle)、E75 (蜕皮激素诱导蛋白 75)、HR3 (激素受体 3)。(B):4龄幼虫体内的 20E 滴度。(C):外源补充 20E 后的 RNAi 效率(Rescue实验结果)。
(四)HvTrh对表皮重塑的影响
组织学观察发现,控制组幼虫经历了正常的表皮离层和新表皮沉积,而 HvTrh 敲降组完全未能脱去旧表皮,且新表皮合成失败。此外,壳多糖合成酶基因 HvCHS1 显著下调,且壳多糖沉积大幅减少。
图 4. 沉默 HvTrh 对4龄幼虫蜕皮的影响。(A):壳多糖合成酶 1 (HvCHS1) 的表达水平。(B–C):dsGFP 处理组(对照组)与 dsHvTrh 处理组4龄幼虫腹部表皮的 HE 染色观察。蓝色箭头表示新形成的表皮,EC 代表表皮细胞。(D–E):dsGFP 处理组与 dsHvTrh 处理组表皮的荧光增白剂 28 (FB28) 染色结果,用于观察壳多糖沉积。
(四)分子机制:HvTrh直接激活HvE75
通过双荧光素酶报告基因实验 (DLR) 和凝胶迁移实验 (EMSA) 证实:
HvTrh 能显著增强 HvE75 的启动子活性 。
HvTrh 蛋白通过结合 HvE75 启动子区域的一个特定 CME (ACGTG) 基序来实现转录激活作用。
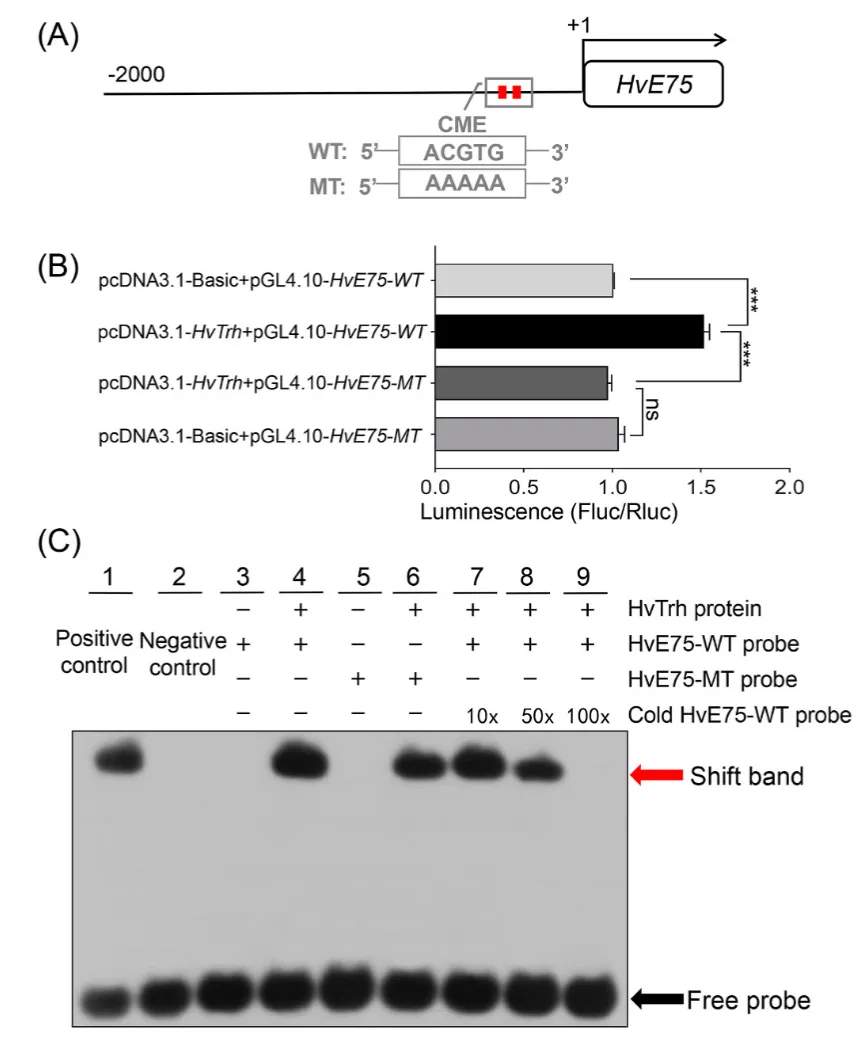
图 5. HvE75 启动子中 CME 位点的功能分析。(A):克隆的 2000-bp HvE75 启动子示意图,标示了两个推测的中枢神经系统中线元件 (CME) 位点(红色框)。(B):使用包含野生型 (HvE75-WT) 或突变型 (HvE75-MT) 的短启动子片段(约 200 bp)进行双荧光素酶报告基因 (DLR) 检测。HEK293T 细胞共转染野生型或突变型构建体,以及 HvTrh 表达质粒 (pcDNA3.1-HvTrh) 或空载体对照 (pcDNA3.1-Basic),并以 pRL-TK 质粒作为内参照。(C):电泳迁移实验 (EMSA) 显示 HvTrh 蛋白与 HvE75 探针的结合。实验条件包括:生物素标记的 HvE75-WT 和突变型 (HvE75-MT) 探针与重组 HvTrh 蛋白孵育;竞争实验中使用递增浓度(10倍、50倍、100倍摩尔过量)的未标记 HvE75-WT 探针。