2.1 植物材料、遗传转化与生长处理
本研究以紫花苜蓿(Medicago sativa)‘中苜1号’为受体材料,旨在探究MfERF053基因的功能。研究人员从黄花苜蓿(Medicago falcata)中克隆MfERF053基因,分别构建了其过表达(OE)和RNA干扰(RNAi)载体,并通过农杆菌介导的叶盘转化法获得了转基因紫花苜蓿株系,最终筛选出阳性株系用于后续实验。所有植株均在标准化的气候室条件下培养,并通过停止浇水的方式施加自然干旱胁迫处理,以模拟干旱环境。
2.2 生理表型指标测定
为评估MfERF053基因对紫花苜蓿抗旱性的影响,研究对不同株系(野生型、OE、RNAi)在正常及干旱胁迫下的生理表型进行了系统测定。测定内容涵盖了植株的水分状态(叶片失水率、相对含水量)、细胞膜损伤程度(相对电导率、MDA含量)、气孔调控(气孔密度与开度)、氧化应激响应(ROS积累、CAT与APX酶活性)以及光合性能(叶绿素含量、气体交换参数Pn、Gs等、叶绿素荧光参数Fv/Fm、NPQ)。这些多维度的指标共同构成了对植株抗旱能力的综合评价。
2.3 转录组测序分析与数据验证
为了揭示MfERF053调控紫花苜蓿抗旱性的分子机制,研究对不同处理下的各株系叶片和根系样本进行了RNA测序(RNA-seq)。通过生物信息学分析,以|log₂FC| ≥ 2和FDR < 0.05为标准筛选差异表达基因(DEGs),并利用GO和KEGG数据库对这些基因进行功能富集分析,以识别核心调控通路。为确保测序数据的准确性,研究选取了部分核心DEGs,通过qRT-PCR技术对其表达模式进行验证。所有实验数据均经过严格的统计学分析(如ANOVA),以确保结论的可靠性(显著性水平设为P < 0.05)。
3.1. 过表达MfERF053增强紫花苜蓿的抗旱性
株系构建:成功构建转基因株系。
表型差异:OE株系耐旱性显著增强。
生理指标:OE株系持水力强损伤轻。
根系发育:OE株系根系更发达。
为探究MfERF053在干旱胁迫响应中的作用,研究利用了紫花苜蓿的过表达(OE,MfERF053表达水平升高的株系)和RNA干扰(RNAi,ERF053表达被沉默的株系)株系。通过遗传转化共构建了83个OE株系和23个RNAi株系;经PCR和RT-qPCR验证,鉴定出40个阳性OE株系和16个阳性RNAi株系,其MfERF053 mRNA表达水平存在差异。自然干旱胁迫5天后,各株系间观察到明显的表型差异。具体而言,RNAi株系的叶片表现出严重的卷曲和萎蔫,野生型(WT,非转基因紫花苜蓿植株)植株表现出轻微的叶片卷曲和萎蔫,而OE株系则维持正常生长。随着干旱胁迫的加剧,RNAi株系最先死亡,其次是WT植株,而OE株系存活时间最长。至干旱胁迫第13天,RNAi株系的存活率(12.96%)显著低于OE株系(68.05%)。此外,干旱胁迫显著降低了紫花苜蓿的叶片相对含水量(RWC),OE株系的RWC(29.45%)远高于WT植株(16.15%),而WT植株的RWC又远高于RNAi株系(7.87%)。叶片相对电导率(RC)和丙二醛(MDA)含量在干旱胁迫期间均有上升:RNAi株系的RC和MDA含量(分别为22.51%,180.03 nmol g⁻¹)显著高于WT植株(分别为13.03%,133.64 nmol g⁻¹),而WT植株的这些指标又显著高于两个OE株系(OE13, OE70;分别为7.33%,103.20 nmol g⁻¹)。干旱胁迫下,OE株系受到的损伤显著小于RNAi株系,这证实了MfERF053通过增强持水能力和减轻膜脂过氧化损伤,作为紫花苜蓿抗旱性的正向调控因子发挥作用(Fig. 1)。对于根系,在正常浇水和10天干旱胁迫处理后,与RNAi株系相比,OE株系形成了更多的侧根并表现出更大的根系生物量。在干旱胁迫下,紫花苜蓿的根系RWC和生物量均急剧下降:OE株系的根系RWC和生物量(分别为11.62%,0.51 g)显著高于RNAi株系(分别为3.72%,0.21 g)。这些结果表明MfERF053促进侧根形成并提高水分吸收能力。总而言之,MfERF053是紫花苜蓿响应干旱胁迫的正向调控因子(Fig. 2)。
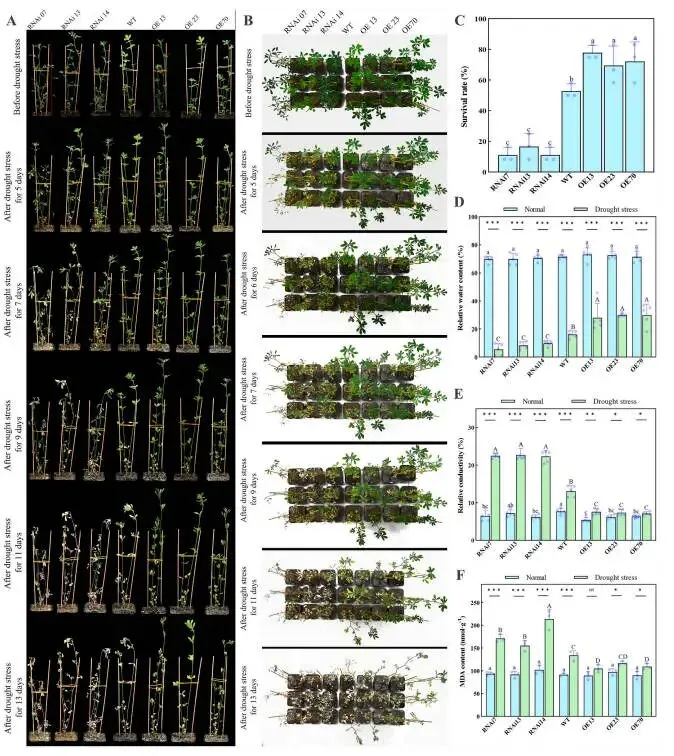
图1. 过表达MfERF053增强紫花苜蓿的干旱响应。 (A, B) RNAi、WT和OE紫花苜蓿株系在自然干旱条件下的表型表现。(C) 各株系在13天自然干旱后的存活率。(D–F) 各株系在充分浇水和干旱处理下的叶片相对含水量(D)、相对电解质渗漏(E)和丙二醛(MDA)水平(F)。误差棒代表基于至少三次独立实验重复的平均值±标准差(SD)。不同的小写和大写字母分别表示在充分浇水和干旱处理下存在统计学显著差异(p < 0.05)。符号*、**、和***分别表示与对照组相比在p< 0.05、p < 0.01和p < 0.001水平上存在显著差异;“ns”表示无统计学显著差异。下同。
图2. MfERF053正向调控紫花苜蓿的根重。 (A) RNAi、WT和OE紫花苜蓿株系在自然干旱胁迫处理下的根系表型特征。(B, C) 各株系在充分浇水和干旱处理生长环境下的根系相对含水量(B)和根重(C)。
3.2. 过表达MfERF053通过调控气孔运动减少苜蓿叶片水分流失
离体失水:OE叶片保水能力更强。
气孔动态:OE株系气孔关闭更显著。
使用各株系的离体叶片在室温下进行了8小时的风干实验。2小时后,RNAi株系的叶片表现出轻微的萎蔫症状,而WT和OE株系的叶片表型保持正常;随着时间的推移,RNAi株系叶片的萎蔫症状最为严重。在整个8小时的动态脱水过程中,OE株系叶片保持了最多的水分(54.15%),其次是WT植株叶片(38.15%),而RNAi株系叶片保持的水分最少(9.22%)。为阐明OE株系叶片维持较高含水量的机制,研究评估了RNAi、WT和OE紫花苜蓿株系叶片下表皮的气孔密度、开度及调控动态。三种株系叶片的气孔密度无显著差异。在充分浇水条件下,OE株系的平均气孔开度(宽长比为0.32)显著小于RNAi株系(0.39)。在干旱胁迫下,所有株系的平均气孔开度均急剧减小:OE株系的气孔开度(0.20)显著小于WT植株(0.25),而WT植株的气孔开度又显著小于RNAi株系(0.30)。此外,在充分浇水条件下,各株系间的气孔开闭状态无明显差异;然而,在干旱胁迫下,OE株系中完全关闭的气孔比例(35.80%)高于WT株系(23.59%)和RNAi株系(9.98%),而RNAi株系中完全开放的气孔比例(44.89%)则大于WT株系(28.26%)和OE株系(19.76%)。这些观察结果表明,MfERF053可能通过介导气孔关闭来控制干旱胁迫下的叶片水分流失(Fig. 3)。
图3. 过表达MfERF053在干旱胁迫下驱动紫花苜蓿气孔关闭。 (A) 各株系离体叶片风干8小时后的表型。(B) 离体叶片的失水率。(C) 各株系的气孔密度。(D) RNAi、WT和OE紫花苜蓿株系在自然干旱下的气孔形态特征。(E) 各株系在充分浇水和干旱处理下的气孔导度。(F, G) 紫花苜蓿叶片在充分浇水(F)和干旱(G)条件下三种气孔状态(完全开放/部分开放/完全关闭)的比例。
3.3. 过表达MfERF053增强干旱胁迫下ROS清除的抗氧化酶活性
ROS积累:OE株系ROS水平显著降低。
酶活变化:OE株系CAT和APX活性更高。
为评估MfERF053在干旱引发的氧化胁迫中的功能,研究通过NBT和DAB染色以及量化超氧阴离子(O₂⁻)和过氧化氢(H₂O₂)水平来评估各株系的叶片损伤严重程度。结果显示,在干旱胁迫下,所有株系叶片中的O₂⁻和H₂O₂水平均急剧上升。RNAi株系叶片的NBT和DAB染色强度强于WT和OE株系;RNAi株系中的O₂⁻和H₂O₂含量(分别为1043.50 nmol g⁻¹,6.94 μmol g⁻¹)显著高于WT株系(分别为847.47 nmol g⁻¹,5.72 μmol g⁻¹),而WT株系的水平又明显高于OE株系(分别为628.82 nmol g⁻¹,4.61 μmol g⁻¹)。这些数据表明,MfERF053通过抑制干旱暴露期间活性氧(ROS)的积累,减轻细胞损伤并增强紫花苜蓿的抗旱能力。为更深入了解MfERF053调控ROS积累的途径,研究测量了抗氧化防御通路中关键酶的活性水平。在干旱胁迫下,所有株系的过氧化氢酶(CAT)和抗坏血酸过氧化物酶(APX)的催化活性均显著增加;值得注意的是,这些酶在OE株系中的活性增幅(CAT为105.61%,APX为376.49%)远大于RNAi株系(CAT为44.23%,APX为181.85%)。这些观察结果表明,MfERF053可能通过提高抗氧化酶活性来增强ROS清除能力,从而有效减轻干旱引发的氧化损伤并增强紫花苜蓿的干旱恢复力(Fig. 4)。
图4. MfERF053在干旱胁迫下作为紫花苜蓿抗氧化防御的正向调控因子。 (A, B) RNAi、WT和OE紫花苜蓿株系在充分灌溉和干旱暴露生长条件下的NBT(A)和DAB(B)染色结果。(C, D) 各紫花苜蓿株系中超氧阴离子(O₂⁻)(C)和过氧化氢(H₂O₂)(D)的浓度。(E, F) 各株系在充分灌溉和干旱暴露生长条件下的过氧化氢酶(CAT)(E)和抗坏血酸过氧化物酶(APX)(F)的酶活性。
3.4. 过表达MfERF053增强转基因紫花苜蓿的光合作用
光系统保护:OE株系PSII效率更稳定。
色素含量:OE株系叶绿素降解减缓。
光合指数:OE株系Pn下降少WUE升高。
干旱胁迫通常会抑制光合过程。为验证MfERF053是否在干旱胁迫下调控紫花苜蓿的光合效率,研究从叶绿素荧光、叶绿素含量和光合指数三个维度进行了评估。对于叶绿素荧光参数,干旱胁迫导致所有株系的Fv/Fm显著下降。具体而言,OE株系的下降幅度(3.18%)明显小于WT植株(21.66%),而WT植株的下降幅度又明显低于RNAi株系(34.68%)。所有株系叶片的非光化学猝灭(NPQ)均有增加,其中RNAi株系的增幅最大(265.50%),该值显著大于WT株系(197.53%)和OE株系(23.63%)。这些结果表明,MfERF053可通过维持光系统II效率和平衡光能分配来增强耐旱光合性能。对于叶绿素含量,干旱胁迫下,所有株系的叶绿素a和叶绿素b含量均急剧下降,且RNAi株系的下降幅度(叶绿素a为54.39%,叶绿素b为56.56%)显著大于OE株系(叶绿素a为11.28%,叶绿素b为19.47%)。在充分浇水条件下,RNAi株系的类胡萝卜素含量(1.81 mg g⁻¹)显著高于WT株系(0.37 mg g⁻¹)和OE株系(0.39 mg g⁻¹);干旱胁迫下,RNAi株系的类胡萝卜素含量显著下降(1.37 mg g⁻¹),而在WT植株(0.55 mg g⁻¹)和OE株系(0.66 mg g⁻¹)中则显著上升。即便如此,RNAi株系的类胡萝卜素含量仍显著高于WT和OE株系。这些结果表明MfERF053可通过稳定叶绿素水平和介导类胡萝卜素的动态响应来增强紫花苜蓿的抗旱性。关于光合指数,干旱胁迫下,所有株系的净光合速率(Pn)、蒸腾速率(Tr)、气孔导度(Gs)和胞间CO₂浓度(Ci)均显著下降。在干旱条件下,RNAi株系Pn的下降幅度(68.83%)显著大于OE株系(9.69%);相反,OE株系中Tr、Gs和Ci的下降幅度(分别为44.99%、50.85%、40.35%)显著大于RNAi株系(分别为34.06%、35.71%、34.46%)。此外,在充分浇水条件下,RNAi株系的水分利用效率(WUE)(3.66 mmol CO₂ mmol⁻¹ H₂O)远低于OE株系(6.41 mmol CO₂ mmol⁻¹ H₂O);干旱胁迫下,RNAi株系和WT植株的WUE显著下降,但OE株系的WUE则显著上升。这些结果表明,MfERF053能够通过协调气孔和非气孔限制因素来增强干旱下的光合适应性。总之,MfERF053有助于在干旱暴露期间维持紫花苜蓿的光合性能(Fig. 5)。
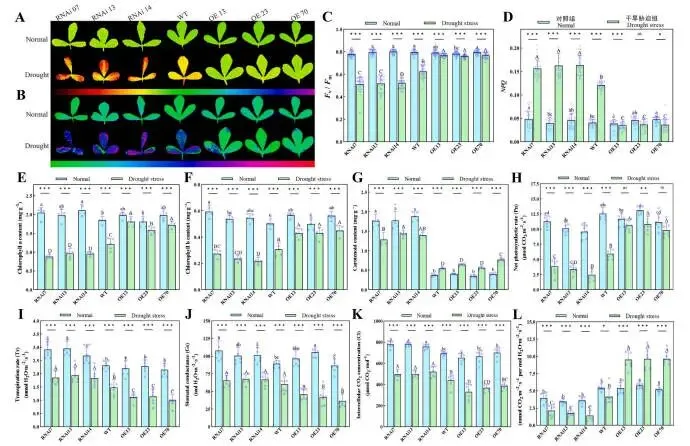
图5. 干旱胁迫下MfERF053-OE和RNAi紫花苜蓿株系的光合特性。 (A, B) RNAi、WT和OE株系在充分灌溉和干旱暴露生长条件下的Fv/Fm(A)和NPQ(B)图谱。(C, D) Fv/Fm(C)和NPQ(D)的定量值。(E–G) 各株系在充分灌溉和干旱暴露生长条件下的叶绿素a(E)、叶绿素b(F)和类胡萝卜素(G)的浓度。(H–L) 各株系在充分灌溉和干旱暴露生长条件下的净光合速率(H)、蒸腾速率(I)、气孔导度(J)、胞间CO₂浓度(K)和水分利用效率(L)。
3.5. MfERF053介导的抗旱机制分析
转录组分析:揭示基因表达谱变化。
功能富集:聚焦激素、氧化、光合。
通路解析:明确核心通路调控模式。
网络构建:鉴定协同调控基因模块。
为阐明MfERF053介导紫花苜蓿抗旱性的分子途径,研究对在正常生长条件或5天干旱胁迫下的MfERF053 RNAi、WT及OE株系的叶片和根系样本进行了RNA测序(RNA-seq)。测序数据质量评估显示其准确可靠,足以支持后续分析。主成分分析(PCA)表明,不同株系基因型和干旱胁迫处理对转录组表达模式均有显著影响。差异表达基因(DEGs)的统计评估揭示了MfERF053介导的干旱响应基因调控具有组织特异性。对各株系在干旱胁迫下共调控的DEGs进KEGG和基GO富集分析,结果表明:叶片组织中,上调的DEGs主要富集于“植物激素信号转导”和“精氨酸和脯氨酸代谢”等生物学途径;根系组织中,上调的DEGs集中于“精氨酸和脯氨酸代谢”和“代谢途径”。对叶片和根系组织的综合富集分析显示,“植物激素信号转导(ABA途径)”、“氧化还原酶活性”和“光合作用相关途径”是最显著富集的通路,证实MfERF053主要通过调控这些途径介导抗旱性(Fig. 6)。对核心通路的进一步解析阐明了MfERF053的调控模式:在ABA信号通路中,MfERF053通过上调ABA受体基因PYR/PYL、激酶基因SnRK2和转录因子基因ABF,同时下调负调控基因PP2C来增强ABA信号传递,从而促进气孔关闭;在氧化还原酶活性通路中,该基因显著上调CAT1和APX等基因的表达,增强抗氧化酶活性以清除ROS;在光合作用通路中,MfERF053通过下调叶绿素降解酶基因PPH和PAO、上调光保护蛋白基因ELIP和PSII修复蛋白基因FTSH6来维持光合效率(Fig. 7)。为鉴定MfERF053调控的干旱响应基因模块,研究采用加权基因共表达网络分析(WGCNA),分别在叶片和根系组织中鉴定出在OE株系中显著高表达的“紫色模块”和“绿黄色模块”,其核心基因(如参与脂肪酸代谢的ACX5、调控糖代谢的SUS4)协同作用以增强植物的抗旱性。
图6. RNAi、WT和OE紫花苜蓿株系叶片和根系中共同DEGs的KEGG和GO富集分析。 Y轴代表KEGG或GO通路;X轴代表富集因子。高FDR(错误发现率)值以红色突出显示,而低FDR值以蓝色显示。此处,富集因子指特定通路中差异表达基因数与注释基因总数的比值;富集因子越大,通路富集程度越高。
图7. 与ABA信号转导、氧化还原酶活性和光合过程相关的DEGs。 (A) ABA信号转导通路;(B) 氧化还原酶活性相关的DEGs;(C) 光合过程相关的DEGs。