东北农业大学《Carbohydr. Polym.》综述:作为功能性食品成分载体的多糖基微凝胶
生活水平的提高和健康意识的增强,使得人们对酚类化合物、类胡萝卜素和益生菌等功能性食品成分的关注度日益提升。功能性食品成分在加工、储存及消化过程中普遍存在稳定性差与生物利用度低的问题,这限制了其功能效用的发挥,从而推动了高效递送载体的研发。通过调控多糖分子结构(包括糖苷键类型、支化度、分子量及其分布、链构象等),可在不同诱导条件下构建具有目标特性的多糖基微凝胶载体。进一步通过自组装、物理包埋或化学嵌入等方式封装功能成分,可形成多糖基微凝胶递送体系。
来自东北农业大学的杜鑫等团队系统综述了多糖基微凝胶递送体系的核心功能特性(如消化特性、流变特性、水合特性等)。在此基础上深入探讨了其在不同环境下的释放行为、作用机制以及凝胶网络对释放的调控效应,并详细阐述了其在改善功能成分生物利用度、开发吞咽障碍友好型食品、作为固定化酶载体等新兴食品领域的应用。本文旨在从分子结构调控、凝胶构建到食品应用的全链条研究脉络,系统梳理多糖基微凝胶的研究体系,明确其在新兴食品领域的应用潜力。相关工作以题为“Polysaccharide-based microgels as carriers for functional food ingredients: Fabrication, functional properties, mechanisms, and applications”的综述文章发表在2026年04月08日的期刊《Carbohydrate Polymers》。

【多糖分子结构对凝胶特性、流变特性及消化特性的调控机制】
多糖分子的糖苷键类型、支化度、分子量及链构象共同决定了其结构特征。这些结构参数的差异能够调控多糖基微凝胶的凝胶特性、流变特性及消化特性等关键性质,并直接影响其网络结构(图1)。糖苷键的类型(α/β构型)与连接位置(如1,3-、1,4-、1,6-连接)直接调控多糖分子的相互作用强度、分子链聚集状态、链柔顺性及酶解特性。β-糖苷键连接的多糖通常比α-糖苷键多糖(半柔性链)表现出更高的链刚性(图1A),其溶液在同等浓度下具有更高的零剪切黏度与更显著的假塑性(剪切稀化)行为,部分体系还可能呈现触变性。糖苷键的类型与连接位置决定了多糖主链的特性,同时支化度通过调控分子间相互作用与酶结合位点,进而影响多糖的凝胶特性、流变特性及消化特性。直链多糖可通过丰富的氢键作用形成致密凝胶网络或结晶区(图1B),此类凝胶具有高刚性、高热稳定性及低溶胀率的特点,因此将其添加至肉制品中可提升持水性与结构完整性,防止烹饪后结构崩解。但在消化方面,致密网络或高结晶区反而可能限制酶分子的渗透与结合,因此其消化速率未必低于支链多糖。例如直链淀粉通过回生形成致密有序的结晶结构,阻碍了酶的渗透;而高度支化的支链淀粉结构破坏了分子的有序聚集,形成松散构象,更易被消化酶接触。
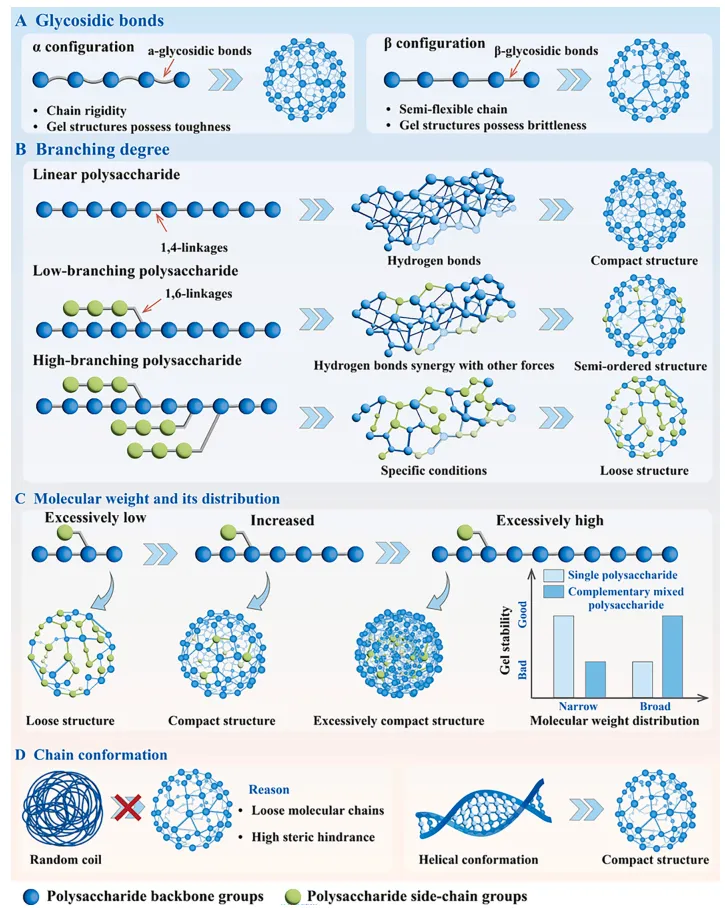
图1 多糖分子结构特性对其凝胶性质的影响
【多糖基微凝胶体系的构建】
多糖的溶胶-凝胶转变过程涉及分子链从分散状态向有序交联状态的转变,其核心驱动力是氢键、静电作用、疏水作用等非共价键的协同效应。这些弱相互作用易受环境变化(如pH、离子强度、温度、压力)的影响,因此通过精准调控加工参数可实现多糖基微凝胶的可控制备。下文将围绕pH、离子强度、温度、压力变化下多糖的结构转变与凝胶化行为展开探讨(图2),为微凝胶制备提供理论依据。pH值可通过改变多糖的溶解性、分子构象及电荷密度影响其形成微凝胶的能力。这种改变主要涉及聚合物基团(如氨基与羧基)的解离度和/或净电荷的调控。当这些基团的解离度与净电荷降低时,分子间静电斥力减弱,疏水相互作用增强,从而驱动分子聚集并形成凝胶(图2A)。
离子诱导型多糖微凝胶通过在凝胶化过程中向多糖溶液中添加离子制备。该过程利用静电相互作用中和体系电荷并形成离子交联点,从而构建三维网络结构(图2B)。凝胶状态(分散微凝胶或宏观水凝胶)受离子种类、浓度、pH及温度等因素影响。通过提高离子强度可维持收缩凝胶化过程获得微凝胶。随着温度升高,多糖分子间或分子内的次级键(如氢键)发生断裂,导致构象变化(分子链部分展开,暴露出功能基团)(图2C)。随着基团暴露,分子间作用力(包括疏水作用与静电相互作用)得到增强,促进分子链聚集,最终形成热不可逆凝胶。此外,通过热诱导不稳定凝聚液滴(蛋白质与多糖形成的复合凝聚体)转化为微凝胶的方法日益受到关注。该方法制备路线简单,无需额外添加多糖或复杂处理,仅需调节pH和/或离子强度即可实现。
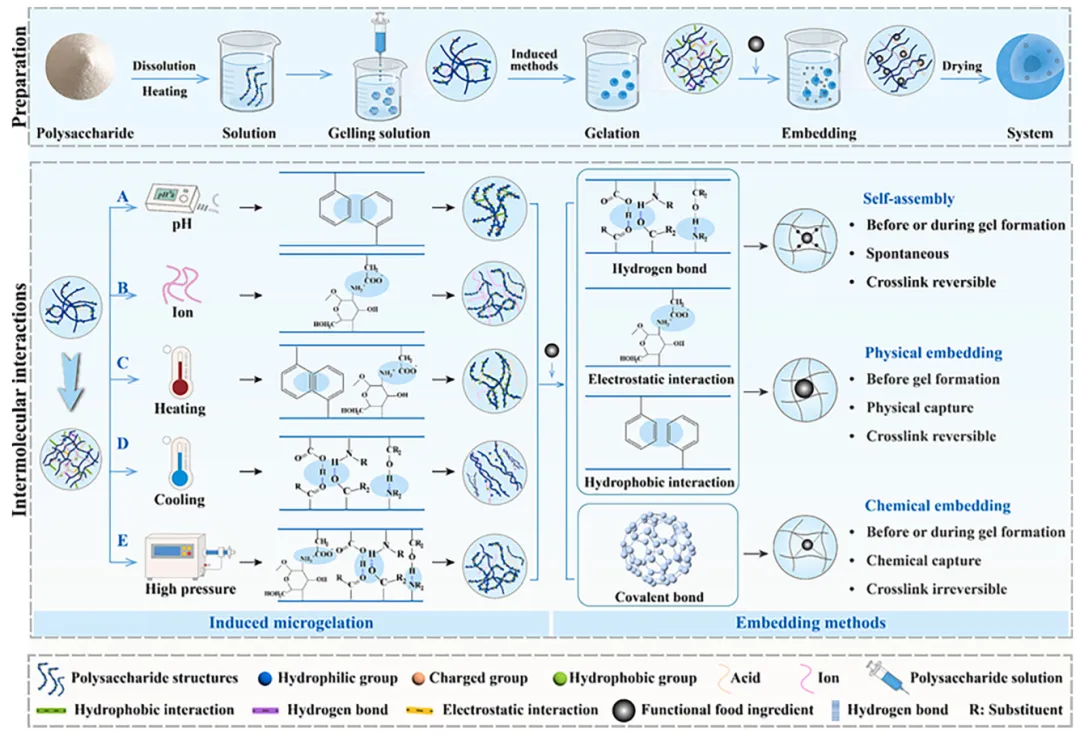
图2 多糖基微凝胶体系的形成过程及其反应条件
【多糖基微凝胶体系的功能特性与释放机制】
由多糖基微凝胶载体与功能性食品配料形成的多糖基微凝胶体系展现出多种功能特性,这些特性是食品应用的基础。为实现并有效调控这些特性,必须明确其释放行为及背后的体系机制。阐明微凝胶体系在不同消化环境中的作用机制,可为针对性设计适应这些环境的微凝胶提供关键指导(图3)。在近中性的口腔环境(pH 5–7)中,唾液酶(如将淀粉降解为麦芽糖的唾液淀粉酶)、持续分泌的唾液产生的冲刷效应,以及咀嚼和吞咽行为共同影响着功能性食品配料。这些因素不仅会损害功能性食品配料的活性,还会缩短其在口腔中的停留时间,从而降低其生物利用度。与游离的功能性食品配料相比,多糖基微凝胶可通过多种机制实现口腔环境适应性递送,并增强配料的功能功效。首先,它们可以粘附在口腔黏膜表面,延长功能性配料在作用部位的停留时间,从而抵抗唾液的冲刷和吞咽。其次,多糖基微凝胶可作为物理屏障,通过防止功能性配料与唾液酶及不利环境直接接触,最大限度地减少其活性损失。最后,凭借其微小尺寸和表面修饰特性,多糖基微凝胶可通过细胞旁路/跨细胞途径穿透口腔上皮屏障,到达固有层,从而在目标部位增强功能性食品配料的功能特性(图3A)。在此过程中,被包封的功能性配料主要通过扩散机制从凝胶网络中释放,因此可通过增加凝胶硬度等措施降低功能性食品配料在凝胶中的扩散和传质速率。
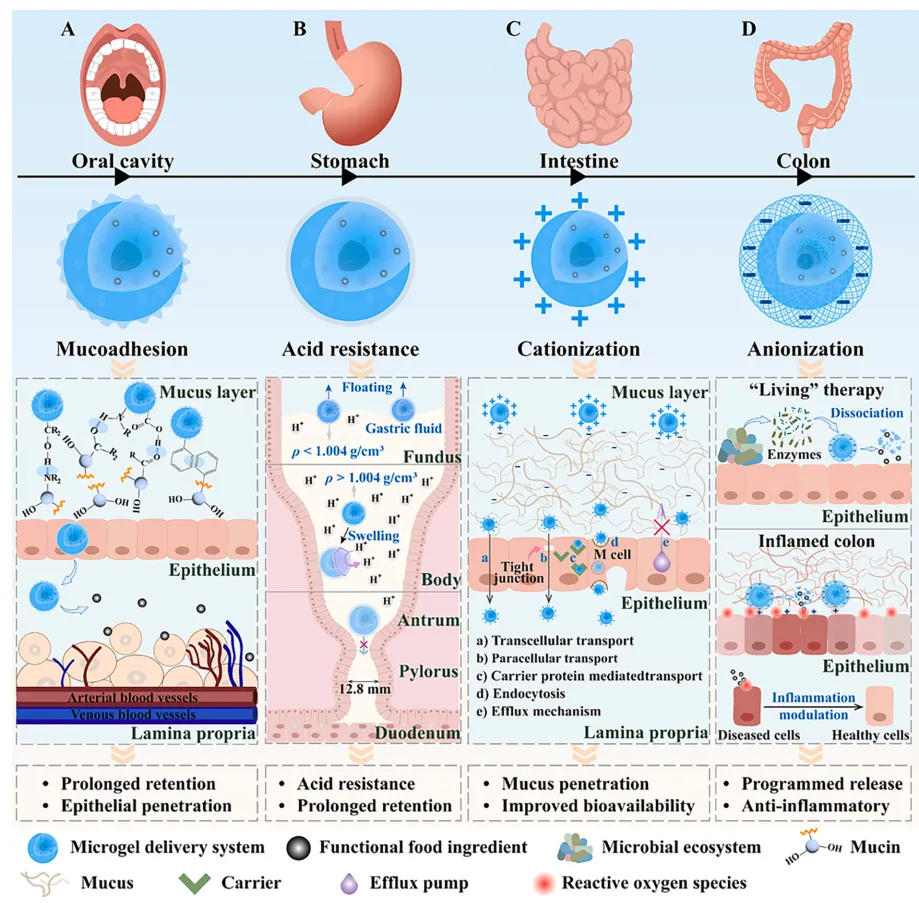
图3 多糖基微凝胶载体在消化道中对功能性食品配料的保护与递送作用
多糖基微凝胶的pH敏感性主要与多糖分子中的可电离化学基团(阴离子基团、阳离子基团和两性离子基团)以及酸敏感键有关。这些结构特征使其能在不同pH条件下发生溶胀-收缩转变或结构降解,从而实现功能性食品配料的可控释放。具体而言,多糖基微凝胶中的阴离子基团(如羧基)在低pH条件下发生质子化。此时,多糖分子内极性基团间的氢键作用显著增强,而分子间(多糖与水分子)的氢键不占主导地位。这导致微凝胶亲水性下降,发生收缩。随着pH升高,阴离子基团逐渐解离形成带负电的离子基团,基团间的静电排斥作用取代分子内氢键成为主导力,促使多糖链伸展,引起微凝胶溶胀(图4A)。相比之下,多糖基微凝胶中的阳离子基团则表现出相反的pH响应行为。
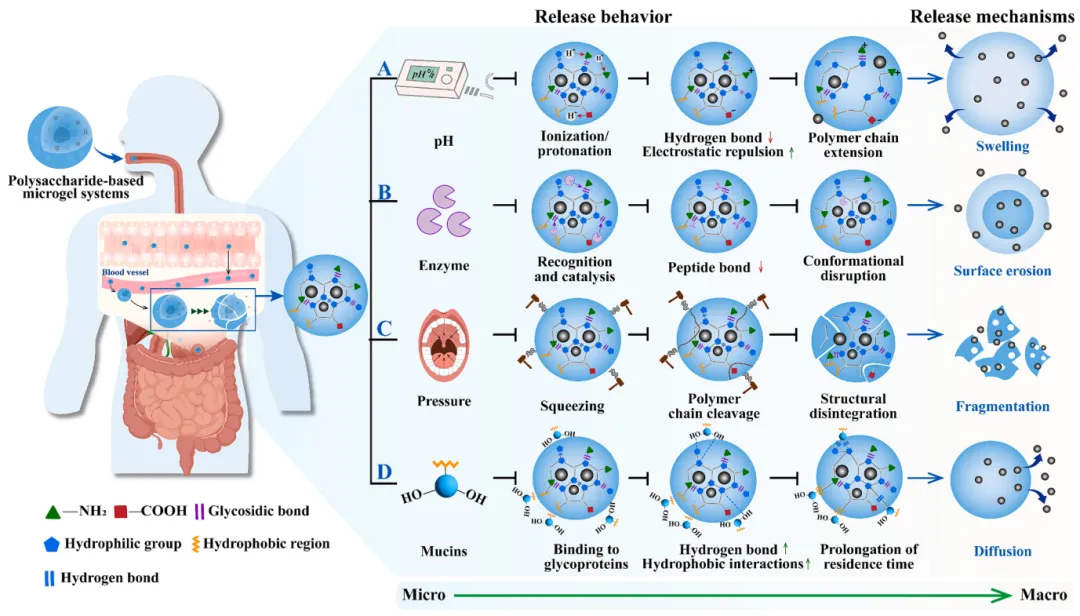
图4 功能性食品配料在多糖基微凝胶体系中的释放行为与机制
【总结与展望】
多糖基微凝胶作为功能性食品配料载体,因其固有的安全性和可调控性而备受关注。通过调控多糖分子结构并结合pH诱导、温度诱导等形成方法,可构建具有定制化功能的微凝胶载体。功能性食品配料可通过自组装、物理包埋或化学包封等方式高效负载其中。该体系不仅具有良好的可控消化特性,能显著提升功能性食品配料的生物利用度,还具备优异的流变学特性与持水性,在开发吞咽障碍友好型食品方面展现出巨大潜力。此外,通过调控微凝胶网络结构响应不同环境刺激,可实现对其释放行为的精准调控。目前,多糖基微凝胶的研究尚处于初级阶段,需进一步深入探索以满足高端应用的具体需求,并充分发掘和实现其在食品领域的潜力。
参考资料:
https://doi.org/10.1016/j.carbpol.2026.125287
来源:EngineeringForLife
声明:仅代表作者个人观点,用于研究用途,作者水平有限,如有不科学之处,请在下方留言指正!
