JIPB|华中农业大学刘秀群教授课题组通过泛基因组分析揭示青藏高原杜鹃花属植物高海拔适应性的遗传机制
- 2026-05-09 06:59:35

青藏高原是全球生物起源和多样性热点地区, 孕育了丰富的动植物种类。该地区气候环境恶劣, 具有严寒、低氧、高紫外辐射等特点。如此严酷的生存条件却无法限制生命的绽放——杜鹃花属 (Rhododendron) 作为中国-喜马拉雅植物区系的标志性物种, 以全球近1,200种的规模, 被列为北半球最大的木本植物属。该属广泛分布于亚洲、欧洲和北美洲, 从低海拔的幽谷湿地到高海拔的雪线边缘, 都能见到其傲立的身影。杜鹃花属不仅具有重要的园艺价值, 还对山地 (如青藏高原) 生态系统的稳定性至关重要。然而, 青藏高原地区的杜鹃花如何适应这种极端环境的分子机制, 目前仍知之甚少。与该属的低海拔种质相比, 高海拔杜鹃花在高原适应性上有何优势尚不明确。
近日, JIPB在线发表了华中农业大学刘秀群教授课题组题为“Pangenome analysis reveals the genetic mechanism underlying high-altitude adaptation in Qinghai–Xizang (Tibet) Plateau Rhododendron”的研究论文 (https://doi.org/10.1111/jipb.70252)。该研究构建了杜鹃花属基于图谱的泛基因组, 揭示了抗逆基因内或其附近的LTRs和结构变异是影响高原杜鹃花适应性的关键。并且, 该研究发现高海拔杜鹃花冷感知基因的快速响应以及CBF/DREB1相关信号通路的持续激活是杜鹃花适应高原低温环境的主要优势。
研究团队完成了7种杜鹃花属植物染色体水平的全基因组测序工作 (图1), 并结合11种已发布杜鹃花和其他14种被子植物基因组的低拷贝直系同源基因簇构建了系统发育树, 其拓扑结构与APG IV一致。根据分子钟分析明确了杜鹃花属与越橘属分化时间 (约在57.7–62.8Mya), 以及映山红亚属和马银花亚属与其他的种类分化时间 (约在47.4 Mya), 此后杜鹃花属的基因组显著扩张 (图1和图2)。基于低拷贝直系同源基因簇和SNP的系统发育分析支持马银花亚属 (subg.Azaleastrum) 整合到映山红亚属 (subg.Tsutsusi) 中的观点 (图2)。利用KEGG分析对3种生长于极高海拔环境的杜鹃花属物种进行基因家族扩张与收缩模式比较时发现, 雪层杜鹃 (R. nivale) 与毛冠杜鹃 (R. laudandum) 具有共同的进化趋势。相比之下, 藏南杜鹃 (R. principis) 呈现出独特模式, 这可能是其株型的显著差异所致。为探究杜鹃花属进化史中的全基因组复制 (WGD) 事件, 对5亚属9种代表性杜鹃花属种类进行了共线性分析, 支持杜鹃花属谱系中发生过两次WGD事件的结论。利用18种杜鹃花属植物的基因组与祖先核心真双子叶植物核型 (ACEK) 相结合重建了杜鹃花属核型的进化轨迹。
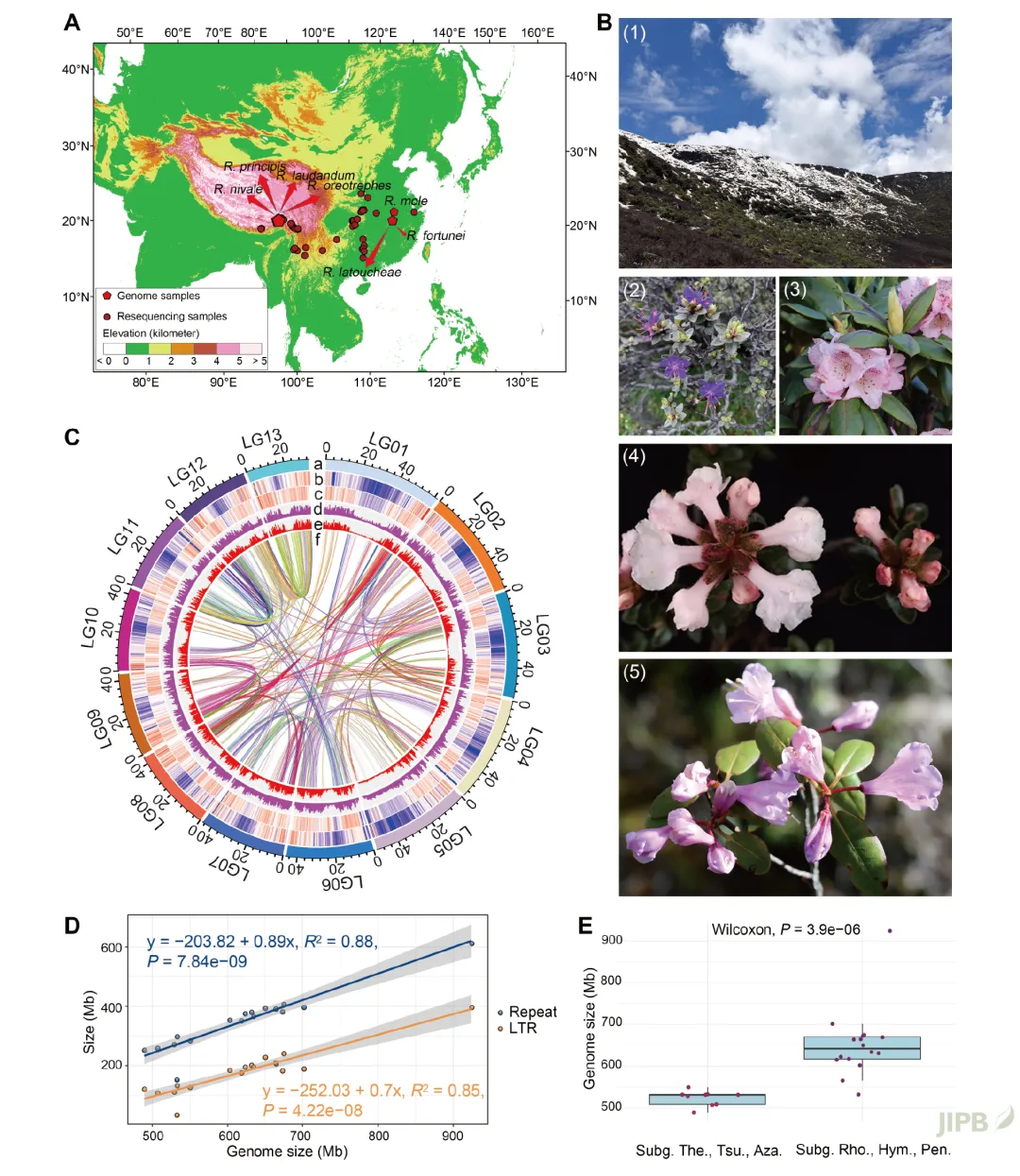
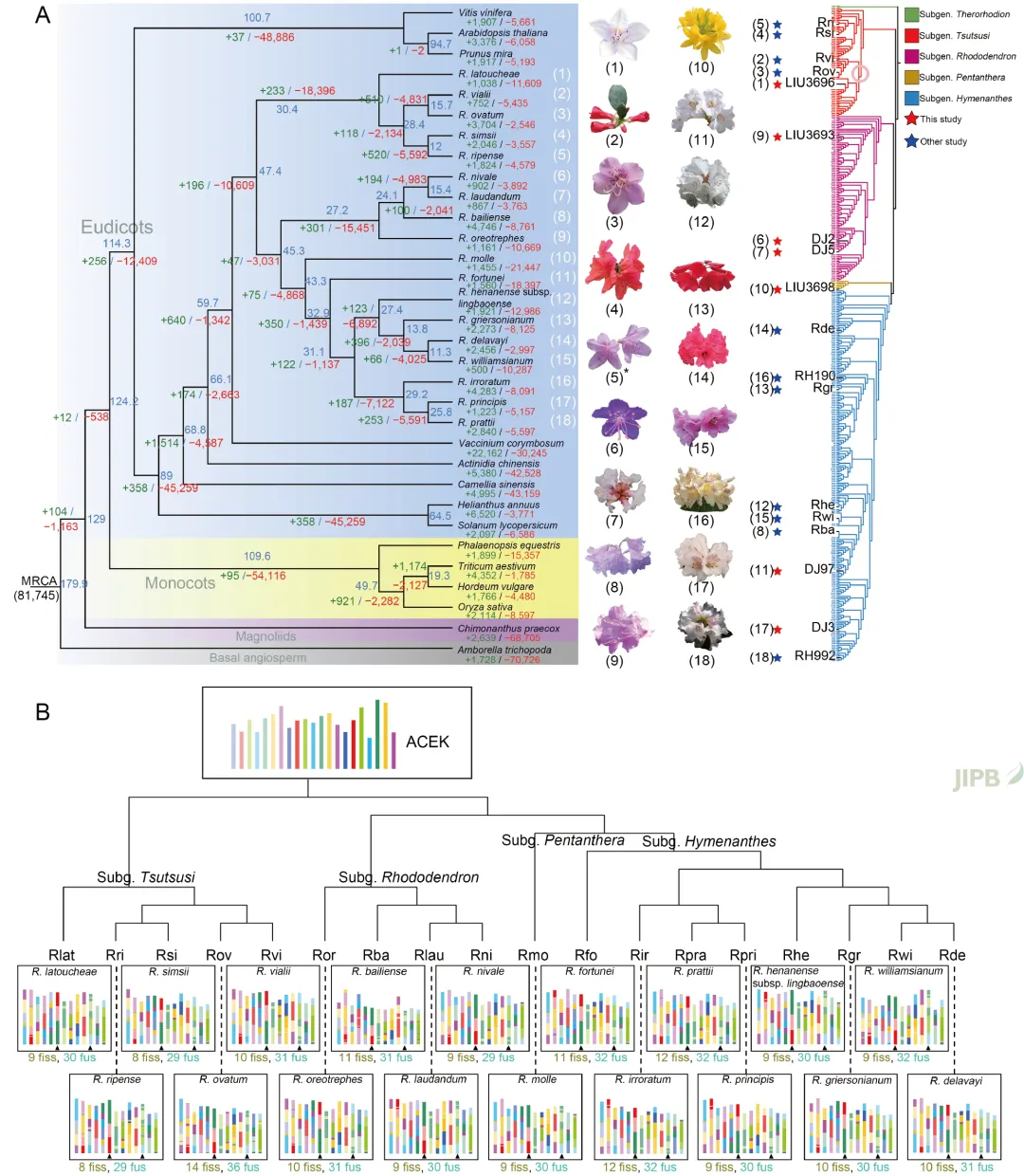
图2 杜鹃花属的比较基因组和核型演化分析
该研究基于18种杜鹃花属植物全基因组的遗传信息构建了基于图形的泛基因组 (图3)。将杜鹃花属植物分为高海拔组和低海拔组, GO结果显示高海拔组特有基因家族主要与核苷酸结合及膜相关过程关联, 而低海拔组特有基因家族则主要与核酸酶活性和离子结合相关。进一步的KEGG通路分析表明, 高海拔组在辅因子、维生素、氨基酸和碳水化合物代谢相关通路中显著富集; 而低海拔组特有基因家族主要富集于萜类和聚酮化合物生物合成通路以及环境响应通路。另外, 该研究对高、低海拔杜鹃花特有LTRs下游基因进行了富集分析, 发现高海拔组特有LTRs所影响的基因显著富集在脂质代谢、碳水化合物代谢、氨基酸代谢等途径, 例如不饱和脂肪酸的生物合成、角质层、木栓层和蜡的生物合成、淀粉和蔗糖代谢等通路。这些通路与高海拔环境抗寒抗紫外等逆境相关。低海拔特有LTRs所影响基因则显著富集于环境适应中的植物-病原体互作通路、核酸复制和修复、萜类化合物和聚酮类化合物的代谢、氨基酸代谢等通路。这一结果与高、低海拔杜鹃花特有基因家族所处通路类似, 这些抗逆基因及LTRs所处位置可能是杜鹃花环境适应性分化的关键。
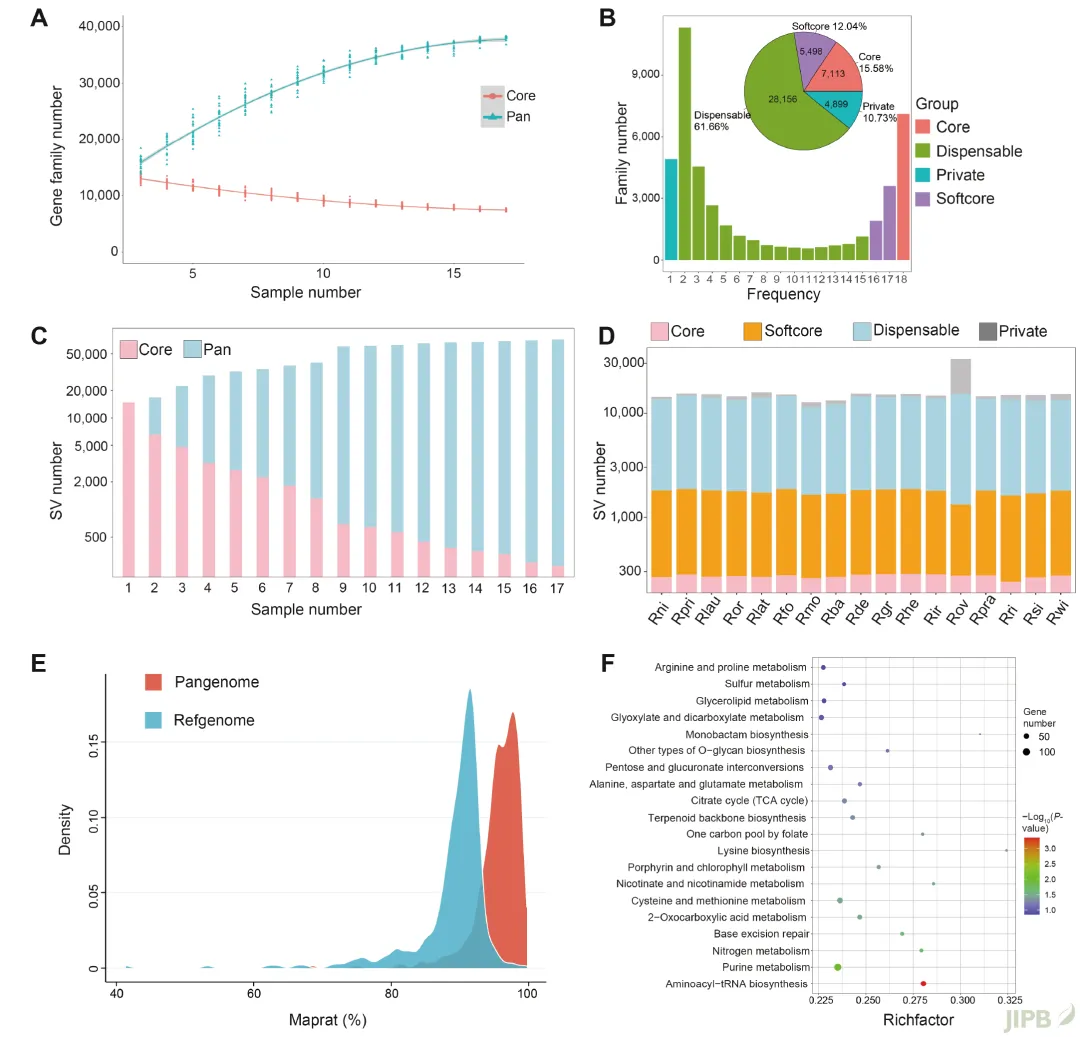
图3 杜鹃花属泛基因组
青藏高原野生杜鹃花群体所面临的环境压力比其他地区的杜鹃花更为严苛, 这些高原群体可能在基因组水平上进化出了强效且保守的适应机制。为探究共享的遗传适应性, 该研究利用389份杜鹃花重测序数据, 结合LFMM和Fst分析, 定位到了与环境和适应性分化相关的基因组变异并筛选了高原适应性候选基因 (图4)。这些基因主要通过信号转导、膜脂稳定、渗透调节等途径介导温度响应或直接、间接地增强植株的紫外防护能力。其中, 信号转导相关的CML基因家族和CPK基因家族成员在两个模型中被反复检出。候选基因中, RFS6和STS1通过调控棉籽糖家族寡糖的生物合成促进渗透平衡。二者存在群体变异模式, 在青藏高原及周边山区的所有群体样本中均为参考等位基因型, 这些地区以较低年均气温为特征, 而其突变型仅见于年均气温较高的地区。LACS4催化长链脂肪酸的活化并维持膜脂稳定性。其突变等位基因 (A) 主要集中于青藏高原群体, 而参考等位基因 (G) 则在其他地区群体中占主导地位。
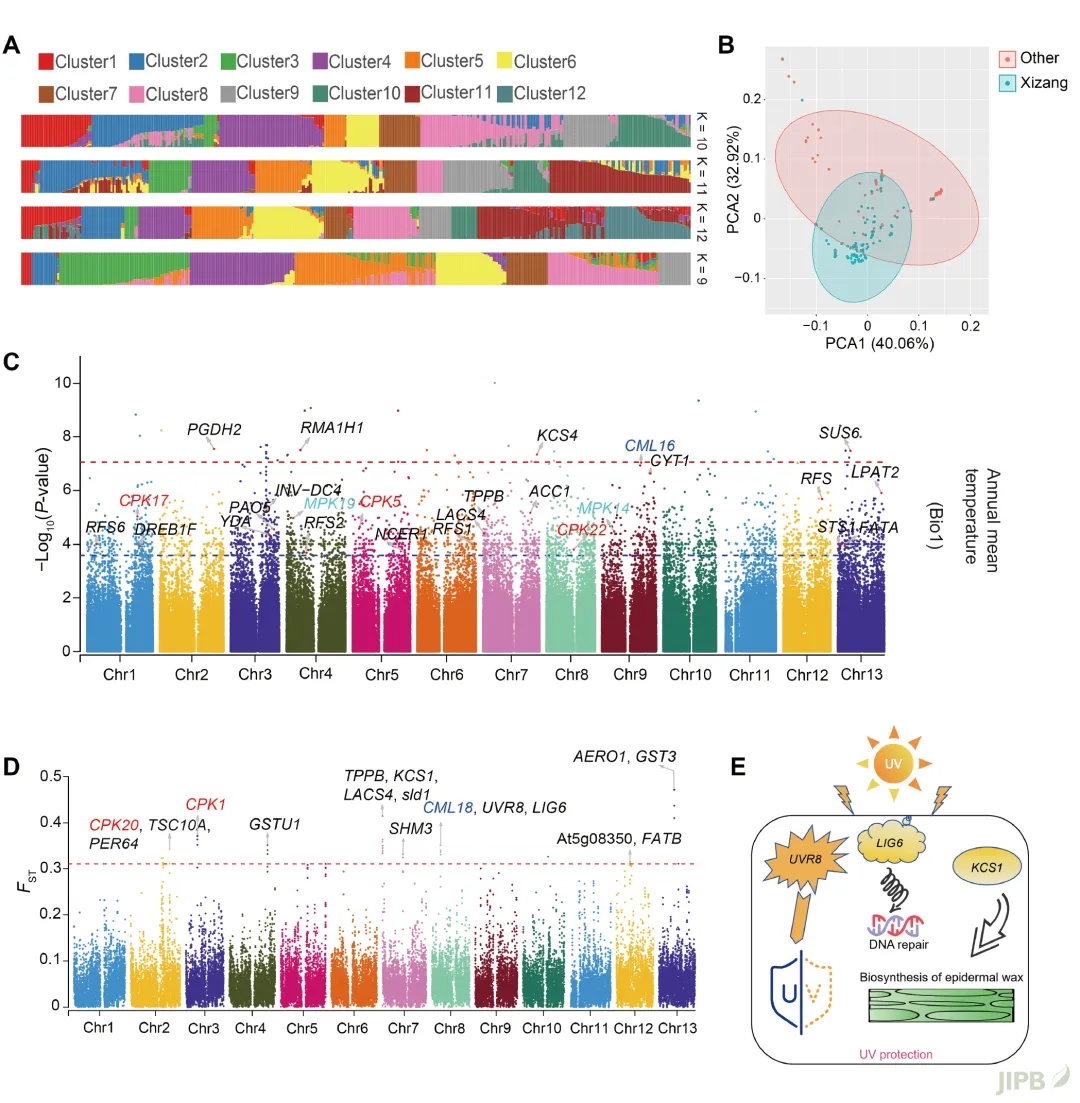
此外, 参与磷脂酸代谢的LPAT2也呈现出独特的遗传模式 (图5)。相较于参考基因组, 9种高海拔杜鹃花中有8种 (88.89%) 在该基因内存在约492 bp的插入片段, 而这一插入片段仅在9种低海拔杜鹃花中的5种中被检测到。该插入片段主要分布于青藏高原地区的杜鹃花群体中, 约占样本总数的半数; 而年均气温较高的地区群体中则出现频率明显较低。
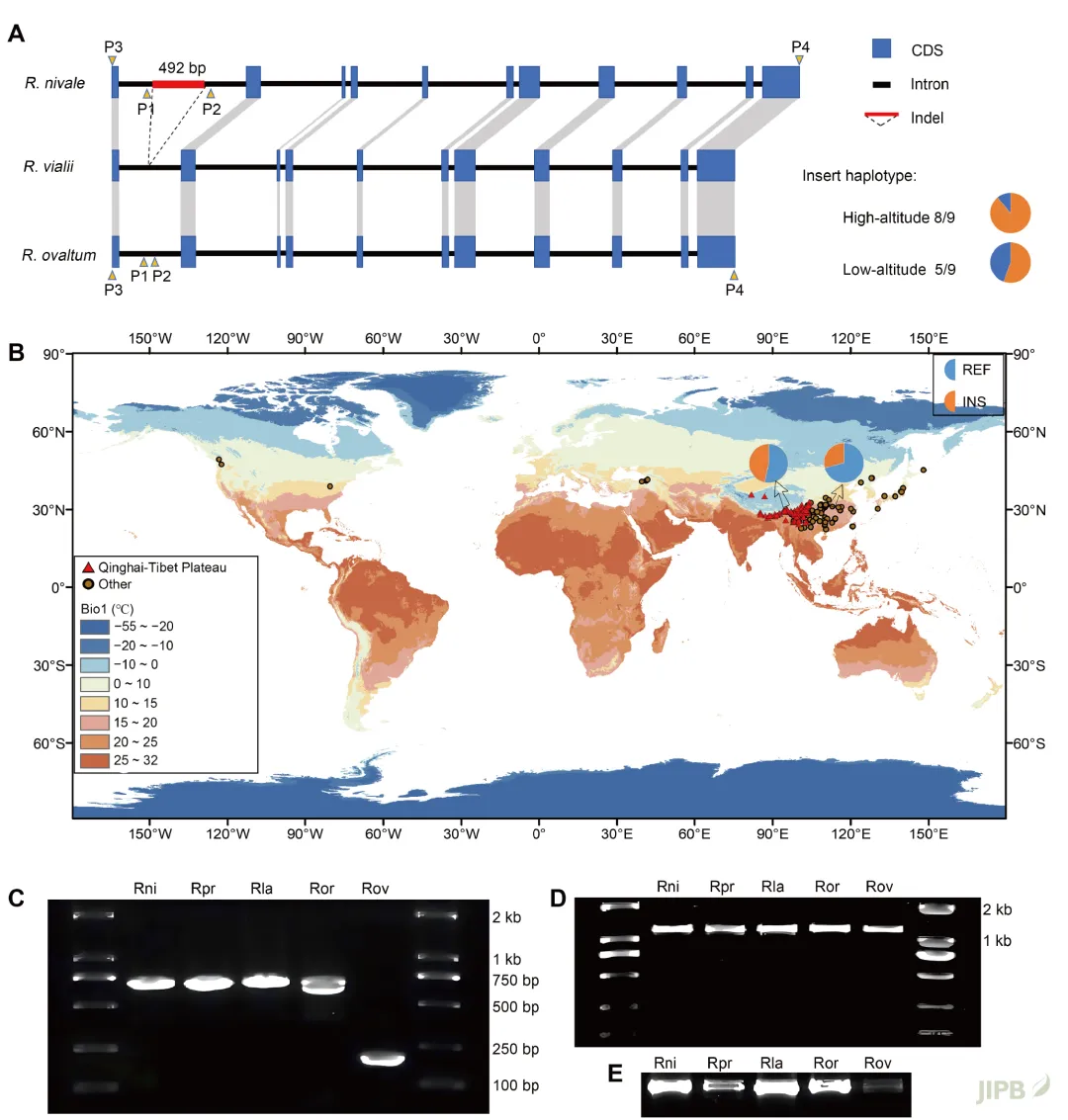
图5 高、低海拔杜鹃花属植物LPAT2结构变异与群体分布模式
为探究高海拔杜鹃花在高原适应上的优势, 该研究对物种特异性响应机制进行了分析。选取高海拔的山育杜鹃 (R. oreotrephes) 和低海拔的羊踯躅 (R. molle) 进行低温处理和转录组分析。结果表明, 杜鹃花属植物的冷胁迫响应通过多种相互关联的通路实现。山育杜鹃中, 冷感知基因 (如CML3等)、信号转导基因 (如CPK1、MAPKKK20、MPK3等) 以及应激反应基因 (包括DREB1家族) 在初始冷暴露阶段迅速上调, 并在整个后续冷应激阶段维持高水平表达 (图6)。相比之下, 羊踯躅中的这些基因变化不大或呈现下调, 部分基因仅在后续冷暴露阶段才显著上调。这一结果在实时荧光定量中也得到了验证。高海拔杜鹃花冷感知基因的快速响应以及CBF相关信号通路的持续激活是杜鹃花属植物适应高海拔寒冷环境的优势机制。相比之下, 低海拔杜鹃花在冷胁迫早期主要依赖氧化还原调节、乙烯信号传导和糖代谢等其他替代性抗寒途径。此类响应可能不足以提供有效的抗寒能力, 导致冷暴露初期出现损伤并影响长期存活。此外, 通过LFMM和Fst分析检测到的多个候选基因在转录组数据中也呈现显著差异表达。GPC1和DREB1E的转基因功能实验表明, 二者可以显著提高烤烟和拟南芥的抗寒能力。
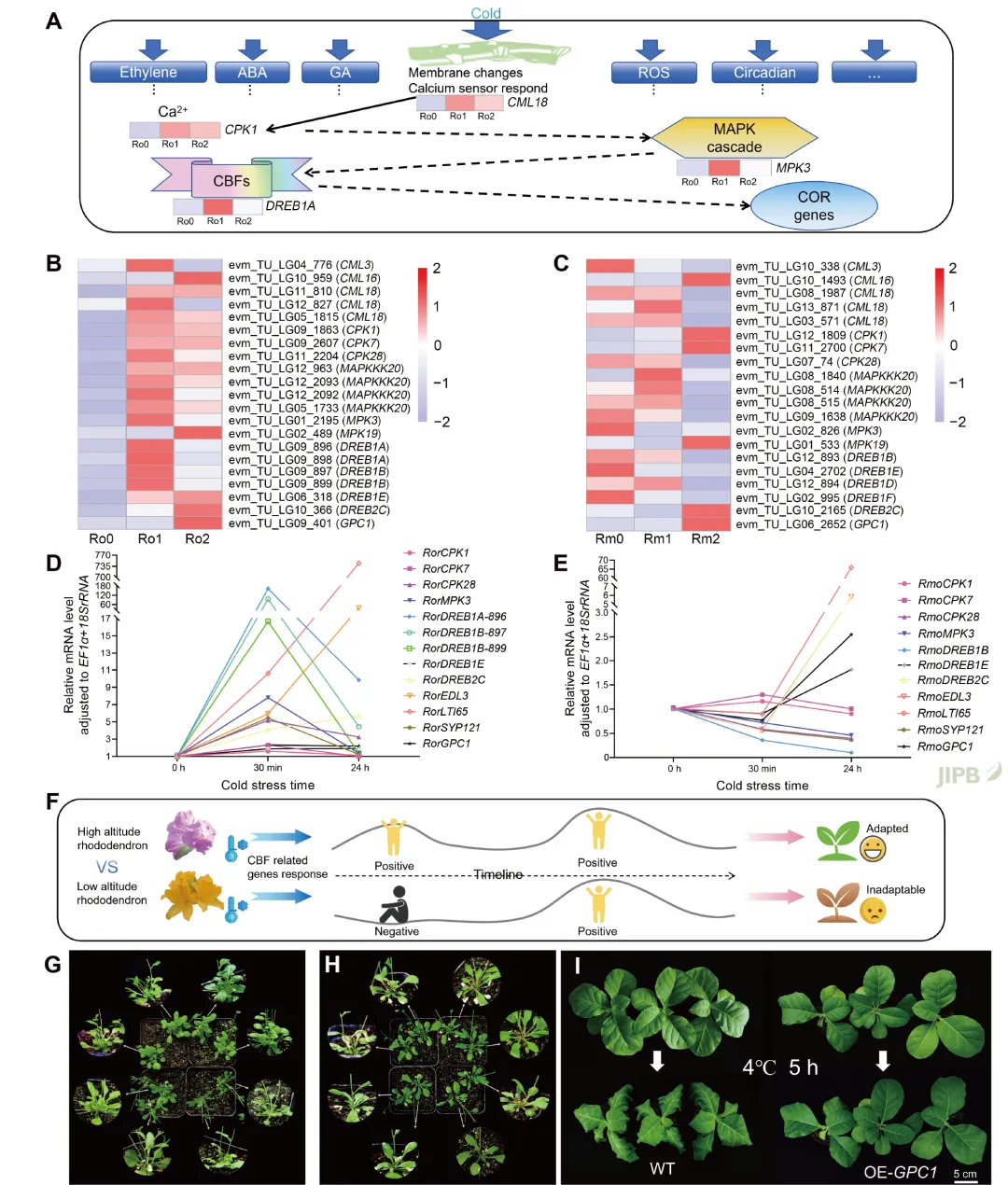
图6 冷胁迫条件下基因表达的差异
华中农业大学博士研究生周浩洋为论文第一作者, 华中农业大学刘秀群教授和金双侠教授为论文的共同通讯作者。华中农业大学许忠平研究员、博士研究生曾凡煌、博士研究生桑海煜、孙苗教授、傅强高级工程师、赵凯歌副教授、包满珠教授、武汉博瑞智客生物科技有限公司的刘振华、西藏自治区农牧科学院谭大明副研究员参与了该项研究。该研究受到西藏自治区科技计划重点研发及转化项目 (XZ202001ZY0016N、XZ202201ZY0006N) 及国家杰出青年科学基金 (32325039) 的支持。
#Cell and Developmental Biology#
#Functional Omics and Systems Biology#
#Molecular Ecology and Evolution#
#Photosynthesis and Crop Physiology#
物种合集:
#水稻##小麦##大豆##玉米##拟南芥##蔬菜##园艺植物#
推荐阅读:


关注JIPB
获知最新研究


