Plant Stress | 甘肃农业大学/兰州大学团队系统综述Rubisco降解机制及其在作物改良中的调控潜力
- 2026-04-25 18:18:21



2026年3月31日,甘肃农业大学农学院孙万仓教授团队与兰州大学生命科学学院安黎哲教授团队在Plant Stress在线发表了题为“Rubisco degradation: A new target for crop improvement”的综述论文。该文系统梳理了Rubisco在植物细胞内的降解通路,重点阐述了其在不同生理与胁迫条件下的选择性降解机制,并探讨了通过调控Rubisco降解实现作物抗逆性提升、产量优化与氮素利用效率改善的潜在路径。
研究背景
Rubisco(核酮糖-1,5-二磷酸羧化酶/加氧酶)是植物叶片中含量最高的可溶性蛋白,占叶片总可溶性蛋白的40%-50%、总氮的30%。它不仅催化光合作用中的碳固定,还在叶片衰老和逆境条件下作为关键的氮、碳储备库。Rubisco的高效降解与氮素再分配直接关系到作物的产量形成与资源利用效率。因此,解析其降解机制,已成为作物改良研究的前沿热点。
综述内容
该论文首先总结了Rubisco的降解通路, Rubisco的降解主要发生在叶绿体内部与液泡两个区域,涉及多条独立又协同的通路:
1.叶绿体内降解:由CND41、Clp、FtsH、Deg等蛋白酶介导,主要清除氧化损伤或构象异常的Rubisco(图1)。
2.液泡依赖降解:包括自噬途径(RCBs、ATI-PS、全叶绿体自噬)和类微自噬途径(SAVs、CV通路),占Rubisco降解总量的70%-80%,是叶片衰老和胁迫条件下氮素再分配的主要途径(图2)。
3. 液泡膜破裂降解:在程序性细胞死亡或严重胁迫下发生,为非选择性“终极”降解途径(图3)。
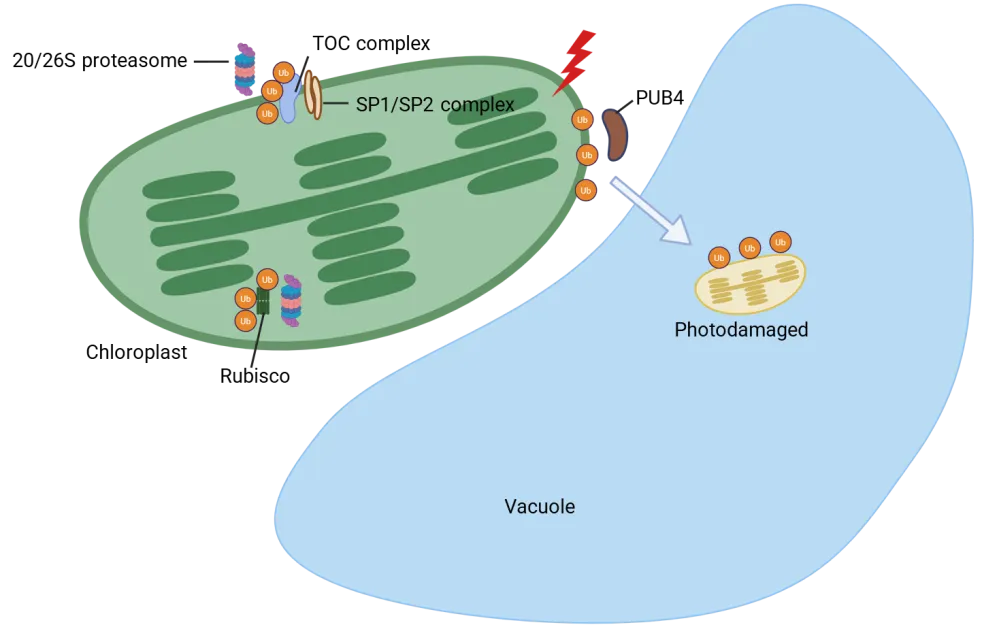
图1 泛素化介导的叶绿体蛋白质及叶绿体的降解过程
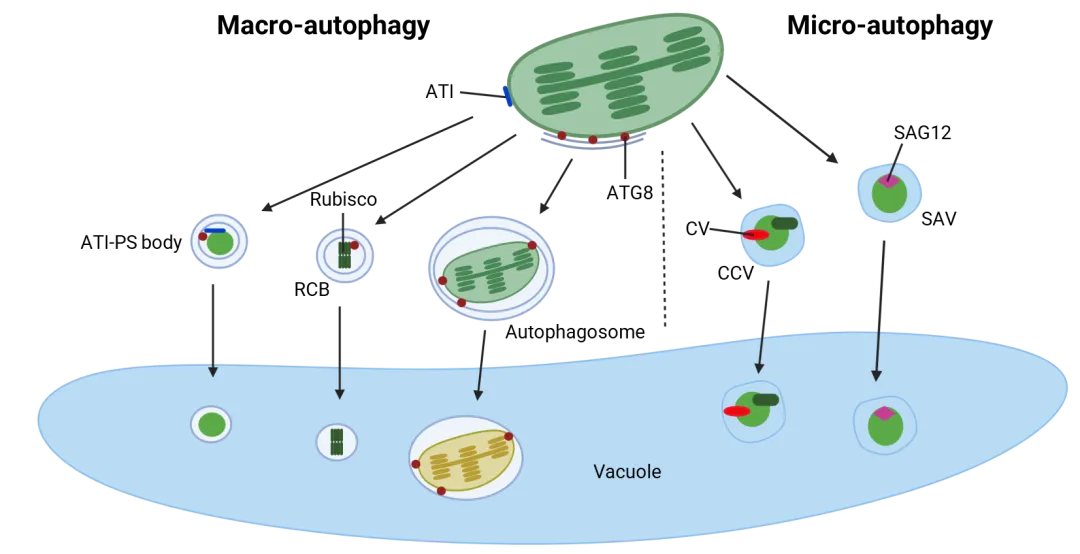
图2 液泡介导的Rubisco降解途径
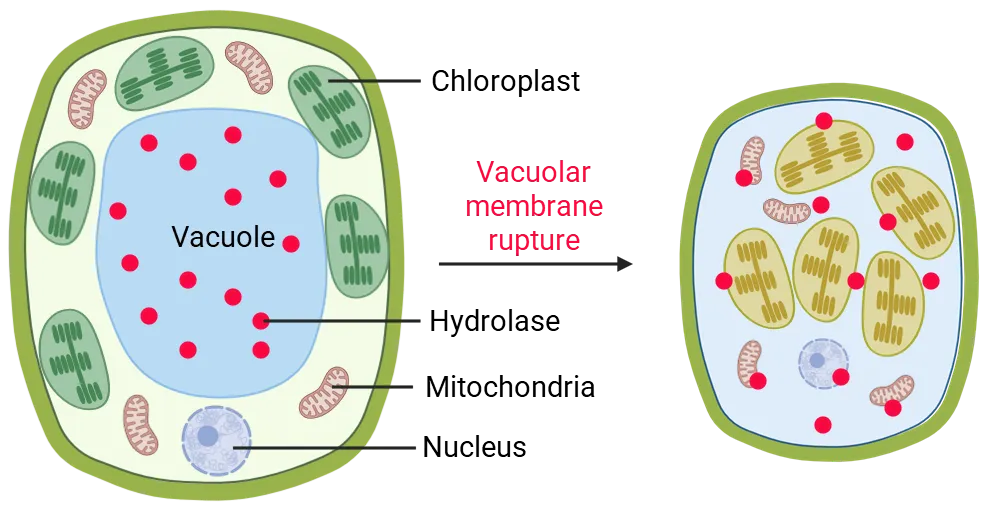
图3 液泡破裂引起的Rubisco降解
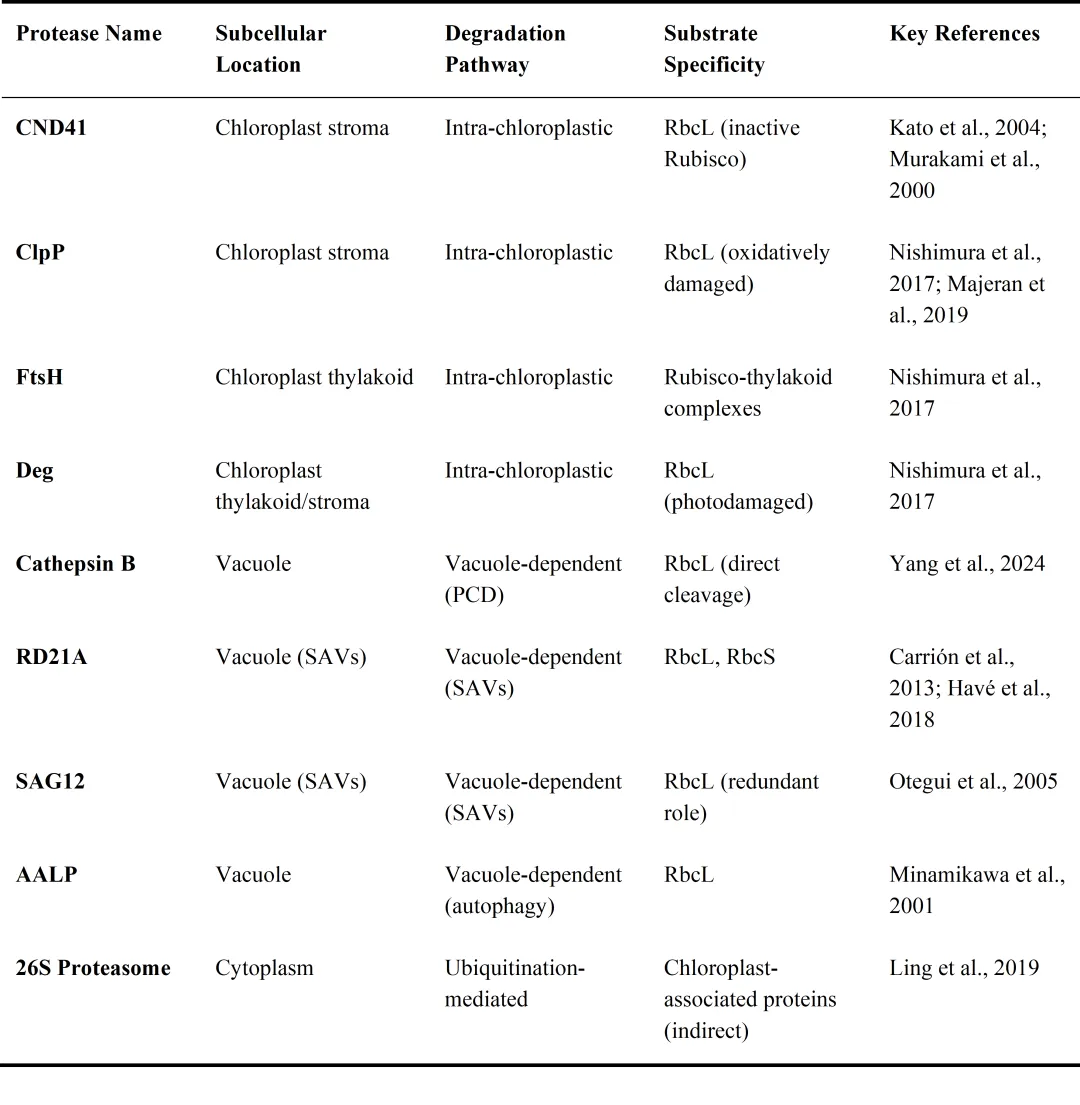
另外,文章系统归纳了参与Rubisco降解的关键蛋白酶及其功能偏好(图4,表1)。其中,CND41、ClpP、FtsH等参与叶绿体内降解;RD21A、SAG12、Cathepsin B等则在液泡中发挥核心作用。尤其在低温诱导的程序性细胞死亡中,Cathepsin B被证实可直接降解Rubisco大亚基RbcL,为植物在极端环境下的氮素再利用提供了新机制。
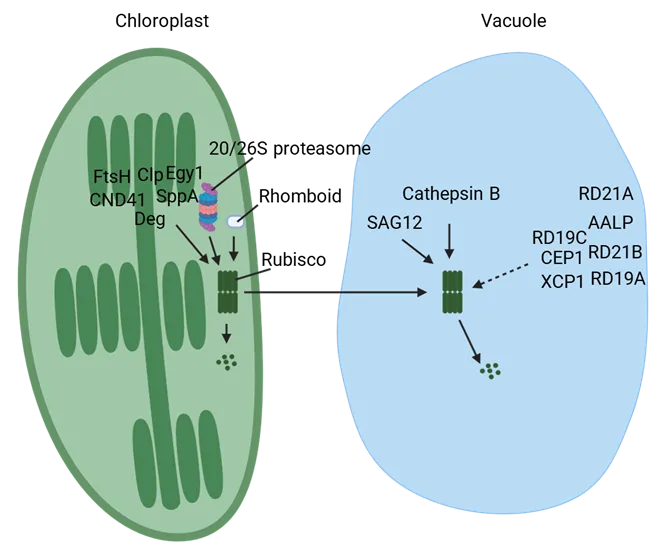
图4 参与Rubisco降解的关键蛋白酶
表1 参与Rubisco降解的关键蛋白酶
最后,基于对降解机制的深入理解,文章提出了三大应用方向:
1
增强抗逆性
通过调控PUB4、ATG8、RD21A、VPE等基因表达,可提升作物对高温、干旱、低氮、盐碱及病害的耐受能力;
2
优化产量形成
精准调控CND41、ATI1、ATG5等基因的时空表达,可在保障光合功能的同时促进氮素向籽粒的高效转运,提升千粒重与结实率;
3
提升氮素利用效率
过表达ClpP1、RD21A等基因,可显著增强Rubisco在低氮条件下的降解速率,推动氮素从营养器官向籽粒的再分配,降低作物对氮肥的依赖。
结论与展望
Rubisco降解是一个由多条通路与多重蛋白酶协同调控的复杂过程,其精准调控对作物的碳氮平衡、逆境适应与产量形成具有决定性作用。尽管当前已识别出多条关键通路与核心蛋白酶,但仍存在若干关键空白亟待填补:
1. Rubisco是否直接受E3泛素连接酶调控尚不明确;
2. CND41在中性叶绿体基质中的激活机制仍存疑;
3. 不同降解通路间的协同与互作机制尚待系统解析。
未来,结合多组学技术、CRISPR-Cas9基因编辑与高分辨率活体成像,将有望实现对Rubisco降解通路的时空精准调控,为培育高产、高效、高抗的作物新品种提供理论支撑与分子工具。
研究团队
甘肃农业大学农学院杨刚副教授为论文第一作者,甘肃农业大学农学院孙万仓教授与兰州大学生命科学学院安黎哲教授为共同通讯作者。兰州大学张华副教授、甘肃农业大学范婷婷副教授、马骊副研究员、蒲媛媛副教授、刘丽君副研究员、王旺田教授和武军艳教授等参与了本论文的撰写。该论文得到了甘肃农业大学公招博士科研启动项目、秦州区2025年基层农技推广体系改革与建设项目及甘肃省科技厅重大专项的资助。
原文链接
https://doi.org/10.1016/j.stress.2026.101364
2026 年,Plant Stress计划进一步加强学术成果的推广与交流,现面向广大学术同仁发出诚挚邀请,招募更多老师参与期刊学术内容的共建(名额不限)。

如有参与意愿,欢迎扫描上方二维码添加运营人员微信,备注 “Plant Stress学术推广” 即可。
如您想加入Plant Stress期刊交流群,同样可以通过二维码添加,备注 “Plant Stress期刊交流群” 。
再次感谢大家对Plant Stress的长期关注与支持!
广告位招租
微信15982378817备注广告咨询
微信公众号|植物科学 - 爱思唯尔
聚焦Elsevier旗下
植物科学期刊最新研究进展
点击阅读原文
