NC(Q1/15.7)|安徽农业大学常成教授团队揭示钙信号介导小麦抗穗发芽的分子机制
- 2026-05-09 01:02:01



文献标题:TaCNGC-2A negatively regulates seed dormancy and pre-harvest sprouting resistance by mediating calcium and hormone signaling in wheat
文献译名:TaCNGC-2A 通过介导钙信号和激素信号负调控小麦种子休眠及穗发芽抗性期刊名称:Nature Communications发表时间:2026年3月27日影响因子:15.7一作单位:安徽农业大学 农学院通讯作者:常成教授、马传喜教授、阮勇凌教授、张海萍教授
通讯邮箱:changtgw@126.com; machuanxi@139.com; yong-ling.ruan@nwafu.edu.cn; zhanghaiping@ahau.edu.cn
项目基金:作者谨此感谢肖世和研究员提供 JH-RILs 和 JW-RILs,以及中国农业科学院作物所夏先春研究员提供 60 份中国地方品种。本研究得到了国家自然科学基金(31871608、32372069);联合基金项目(U20A2033、F2010123002);江苏省现代作物生产协同创新中心(JCIC-MCP)、河北省现代农业产业技术体系(HBCT2023010201)、河南省科技研发联合基金(242301420024)和安徽农业大学创新基金(RC312212)的资助。研究背景
穗发芽(PHS)是指谷物在收获前于穗上提前萌发的现象,严重影响小麦、水稻和玉米等全球重要粮食作物的产量与品质。随着全球气候变化的加剧,该问题发生的频率日益升高,已成为农业生产中的重大挑战。种子休眠(SD)作为抗穗发芽的核心遗传基础,是防止籽粒提前萌发的关键机制。因此,以小麦等重要谷物为研究对象,深入解析控制种子休眠的遗传位点与关键基因,对于培育抗穗发芽的优质作物品种具有极其重要的现实意义。
迄今为止,研究人员已在小麦多条染色体上鉴定出近200个与种子休眠或穗发芽抗性相关的数量性状基因座,但仅有极少数候选基因(如TaMFT-3A、TaMyb10-D、TaPI4K-2A等)被成功克隆与功能验证。尽管这些基因编码转录因子、激酶等多种类型的蛋白,揭示了休眠调控机制的复杂性,但它们直接的上下游分子组件和完整的调控网络仍不清晰。更为关键的是,这些已鉴定基因在实际抗穗发芽育种中的应用潜力尚未得到充分评估,鲜有基因被直接应用于农业生产,形成了从基础分子机制解析到实际育种转化之间的明显研究空白。
当前领域面临的核心挑战在于如何挖掘既能完善休眠调控网络又具备极高实际育种价值的关键基因及其分子组件。本研究成功克隆了小麦种子休眠主效位点Qsd.ahau-2AL的候选基因TaCNGC-2A,揭示了其作为负调控因子在Ca²⁺信号传导及多种植物激素通路中的核心枢纽作用。通过解析转录因子TaMYB-5B和TaMYB-5D的上游靶向抑制机制以及与钙调蛋白TaCaM-3A的下游互作网络,本研究不仅系统阐明了小麦种子休眠与抗穗发芽的全新分子调控机制,还为通过基因组编辑和分子聚合育种培育高抗穗发芽的小麦新品种提供了关键的基因靶点与宝贵的遗传资源。
本研究首次克隆了小麦种子休眠与抗穗发芽主效负调控基因TaCNGC-2A,系统解析了其受上游TaMYB转录因子协同调控、并与下游钙调蛋白TaCaM-3A互作以介导钙信号与多重激素通路的完整调控网络,不仅为禾谷类作物抗穗发芽提供了全新的理论支撑,更通过基因编辑实现了小麦抗逆性与产量的协同提升,展现了巨大的分子设计育种价值。
研究方法
2.1 试验材料与表型鉴定
为了解析控制小麦种子休眠(SD)和抗穗发芽(PHS)的遗传位点及功能基因,本研究利用了多层次的试验材料并在多种环境中开展了表型评估。试验材料包括用于QTL定位的J411与HMC21杂交重组自交系(JH-RILs)及JW-RILs群体、用于关联分析的数百份具有不同休眠水平的自然小麦品种群体,以及用于基因功能验证的EMS诱变突变体(如cngc-2a-jm22等)。此外,利用CRISPR/Cas9基因编辑技术和农杆菌介导的转化方法,在小麦(KN199、AN188、Fielder)和水稻(ZH11)背景下分别创制了TaCNGC-2A、TaCaM-3A等关键基因的敲除突变体、RNAi干扰株系和过表达株系。这些材料被广泛种植于合肥、淮北、宿州等多个田间环境及控温温室中。在表型鉴定方面,通过在严格控制光温湿度的培养皿中进行标准发芽试验,以及对生理成熟麦穗实施人工降雨模拟处理,系统测定了各基因型种子的发芽指数(GI)和发芽率(GP),从而精确量化了其种子休眠强度与穗发芽抗性水平。
2.2 基因克隆、表达分析与分子互作研究
为阐明TaCNGC-2A调控种子休眠的分子机制与调控网络,本研究采用了一系列分子生物学与基因组学研究设计。首先,提取植物组织的基因组DNA和总RNA,结合SLAF-seq和高密度小麦660K SNP阵列技术对主效QTL进行精细定位,并开发了特异性的CAPS和dCAPS分子标记。随后,成功克隆了候选基因TaCNGC-2A的全长及启动子序列,并通过qRT-PCR和转录组测序(RNA-seq)技术全面分析了相关基因在种子吸胀过程中的时空表达模式。在探究上游转录调控机制时,运用酵母单杂交(Y1H)、凝胶电泳迁移率转变(EMSA)、染色质免疫沉淀-定量PCR(ChIP-qPCR)以及双荧光素酶(LUC)报告基因测定等方法,证实了转录因子TaMYB-5B和TaMYB-5D对TaCNGC-2A启动子的直接结合与协同抑制作用。在解析下游蛋白质互作网络时,综合施用酵母双杂交(Y2H)、双分子荧光互补(BiFC)、免疫共沉淀(Co-IP)和体外Pull-down等试验方法,确证了TaCNGC-2A与钙调蛋白TaCaM-3A在细胞内的物理相互作用及其对Ca²⁺浓度的依赖性。
2.3 生理生化测定、统计学分析与数据存储
为了从生理代谢层面验证分子互作带来的生物学效应并确保研究结论的统计学严谨性,本研究实施了严格的生化测定与数据分析流程。在生理生化指标量化方面,利用电感耦合等离子体质谱法(ICP-MS)精准测定了不同基因型种子在吸胀过程中的细胞内Ca²⁺含量变化;同时,采用液相色谱-质谱联用(LC-MS)技术定量分析了脱落酸(ABA)、赤霉素(GA)、茉莉酸(JA)和生长素(AUX)等关键内源植物激素的浓度,并借助商业试剂盒测定了与淀粉降解密切相关的α-淀粉酶活性。在数据处理方面,运用SPSS和Prism等统计软件对所有表型和分子数据进行描述性统计,采用Mann-Whitney U检验等统计学方法评估组间差异,统计显著性均以斜体的p值(如p < 0.05)严格标示。此外,为保障科学研究的透明度与数据的可追溯性,本研究所产出的所有转录组测序(RNA-seq)原始基因组学数据均已按规范上传并存储于NCBI的序列读取归档(SRA)公共数据库中,BioProject登录号为PRJNA1328368。

研究结果
3.1鉴定控制种子休眠的Qsd.ahau-2AL候选基因
精细定位:利用包含重组自交系和极端混池的群体,结合SLAF-seq和660K SNP芯片技术开发分子标记,将Qsd.ahau-2AL精细定位至0.47 Mb区间内,该区间可解释9.4%至10.3%的表型变异。
候选筛选:在该区间注释的7个高置信度基因中,转录组和qRT-PCR分析表明编码环核苷酸门控通道蛋白的TaCNGC-2A在种子中特异性高表达,且在强弱休眠品种间存在显著表达差异,被确定为潜在候选基因。
借助重组自交系群体及高密度遗传图谱,结合SNP芯片技术开发分子标记,成功将控制种子休眠的主效位点Qsd.ahau-2AL精细定位至0.47 Mb的物理区间内。结合转录组测序及基因表达模式分析,发现该区间内编码环核苷酸门控通道蛋白的TaCNGC-2A基因在种子中呈现特异性高表达,且在不同休眠特性的品种间表达量差异显著,由此将其锁定为调控小麦种子休眠的关键候选基因。
3.2 TaCNGC-2A与小麦种子休眠及穗发芽抗性的关联
序列比对:克隆并比对强弱休眠品种的TaCNGC-2A启动子及全长序列,发现存在多个多态性位点。
变异分析:针对启动子区和编码区的四个关键突变位点开发CAPS标记并在多群体中进行基因型鉴定,发现启动子区-312 bp处的T/A突变是决定休眠和抗性表型差异的关键变异,携带A等位基因的品种表现出更强的休眠特性。
通过对不同休眠特性小麦品种的TaCNGC-2A基因序列进行克隆与比对,揭示了启动子及编码区存在多个多态性位点。进一步利用开发的分子标记在多个自然及遗传群体中进行关联分析,明确了启动子区-312 bp处的T/A单核苷酸多态性是决定种子休眠及穗发芽抗性表型差异的关键变异位点,其中A等位基因与更强的种子休眠及穗发芽抗性显著相关。
3.3 TaCNGC-2A负向调控小麦种子休眠与穗发芽抗性
功能验证:利用EMS突变体、CRISPR/Cas9基因编辑敲除系及过表达系进行表型鉴定,证实TaCNGC-2A功能丧失可显著提升种子休眠与穗发芽抗性,而过表达则导致抗性降低。
育种潜力:将基因编辑敲除系与现代栽培品种杂交或直接在现代品种中进行敲除,均能有效提升后代的穗发芽抗性,且田间试验表明该基因敲除不会对株高、分蘖、穗部结构及产量相关农艺性状产生负面影响。
为深入探究TaCNGC-2A的生物学功能,综合运用EMS突变体、CRISPR/Cas9多靶点基因编辑以及转基因过表达技术,在温室与多地田间环境下进行了系统的表型验证。结果表明,TaCNGC-2A的功能缺失能够显著增强小麦种子的休眠特性并提高穗发芽抗性,而其同源基因TaCNGC-2B和TaCNGC-2D对休眠无显著影响。此外,将该基因的敲除突变引入现代高产小麦品种中,可在不影响产量及其他关键农艺性状的前提下大幅提升其穗发芽抗性,凸显了该基因在抗穗发芽分子育种中的重要应用价值。(Fig.1)
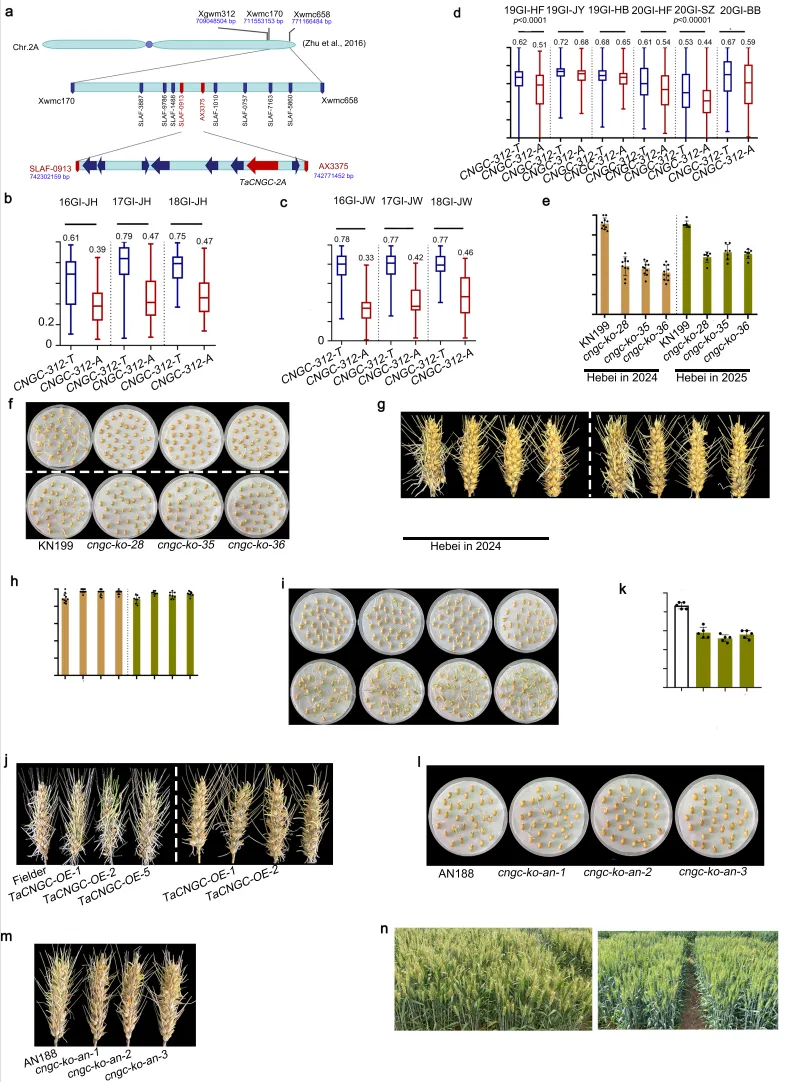
图1. 控制种子休眠的Qsd.ahau-2AL候选基因TaCNGC-2A的鉴定及其在小麦种子休眠和穗发芽抗性中的作用。 a Qsd.ahau-2AL被缩小至包含8个基因的0.47 Mb区间内。b-d 在JH-RILs、JW-RILs和431WVs群体中,携带CNGC-312-T和CNGC-312-A的品系间发芽指数(GI)存在显著差异。箱线图显示中位数(中心线)、四分位距(箱体边界)以及最小至最大值(触须)。平均值标注在每个箱体上方。(b)CNGC-312-T和CNGC-312-A的生物学独立植株数分别为n = 101和52。**** p < 0.0001(双尾Student's t检验)。(c)CNGC-312-T和CNGC-312-A的生物学独立植株数分别为n = 112和53。**** p < 0.0001(双尾Student's t检验)。(d)CNGC-312-T和CNGC-312-A的生物学独立植株数分别为n = 276和136。** p < 0.01,*** p < 0.001,**** p < 0.0001(双尾Student's t检验)。e-g 在河北省大田(2024年和2025年)收获的TaCNGC Cas9编辑品系和野生型KN199的发芽率及表型。种子和麦穗吸胀3天。(e)种子发芽率。数据以均值±标准差表示(河北取样的生物学独立植株数:2024年n = 10;2025年n = 7)。**** p < 0.0001(双尾Student's t检验)。(f)种子发芽表型。(g)穗发芽表型。h-j 在温室(2024年)和河北省大田(2025年)收获的TaCNGC-2A过表达品系和野生型Fielder的发芽率及表型。种子和麦穗吸胀3天。(h)种子发芽率。数据以均值±标准差表示(温室和河北取样的生物学独立植株数:温室n = 10;河北n = 8)。* p < 0.05,** p < 0.01,*** p < 0.001(双尾Student's t检验)。k-m 在温室(2025年)收获的TaCNGC Cas9编辑品系和野生型AN188的发芽率及表型。种子和麦穗吸胀3天。(k)种子发芽率。数据以均值±标准差表示(n = 5个生物学独立植株)。**** p < 0.0001(双尾Student's t检验)。n TaCNGC Cas9编辑品系和野生型KN199在河北省大田(2024年和2025年)的照片。源数据作为源数据文件提供。
3.4 TaCNGC-2A直系同源基因在水稻中发挥类似负调控作用
跨物种验证:在水稻中过表达TaCNGC-2A并利用基因编辑敲除其直系同源基因OsCNGC6,发现过表达系发芽率升高,而敲除系发芽率显著降低。
为了验证TaCNGC-2A在禾本科作物中的功能保守性,在水稻中进行了异源过表达及同源基因OsCNGC6的靶向敲除实验。表型分析证实,TaCNGC-2A同样能够打破水稻种子的休眠并降低其穗发芽抗性,且水稻同源基因OsCNGC6发挥着与小麦中高度相似的负向调控作用,表明该调控机制在禾谷类作物中具有保守性。
3.5 TaMYB-5B与TaMYB-5D直接结合并协同抑制TaCNGC-2A表达
上游互作:酵母单杂交、LUC报告基因及EMSA实验证实,转录因子TaMYB-5B和TaMYB-5D能够直接结合TaCNGC-2A启动子区的关键突变位点。
协同抑制:蛋白互作及共表达分析表明,TaMYB-5B与TaMYB-5D存在物理互作,并协同抑制TaCNGC-2A的转录,且对携带A等位基因的启动子抑制作用更强。
表型调控:过表达TaMYB-5B和TaMYB-5D可显著增强种子休眠,而共表达TaCNGC-2A可部分恢复该表型,证实两者作为上游调控因子通过抑制TaCNGC-2A发挥作用。
针对TaCNGC-2A启动子区关键突变位点的上游调控机制解析表明,转录因子TaMYB-5B和TaMYB-5D能够直接结合该区域。通过体内外互作及转录活性分析证实,这两种MYB转录因子不仅存在直接的物理互作,还能协同抑制TaCNGC-2A的转录表达,且这种抑制效应在携带A等位基因的强休眠材料中更为显著。遗传学证据进一步表明,过表达TaMYB-5B或TaMYB-5D均能显著提升小麦种子的休眠水平,而TaCNGC-2A的引入可部分逆转这一表型,从而确立了TaMYB-5B/5D作为上游负调控因子通过抑制TaCNGC-2A表达来增强穗发芽抗性的分子调控网络。(Fig.2)(Fig.3)
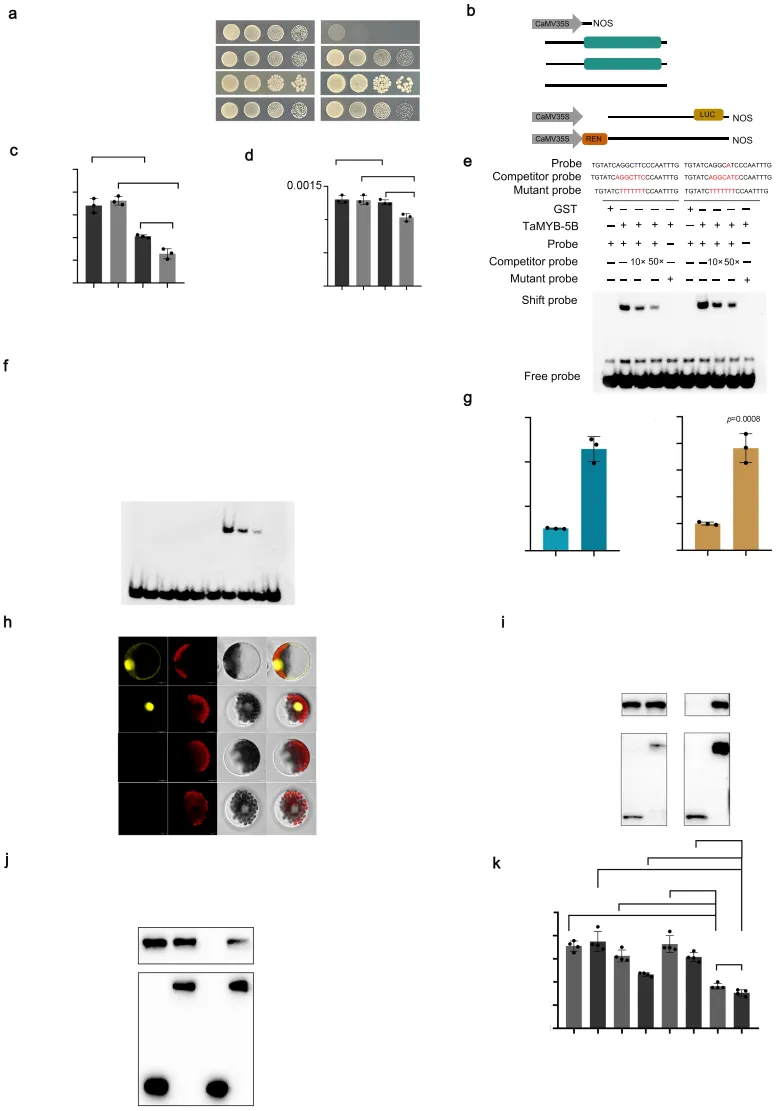
图2. MYB转录因子TaMYB-5B和TaMYB-5D直接结合TaCNGC-2A启动子并协同抑制其表达。 a 在酵母单杂交实验中,TaMYB-5B、TaMYB-5D和TaB3-4D与TaCNGC-2A-312A片段(包含-312 bp处A位点前后各10 bp)相互作用。b 双荧光素酶报告基因实验载体构建示意图。c 在LUC活性测定中,TaMYB-5B结合CNGC-312-T(906 bp启动子,-312 bp为T)和CNGC-312-A(906 bp启动子,-312 bp为A)启动子。数据以均值±标准差表示(n = 3次生物学独立实验)。** p < 0.01 且 *** p < 0.001(双尾Student's t检验)。d 在LUC活性测定中,TaMYB-5D结合CNGC-312-A启动子。数据以均值±标准差表示(n = 3次生物学独立实验)。** p < 0.01,ns表示不显著(双尾Student's t检验)。e 在EMSA实验中,TaMYB-5B结合TaCNGC-2A-312T(包含-312 bp处T位点前后各10 bp)和TaCNGC-2A-312A片段。该实验重复3次,结果相似。f 在EMSA实验中,TaMYB-5D结合TaCNGC-2A-312A片段。该实验重复3次,结果相似。g ChIP-qPCR实验证实TaMYB-5B和TaMYB-5D在体内结合TaCNGC-2A的启动子。使用抗FLAG抗体在TaMYB-5B-OE-2和TaMYB-5D-OE-6幼苗中进行免疫沉淀。数据以均值±标准差表示(n = 3次生物学独立实验)。*** p < 0.001(双尾Student's t检验)。h-j 在BiFC、Co-IP和GST pull-down实验中TaMYB-5B和TaMYB-5D之间的相互作用。i和j中的实验重复3次,结果相似。k 在LUC活性测定中,TaMYB-5B和TaMYB-5D协同抑制CNGC-312-T和CNGC-312-A的转录。数据以均值±标准差表示(n = 4次生物学独立实验)。* p < 0.05 且 **** p < 0.0001(双尾Student's t检验)。源数据作为源数据文件提供。
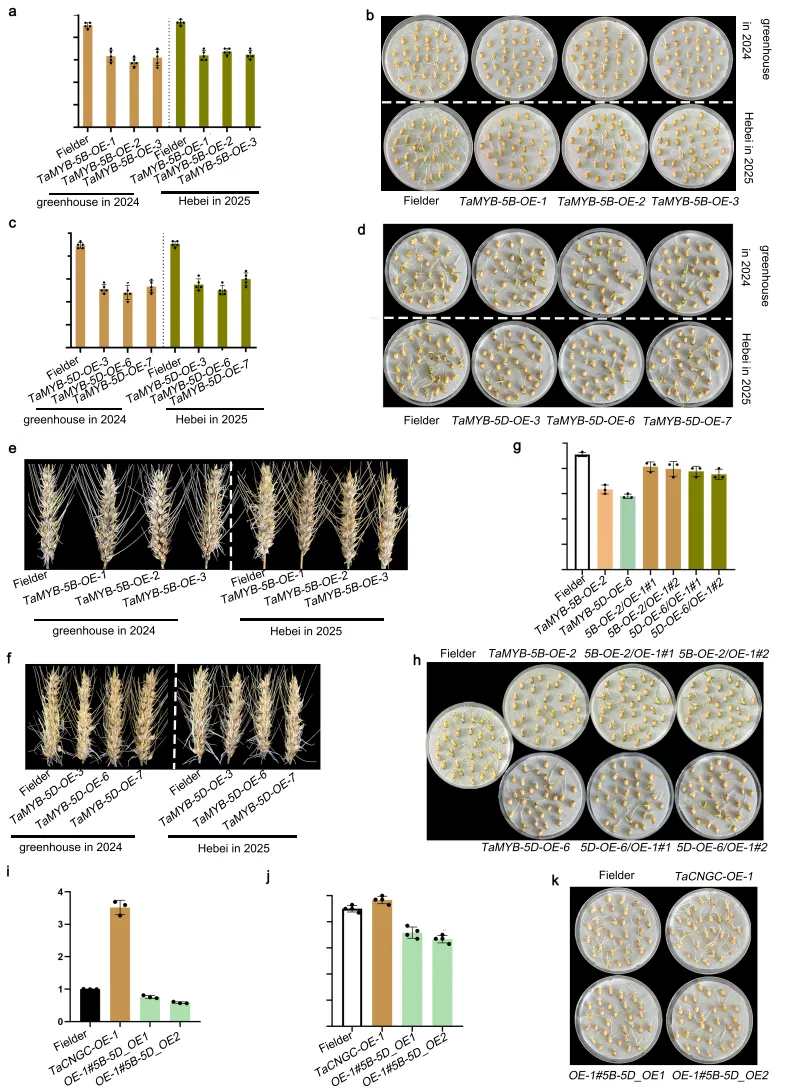
图3. TaMYB-5B和TaMYB-5D在小麦种子休眠和穗发芽抗性中的作用。 a, b 在温室(2024年)和河北省大田(2025年)收获的TaMYB-5B过表达品系和野生型Fielder的发芽率及表型。种子吸胀3天。(a)种子发芽率。数据以均值±标准差表示(n = 5个生物学独立植株)。**** p < 0.0001(双尾Student's t检验)。c, d 在温室(2024年)和河北省大田(2025年)收获的TaMYB-5D过表达品系和野生型Fielder的发芽率及表型。种子吸胀3天。(c)种子发芽率。数据以均值±标准差表示(n = 5个生物学独立植株)。**** p < 0.0001(双尾Student's t检验)。e, f 在温室(2024年)和河北省大田(2025年)收获的TaMYB-5B和TaMYB-5D过表达品系及野生型Fielder的穗发芽图像。麦穗吸胀3天。g, h 5B-OE-2/OE-1#1/2、5D-OE-6/OE-1#1/2、TaMYB-5B-OE-2、TaMYB-5D-OE-6和野生型Fielder的发芽率及表型。种子吸胀3天。(g)种子发芽率。数据以均值±标准差表示(n = 3个生物学独立植株)。* p < 0.05,** p < 0.01,*** p < 0.001,且 **** p < 0.0001(双尾Student's t检验)。i TaCNGC-2A在过表达品系TaCNGC-OE-1以及双过表达品系OE-1#5B-5D_OE1和OE-1#5B-5D_OE2中的表达分析。数据以均值±标准差表示(n = 3次生物学独立实验)。*** p < 0.0001(双尾Student's t检验)。j, k OE-1#5B-5D_OE1、OE-1#5B-5D_OE2、TaCNGC-OE-1和Fielder的发芽率及表型。种子吸胀3天。(j)种子发芽率。数据以均值±标准差表示(n = 4个生物学独立植株)。* p < 0.05 且 **** p < 0.0001(双尾Student's t检验)。源数据作为源数据文件提供。
3.6 钙调蛋白TaCaM-3A与TaCNGC-2A发生互作
蛋白筛选:结合序列比对与转录组数据分析,筛选出多个可能与TaCNGC-2A互作的钙调蛋白,其中TaCaM-3A表现出最强的互作信号。
互作验证:酵母双杂交、BiFC及Co-IP等实验证实TaCNGC-2A与TaCaM-3A在内质网和细胞质中发生物理互作,且该互作具有Ca²⁺依赖性。
结构域鉴定:截短突变分析明确了TaCaM-3A的四个EF手结构域作为一个整体与TaCNGC-2A的IQ结构域特异性结合。
基于CNGC蛋白的结构特征及同源性分析,筛选并鉴定出小麦钙调蛋白TaCaM-3A为TaCNGC-2A的互作蛋白。多重体内外蛋白互作实验不仅证实了两者在内质网及细胞质中的物理结合,还揭示了这种互作高度依赖于Ca²⁺浓度。进一步的结构域截短与定点突变分析精准定位了互作的核心区域,即TaCaM-3A完整的四个EF手结构域与TaCNGC-2A的IQ基序发生特异性结合,为解析Ca²⁺信号传导机制提供了生化基础。(Fig.4)
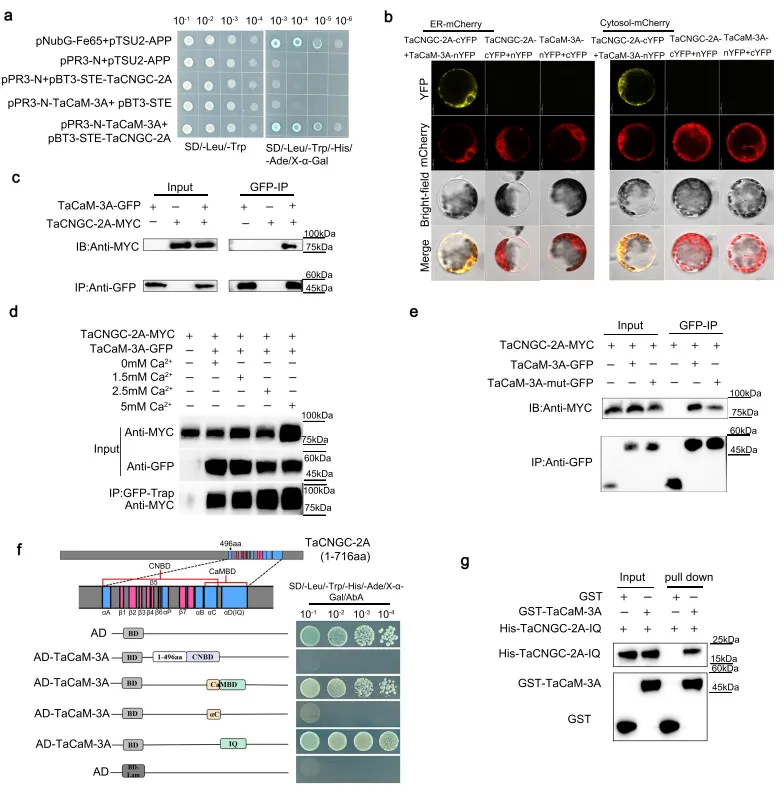
图4. TaCNGC-2A与TaCaM-3A相互作用。 a-c 在Y2H、BiFC和Co-IP实验中TaCNGC-2A与TaCaM-3A的相互作用。d 1.5 mM、2.5 mM和5 mM的钙处理增强了TaCNGC-2A与TaCaM-3A之间的相互作用。e TaCNGC-2A与TaCaM-3A及TaCaM-3A-mut相互作用的Co-IP实验。f, g 在Y2H和GST pull-down实验中IQ结构域与TaCaM-3A的相互作用。所有实验均独立重复3次,结果相似。源数据作为源数据文件提供。
3.7 TaCaM-3A负向调控小麦种子休眠与穗发芽抗性
表型鉴定:EMS突变体、基因编辑敲除系及RNAi干扰系均表现出种子休眠增强,而过表达系则导致休眠减弱。
遗传上位:杂交聚合分析表明,TaCaM-3A过表达可挽救TaCNGC-2A敲除突变体的发芽缺陷,证实其位于TaCNGC-2A下游发挥作用。
农艺性状:田间试验显示,敲除TaCaM-3A不仅能提升穗发芽抗性,还能显著增加粒长和千粒重,从而提高单株产量。
针对互作蛋白TaCaM-3A的功能解析表明,其在小麦种子休眠中发挥着与TaCNGC-2A相似的负调控作用。通过创制多种遗传材料进行表型评估,证实TaCaM-3A的功能缺失能显著增强穗发芽抗性。遗传上位性分析进一步明确了TaCaM-3A作为下游信号分子介导了TaCNGC-2A的调控通路。尤为重要的是,大田农艺性状考察发现,靶向敲除TaCaM-3A不仅有效改善了穗发芽抗性,还通过增加粒长和千粒重实现了单株产量的显著提升,展现出极高的协同改良育种价值。(Fig.5)
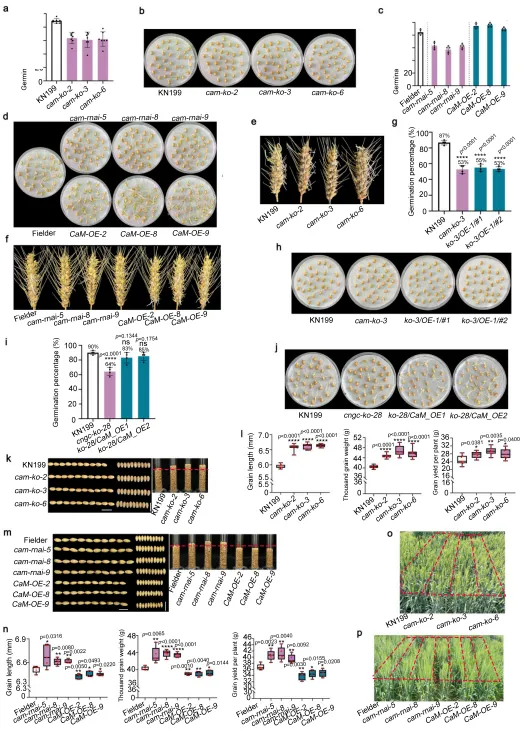
图5. TaCaM-3A在小麦种子休眠中的作用。 a, b 在河北(2025年)收获的TaCaM Cas9编辑品系和野生型KN199的发芽率及表型。种子吸胀3天。(a)种子发芽率。数据以均值±标准差表示(n = 7个生物学独立植株)。**** p < 0.0001(双尾Student's t检验)。c, d 在河北(2025年)收获的TaCaM RNAi品系、TaCaM-3A过表达品系和野生型Fielder的发芽率及表型。种子吸胀3天。(c)种子发芽率。数据以均值±标准差表示(n = 5个生物学独立植株)。* p < 0.05,** p < 0.01,*** p < 0.001,且 **** p < 0.0001(双尾Student's t检验)。e, f 在河北省大田(2025年)收获的TaCaM Cas9编辑和RNAi品系、TaCaM-3A过表达品系以及野生型KN199和Fielder的穗发芽图像。麦穗吸胀3天。g, h 在温室(2025年)收获的ko-3/OE-1#1/2、cam-ko-3和KN199的发芽率及表型。种子吸胀3天。(g)种子发芽率。数据以均值±标准差表示(n = 4个生物学独立植株)。**** p < 0.0001(双尾Student's t检验)。i, j 在温室(2025年)收获的ko-28/CaM_OE1/2、cngc-ko-28和KN199的发芽率及表型。种子吸胀3天。(i)种子发芽率。数据以均值±标准差表示(n = 4个生物学独立植株)。ns表示不显著,**** p < 0.0001(双尾Student's t检验)。k-n TaCaM Cas9编辑和RNAi品系、TaCaM-3A过表达品系以及野生型KN199和Fielder的粒长、千粒重和单株产量。每个量筒内放置500粒小麦种子。箱线图显示中位数(中心线)、四分位距(箱体边界)以及最小至最大值(触须)。(l)数据以均值±标准差表示(n = 7个生物学独立植株)。* p < 0.05,** p < 0.01,且 **** p < 0.0001(双尾Student's t检验)。(n)数据以均值±标准差表示(n = 5个生物学独立植株)。* p < 0.05,** p < 0.01,且 **** p < 0.0001(双尾Student's t检验)。o, p TaCaM Cas9编辑和RNAi品系、TaCaM-3A过表达品系以及野生型KN199和Fielder在河北省大田(2025年)的照片。比例尺 = 1 cm。源数据作为源数据文件提供。
3.8 TaCNGC-2A介导种子休眠与穗发芽抗性的通路
钙离子信号:转录组及ICP-MS分析显示,敲除TaCNGC-2A显著降低了种子内的Ca²⁺含量,并改变了钙离子结合通路相关基因的表达。
激素代谢:敲除突变体中促进生长的激素(GA、AUX)含量及α-淀粉酶活性下降,而抑制生长的激素(ABA、JA)含量升高。
休眠基因:多种已知休眠相关基因的表达模式在TaCNGC-2A敲除和过表达材料中发生显著改变,表明其参与复杂的调控网络。
为全面解析TaCNGC-2A介导的分子网络,通过比较转录组学、离子组学及激素靶向代谢组学分析,揭示了其多维度的调控机制。研究发现,TaCNGC-2A的缺失不仅直接导致胞内Ca²⁺浓度下降及钙信号传导通路基因表达重塑,还引发了植物激素代谢网络的系统性改变,表现为赤霉素和生长素等促生激素减少,而脱落酸和茉莉酸等抑制性激素积累。此外,众多已知休眠关键基因的表达亦受到显著调控,表明TaCNGC-2A通过整合钙信号、多重植物激素通路及下游休眠基因网络,协同调控小麦种子的休眠状态。
3.9 TaCNGC-2A的自然变异与等位基因频率分析
多态性评估:在213份不同遗传背景的小麦种质中鉴定出多个多态性位点,确认启动子区-312 bp处的T/A突变为决定表型差异的唯一关键变异。
频率分布:携带强休眠A等位基因的材料约占一半,且在地方品种中的分布频率高于现代育成品种,提示其在抗性育种中具有重要挖掘潜力。
通过对包含广泛遗传多样性的小麦自然群体进行TaCNGC-2A基因测序与单倍型分析,全面评估了该基因的自然变异情况。关联分析再次确证了启动子区-312 bp处的T/A单核苷酸多态性是驱动种子休眠特性分化的核心变异。群体遗传学统计显示,赋予强穗发芽抗性的优异A等位基因在地方品种中富集,而在现代改良品种中频率相对较低,这不仅反映了育种选择的历史轨迹,也突显了该优异等位基因在未来现代小麦抗逆分子育种中的巨大应用空间。(Fig.6)
3.10 TaCNGC-2A与已知休眠基因聚合对穗发芽抗性的影响
基因聚合:评估了TaCNGC-2A抗性等位基因与六个已知休眠相关基因的聚合效应,鉴定出58种组合类型。
累加效应:表型分析揭示了六种具有极低发芽指数的优异等位基因组合,且发芽指数与抗性等位基因的数量呈显著负相关,表现出明显的累加效应。
为探索TaCNGC-2A在分子标记辅助育种中的实际效用,系统评估了其优异等位基因与六个已知休眠相关基因(TaMFT-3A、TaVp-1、TaMyb10-D、TaMKK3-A、TaQsd1-5B和TaPI4K-2A)抗性等位基因的聚合效应。通过对177份小麦种质进行基因型鉴定,共发现58种等位基因组合类型。表型关联分析不仅筛选出6种具有极低发芽指数的优异多基因聚合组合,还揭示了发芽指数与抗性等位基因数量之间存在显著的负相关关系,充分证明了将TaCNGC-2A抗性等位基因与其他休眠基因进行金字塔式聚合,能够产生显著的累加效应,从而更大幅度地提升小麦的种子休眠水平与穗发芽抗性。(Fig.6)
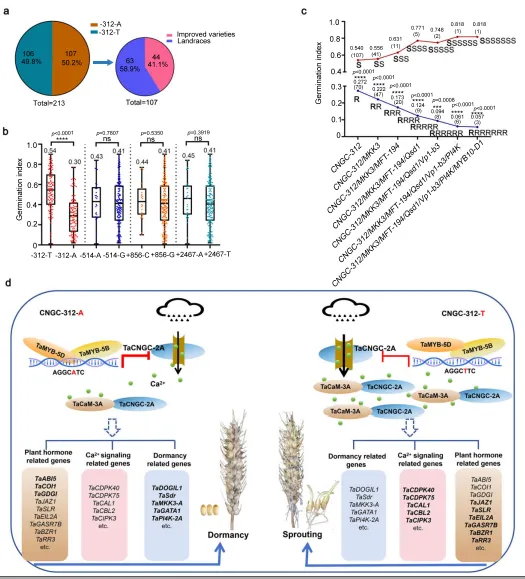
图6. TaCNGC-2A等位基因频率分析、TaCNGC-2A与已知休眠基因聚合对种子休眠的影响以及TaCNGC-2A调控小麦种子休眠与穗发芽抗性的假设工作模型。 a 在213份小麦种质中,携带与强种子休眠/穗发芽抗性相关的-312-A等位基因和与弱种子休眠/穗发芽抗性相关的-312-T等位基因的种质比例,以及携带-312-A的改良品种和地方品种的比例。b 携带-312-A和-312-T、-514-A和-514-G、+856-C和+856-G以及+2467-A和+2467-T的小麦基因型之间在种子休眠上的表型差异。箱线图显示中位数(中心线)、四分位距(箱体边界)以及最小至最大值(触须)。平均值标注在每个箱体上方。-312-T、-312-A、-514-A、-514-G、+856-C、+856-G、+2467-A和+2467-T的生物学独立植株数分别为n = 106、107、32、181、28、185、31和182。ns表示不显著,****P < 0.0001(双尾Student's t检验)。c TaCNGC-2A的R等位基因与六个已知休眠基因的R等位基因聚合对种子休眠的影响。R和S分别表示强休眠和弱休眠等位基因。*** p< 0.001 且 **** p< 0.0001(双尾Student's t检验)。d 在降雨刺激后,上游转录因子TaMYB-5B和TaMYB-5D结合到TaCNGC-2A启动子上并协同调控其表达。与CNGC-312-T相比,它们显著抑制了CNGC-312-A的转录,导致Ca²⁺通道受阻,减少了Ca²⁺从内质网向细胞质的流动,从而减弱了TaCNGC-2A与TaCaM-3A之间的相互作用。结果,参与ABA、JA和AUX通路的基因以及已知休眠基因的表达水平上调,而参与Ca²⁺、JA、AUX、ETH、GA和CTK通路的基因表达水平下调,最终增强了小麦的种子休眠和穗发芽抗性。以粗体标记的基因表明其在cngc-ko-28中表达水平上调,未以粗体突出的基因表明其表达水平下调。源数据作为源数据文件提供。
研究创新性
首次克隆抗穗发芽新基因:成功精细定位并克隆了控制小麦种子休眠的主效QTL候选基因TaCNGC-2A,首次揭示了环核苷酸门控通道(CNGC)蛋白在禾本科作物(小麦和水稻)中作为种子休眠和穗发芽抗性负调控因子的保守生物学功能,极大地丰富了作物抗穗发芽的基因资源库。
阐明上游协同转录调控机制:精准鉴定出TaCNGC-2A启动子区决定休眠表型差异的关键自然变异位点(-312 bp处的T/A单核苷酸多态性),并创新性地发现转录因子TaMYB-5B和TaMYB-5D能够直接结合该位点并发生物理互作,从而协同抑制TaCNGC-2A的转录表达。这一发现为理解优异等位基因(-312-A)如何赋予强休眠特性提供了清晰的分子机制。
揭示下游钙信号与激素互作网络:明确了TaCNGC-2A的IQ结构域与钙调蛋白TaCaM-3A的四个EF手结构域发生Ca²⁺依赖性物理互作的生化机制。研究证实该互作网络将内质网到细胞质的Ca²⁺流与多种植物激素(ABA、GA、JA、AUX等)信号转导途径及已知休眠基因网络紧密联系,系统解析了由离子通道介导的种子休眠复杂分子调控通路。
展现卓越的抗性与产量协同改良潜力:证实了通过CRISPR/Cas9技术靶向敲除TaCNGC-2A或TaCaM-3A能够显著提升现代高产小麦品种的穗发芽抗性。尤为重要的是,敲除TaCaM-3A不仅未造成产量惩罚,反而显著增加了粒长、千粒重和单株产量,实现了抗逆性与产量的协同提升。此外,明确了TaCNGC-2A优异等位基因与已知休眠基因聚合具有显著的累加效应,为小麦抗穗发芽分子设计育种提供了极具应用价值的靶点与策略。

审核|林蘖亙
阅读科研文献,荟萃前沿进展
欢迎关注、转发、投稿、点赞
