最新高产!江苏大学副院长&农业农村部神农青年英才Green Chem-全细胞级联创纪录:工程大肠杆菌高效合成瑞鲍迪苷M与副产物果糖升级
- 2026-05-28 09:44:32
(点击页面左下角阅读原文,直达文献页面)
一、中文标题
高效全细胞平台用于瑞鲍迪苷M生物转化:级联设计、表达调控与过程工程(An efficient whole-cell platform for Rebaudioside M biotransformation: cascade design, expression regulation, process engineering)
二、发表单位及通讯作者
发表单位:江苏大学通讯作者:Cunshan Zhou(周存山)
三、科学问题
如何通过构建大肠杆菌全细胞催化体系,整合级联酶反应、基因表达调控与过程工程策略,实现瑞鲍迪苷M的高效生物合成,并解决辅因子成本高、副产物浪费等关键瓶颈?
四、发表时间
时间:2025年12月29日
链接:DOI https://doi.org/10.1039/D5GC04865F

五、摘要
本研究首次构建了一个集成的大肠杆菌全细胞级联系统,共表达工程化UGT76G1变体和大豆蔗糖合酶(GmSuSy),利用蔗糖实现UDP-葡萄糖原位再生,驱动Reb-D向Reb-M转化。通过多拷贝整合、RBS工程、培养基和诱导条件优化,以及细胞透性化处理和反应条件优化,克服了过程瓶颈。采用补料分批策略,最终在200 mL体系中获得30.6 g/L Reb-M,转化率95.9%,为目前报道的最高水平之一。此外,首次将副产物果糖通过D-塔格糖3-差向异构酶模块转化为高附加值D-阿洛酮糖(2.97 g/L),提高了原子经济性和可持续性。该研究为绿色、经济的Reb-M工业化生产提供了新平台。
六、研究背景
过量糖摄入引发的肥胖、糖尿病等慢性代谢疾病已成为全球性健康危机,推动了对零热量、可持续甜味剂的需求。瑞鲍迪苷M(Reb-M)作为来自甜叶菊的高强度甜味剂,具有蔗糖般纯净口感且无苦后味,甜度约为蔗糖的200–350倍,并兼具多种生物活性,是极具潜力的代糖产品。然而,其工业化生产面临严峻挑战:植物提取法受限于甜叶菊生长周期长、叶片中Reb-M含量极低(<0.1%干重),且提取工艺复杂,经济性差;化学合成法缺乏立体选择性,难以应用。因此,利用合成生物学构建微生物细胞工厂成为可持续替代路径。
近年来,研究者尝试在大肠杆菌或酵母中从头合成Reb-M前体,但产量仅为毫克/升级,远未达到工业要求。相较而言,以相对丰富的糖苷(如Reb-D)为底物,通过糖基转移酶(UGT)进行体外酶法或全细胞转化更具可行性。其中,UGT76G1可催化UDP-葡萄糖(UDP-Glc)向Reb-D的C3-羟基转移生成Reb-M。然而,该路线仍存在四大瓶颈:①植物源UGT76G1在微生物中表达易形成包涵体,可溶性差;②UDP-Glc作为昂贵辅因子,需经济高效的再生体系;③现有研究多集中于酶工程改造,对整体过程优化关注不足;④糖基化反应中会释放等摩尔的果糖副产物,传统工艺未加利用,造成原子浪费。
针对上述问题,本研究拟建立大肠杆菌全细胞催化平台,通过共表达工程化UGT76G1和蔗糖合酶(SuSy),实现UDP-Glc从蔗糖的原位再生,并系统优化基因表达、培养条件、反应参数及补料策略,最终实现Reb-M的高效合成,同时引入副产物果糖高值化模块,提升过程绿色性与经济性。
七、研究结果
结果1、全细胞平台的构建与验证
研究选用结构指导改造的UGT76G1变体(T284S/M88L/L200A),其活性较野生型提高2.38倍。通过比较多种来源的蔗糖合酶,确定大豆来源的GmSuSy具有高可溶性表达、优良催化活性及与UGT76G1匹配的pH/温度耐受范围。将两者构建至pRSFDuet-1质粒,转化大肠杆菌BL21(DE3)获得菌株BL0。SDS-PAGE确认两蛋白成功表达(53.6 kDa和92.5 kDa),HPLC检测到Reb-M生成,证明级联系统功能完整。
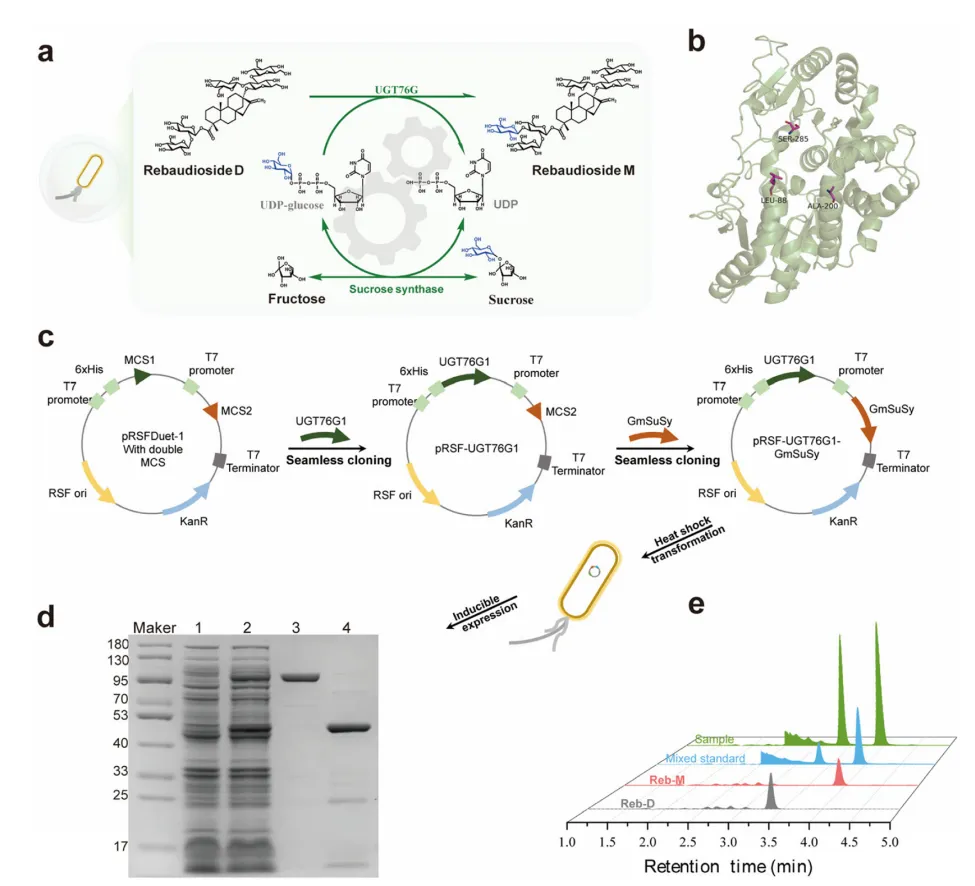
图1 全细胞转化平台
结果2、UGT76G1多拷贝工程提升表达量
粗酶液补充实验显示UGT76G1为限速步骤,因此通过增加UGT76G1基因拷贝数构建菌株BL1(2:1)和BL2(3:1)。随着拷贝数增加,UGT76G1可溶性表达分别提高17%和41%,酶活从45 U/g升至92 U/g,Reb-D转化率从42.55%升至73.63%。但GmSuSy表达因资源竞争下降,提示需平衡两酶表达。
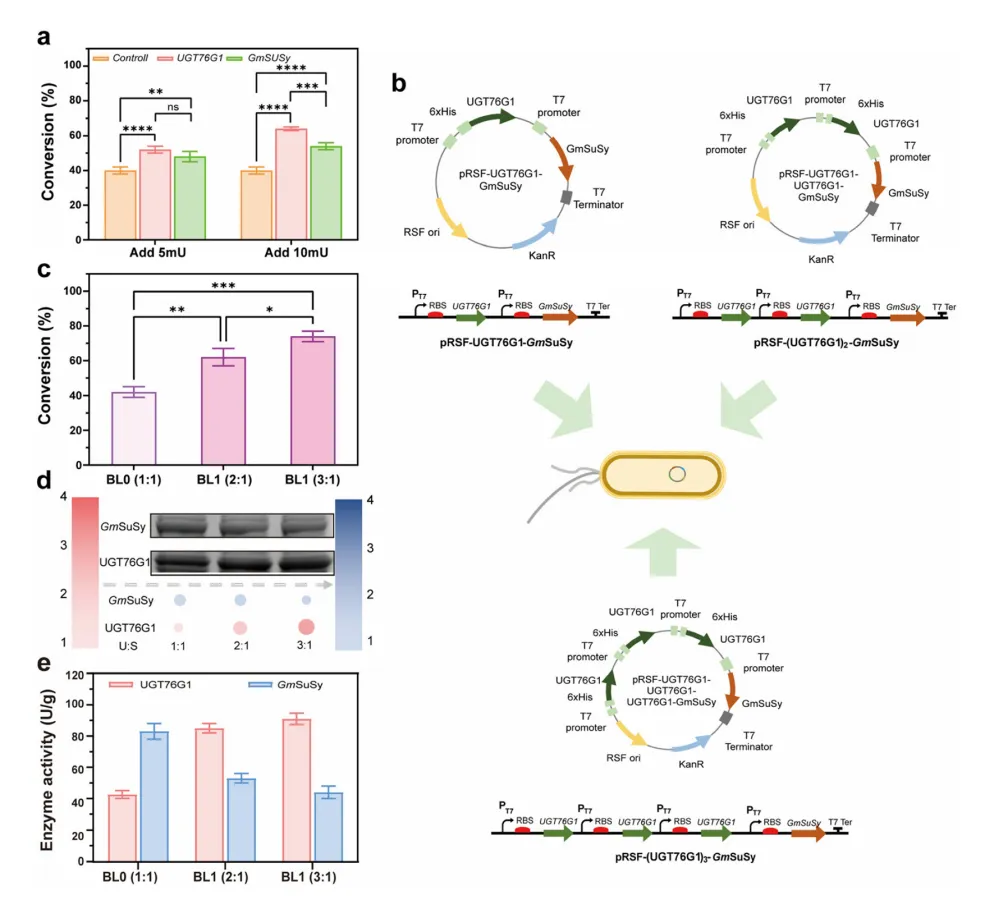
图2 多拷贝优化
结果3、RBS工程精细调控GmSuSy表达
为恢复GmSuSy水平,替换其核糖体结合位点(RBS)为7种不同强度的合成序列,获得菌株BL3–BL9。UGT76G1活性保持稳定(80–95 U/g),GmSuSy活性随RBS强度变化(28–78 U/g)。当两酶活性接近1:1时(BL7,RBS BBa_B0034),转化率最高达85%,较对照提高20%。RBS工程实现了翻译水平的定量调控,优化了级联平衡。
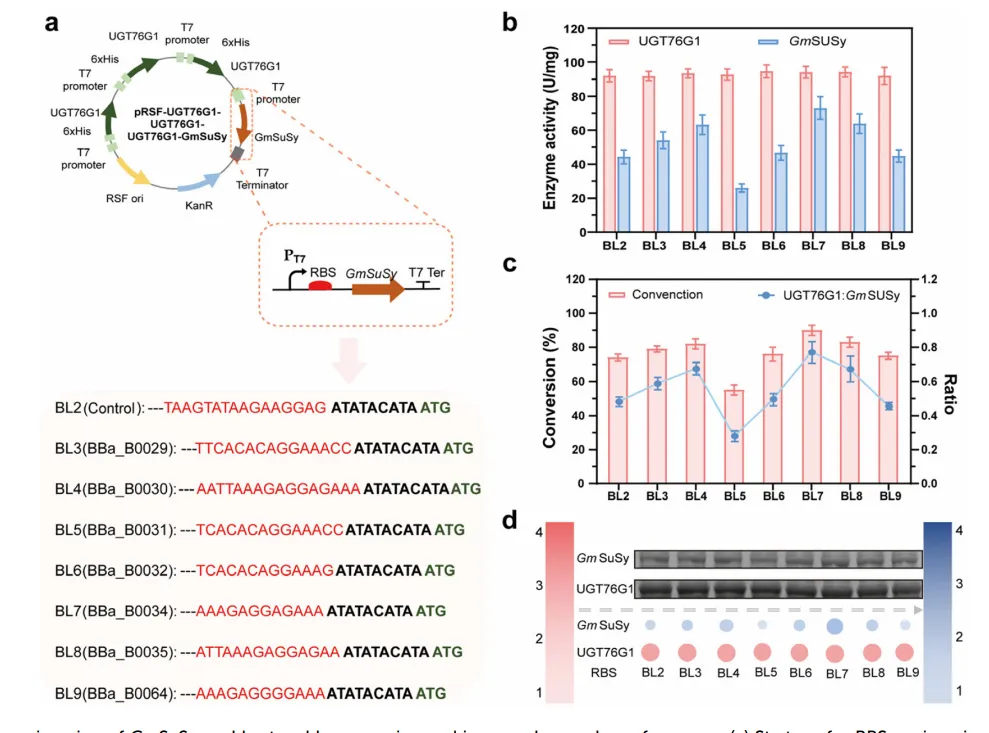
图3 RBS优化
结果4、培养与诱导条件优化提高可溶性表达
比较6种培养基,TB培养基使Reb-M产量最高(219.55 mg/L),较LB提高4.45倍,且UGT76G1可溶性表达增加,包涵体减少。优化诱导条件:0.4 mM IPTG、16°C诱导18 h,获得最佳生物量与酶活,Reb-M产量达160 mg/L。
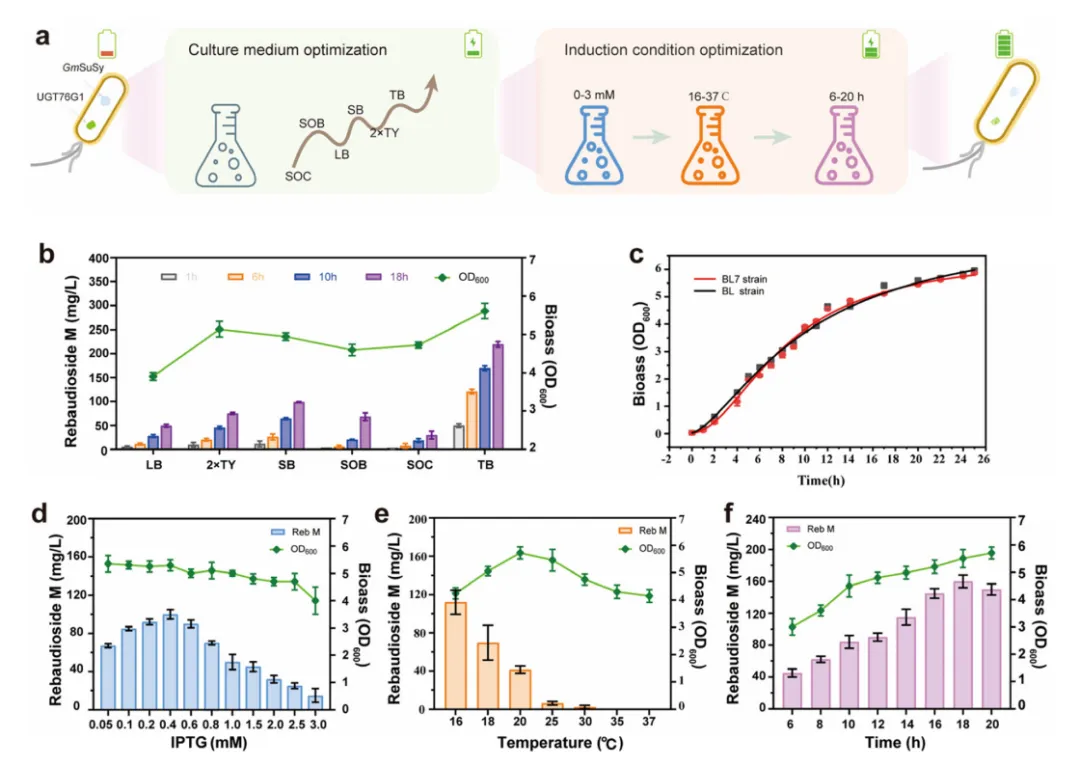
图4 优化培养条件
结果5、细胞透性化处理增强底物传输
针对全细胞催化中膜传质限制,筛选多种透性化试剂。1%二甲苯处理效果最佳,Reb-M产量从2.53 mg/L升至156.86 mg/L,随后活性因细胞裂解下降。确定1%二甲苯为最优浓度,兼顾通透性与细胞完整性。
结果6、反应环境优化
优化温度、pH、金属离子等参数:40°C时活性最高(165.98 mg/L),归因于工程酶热稳定性提升;最适pH 7.5(PBS缓冲),与GmSuSy活性窗口一致;Mn²⁺显著激活反应,6 mM时产量达189.67 mg/L。
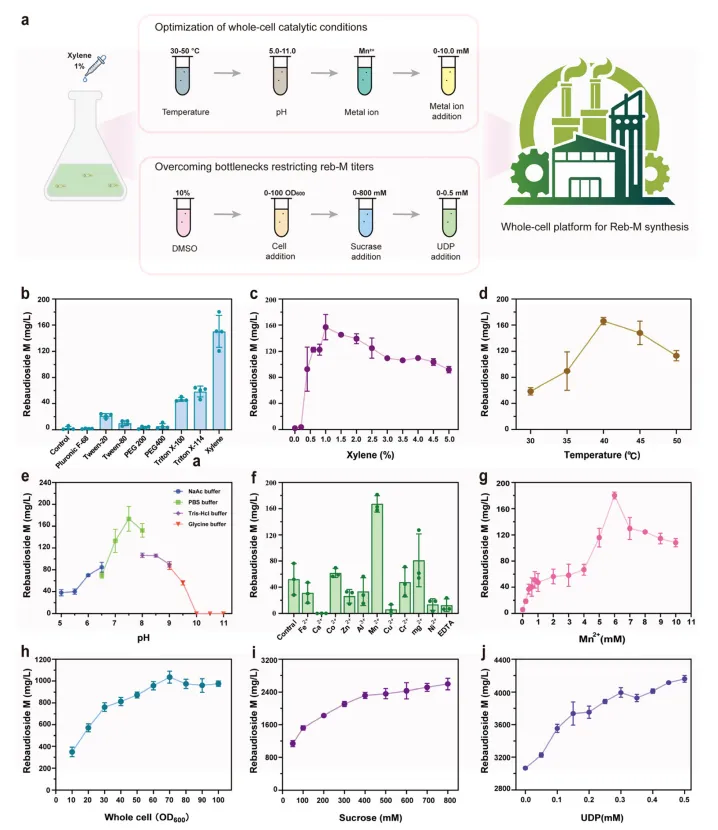
图5 通透性和反应环境优化
结果7、过程瓶颈识别与释放
底物溶解度:添加10% DMSO可维持4 mM Reb-D溶解>2 h,无显著细胞毒性。细胞密度:OD600=70时产量最高(258.83 mg/L)。蔗糖浓度:600 mM时达2426.6 mg/L,兼顾产量与细胞稳定性。UDP添加:0.5 mM UDP使产量提高1.35倍至4158.7 mg/L,但增量边际递减。
结果8、催化剂重复使用性
BL7菌株在优化条件下循环使用6次,前3次活性保持>85%,6次后仍保留34%,显示良好操作稳定性。
结果9、补料分批放大生产
在200 mL摇瓶中进行补料分批转化,每1 h补加Reb-D至4 mM,连续6轮。10 h后Reb-M产量达30.56 g/L,总转化率95.88%,时空产率3056 mg·L⁻¹·h⁻¹,为目前报道的全细胞系统最高水平,媲美纯酶级联。
结果10、副产物果糖高值化利用
反应中累积果糖55 mM,引入D-塔格糖3-差向异构酶(DTE)粗酶液,55°C下2 h转化30%果糖为D-阿洛酮糖(16.5 mM,2.97 g/L)。首次实现Reb-M生产过程中副产物升级,提高碳效率约15%。
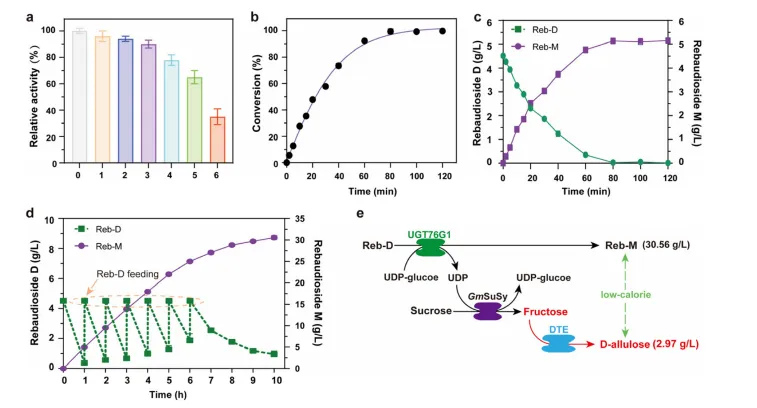
图6 条件优化
八、讨论
本研究成功构建了首个集成化大肠杆菌全细胞级联平台,通过多维度工程策略(酶表达调控、透性化处理、过程优化、补料分批)实现了Reb-M的创纪录高产(30.6 g/L),并创新性将副产物果糖转化为高附加值D-阿洛酮糖,显著提升了原子经济性与绿色度。该平台契合绿色化学原则:①蔗糖驱动的UDP-Glc原位再生,避免外源辅因子添加;②免酶纯化、温和反应条件降低能耗;③催化剂可重复使用减少废弃物;④副产物资源化提升整体效益。未来需进一步强化酶热稳定性、开发更绿色的透性化方法、优化副产物模块与原途径的耦合,以推动工业化应用。本研究为高值糖苷及天然产物的绿色生物制造提供了可扩展的范式。
