IF21.1!中国农业科学院&北大联手用“国自然+多组学”荣登《Science Bulletin》顶刊!揭示50种RNA引导核酸酶活性与特异性全景!
- 2026-05-09 03:07:20



🧬CRISPR/Cas系统作为RNA引导的核酸酶,在基因编辑领域取得了革命性进展。本研究对跨越10个亚型的50种RGNs进行了大规模平行评估,系统测定了其编辑效率、脱靶效应、基因组结构变异和细胞毒性。
🔎结果表明,AsCas12a-Ultra、LbCpf1等变体效率与SpCas9相当或更高,该研究建立了首个RGN多维性能评估框架,为精准基因编辑工具的选择提供了数据驱动的决策支持。
📚如果你也想用“国自然+多组学”发文的话,关注兔子生信,联系我们带你进一步了解~

文章标题:RNA引导核酸酶活性与特异性的大规模平行表征
发表期刊:Science Bulletin
发表时间:2026年3月23日
影响因子:IF21.1/Q1


CRISPR/Cas9自问世以来极大推动了基因编辑领域的发展,但其存在PAM限制和递送瓶颈。然而,这些系统缺乏系统性的平行比较,其编辑效率、特异性、脱靶风险和细胞毒性尚未得到全面评估,限制了研究者针对特定应用场景的合理选择。


本研究选取50种RGNs各设计48个内源位点。RGN和sgRNA分别由两个质粒表达,共转染HEK293T细胞后,通过FACS分选双阳性细胞,利用高通量测序定量编辑效率。通过CCK-8和直接细胞计数评估细胞毒性,通过RNA-seq分析差异表达基因和通路富集。

你是否也在寻找生信分析的最佳拍档?你是否也想拥有同款高分文章的漂亮图表?别再徘徊,速来联系兔子生信团队!我们提供从思路设计到数据挖掘的全流程服务,让你的科研之路轻松跳跃!
🌎为什么需要系统比较这么多基因编辑工具❓
🌟现有RGNs在效率、特异性和安全性上差异巨大,但缺乏平行比较,导致工具选择缺乏数据支撑。
🌎哪些RGNs在效率和特异性上表现优异❓
⌛️AsCas12a-Ultra效率最高,AsCpf1-YH脱靶风险最低,而紧凑型enOsCas12f1兼具较高效率和低毒性,适合AAV递送。
🌎这篇研究覆盖了什么❓
🧠从50种RGNs的编辑效率、删除模式、全基因组脱靶分析、染色体易位检测到细胞毒性评估,系统揭示了效率与特异性的权衡关系,并建立了首个RGN多维性能评价框架!
50种RGNs在多个内源位点的编辑效率比较

针对TTAAN PAM的RGNs中,AsCas12a-Ultra、LbCpf1、AsCas12a-Plus和LbCpf1-RVRR的编辑效率均高于SpCas9,其中AsCas12a-Ultra的提升具有统计学显著性(图1)。
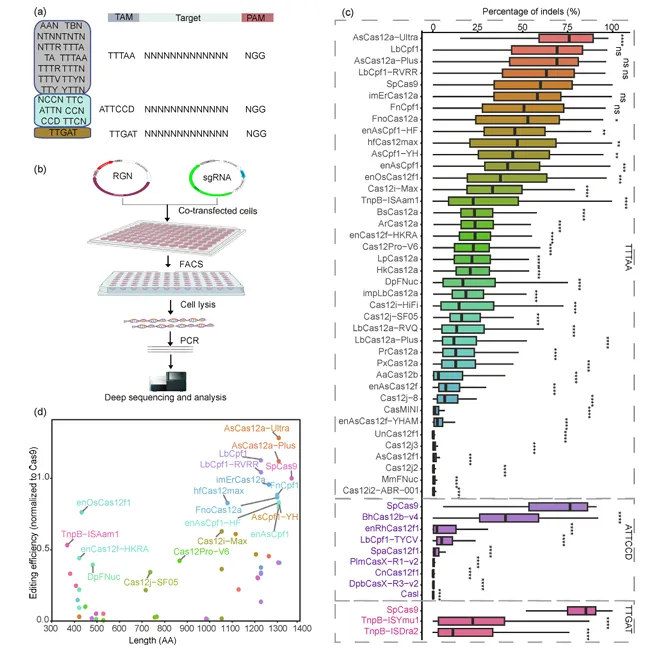
图1. 50种RGNs在多个内源位点的编辑效率比较
针对ATTCCD和TTGAT PAM的所有RGNs效率均低于SpCas9。值得注意的是,紧凑型RGN enOsCas12f1达到了41.50%的编辑效率,展现出良好的应用潜力。

对19种代表性RGNs的删除模式分析显示,多数RGNs的删除概率在靶点中段达到峰值。SpCas9、FnCpf1和FnoCas12a主要诱导18-21位的高密度删除;Cas12i-Max的删除范围更宽;enOsCas12f1呈现独特的删除模式,峰值位于24位,删除主要发生在靶点下游(图2)。
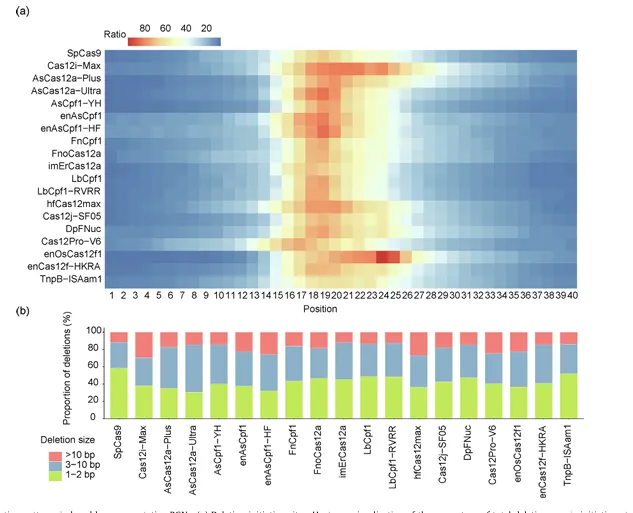
图2. 代表性RGNs诱导的删除模式
删除长度方面,SpCas9和TnpB-ISAm1主要诱导1-2 bp短删除,而大多数其他RGNs以3-10 bp删除为主,Cas12i-Max则倾向于产生超过10 bp的长删除。

通过GUIDE-seq检测发现,DpFNuc的脱靶位点数量最高,其次是enCas12f-HKRA和Cas12i-Max。AsCpf1-YH的脱靶活性最低,优于SpCas9(图3)。
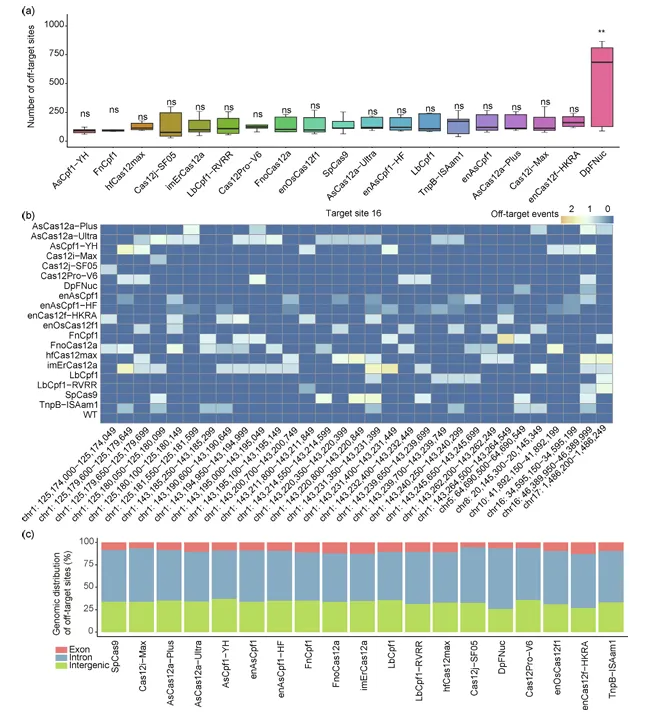
图3. 19种RGNs的sgRNA依赖性脱靶效应分析
脱靶位点在基因组中主要分布于内含子,其次为基因间区和外显子。编辑效率与脱靶活性之间无显著相关性,提示两者可能受不同机制调控。

PEM-seq分析显示,染色体易位频率与总体编辑活性呈显著正相关。sgRNA依赖性易位在DpFNuc和enCas12f-HKRA中比例最高(图4)。
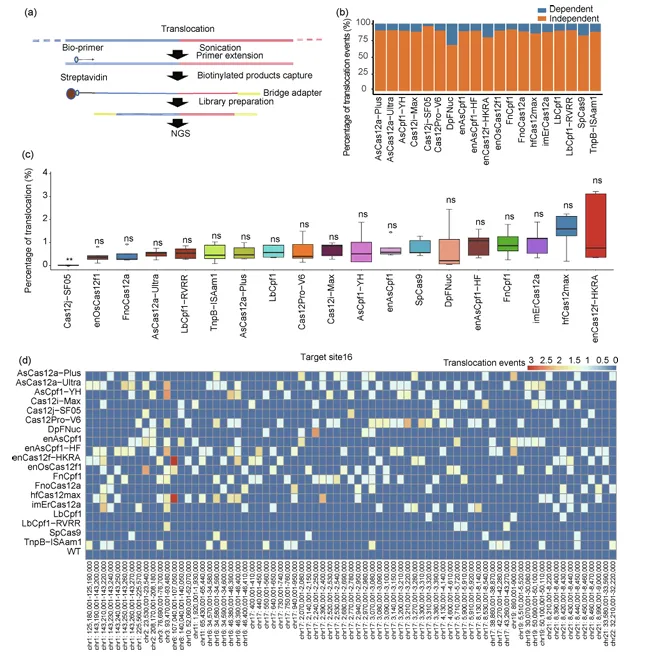
图4. RGNs相关的基因组结构变化。
enCas12f-HKRA、hfCas12max和imErCas12a的总易位率最高,而FnoCas12a、enOsCas12f1和Cas12j-SF05的易位率最低。易位热点主要集中在靶点16附近,占全部检测事件的49.33%。

CCK-8和直接细胞计数评估显示,enRhCas12f1、SpCas12f1和HKcas12a的细胞毒性最低,而Cas12i-HiFi和enAsCpf1-HF的细胞毒性最强(图5)。
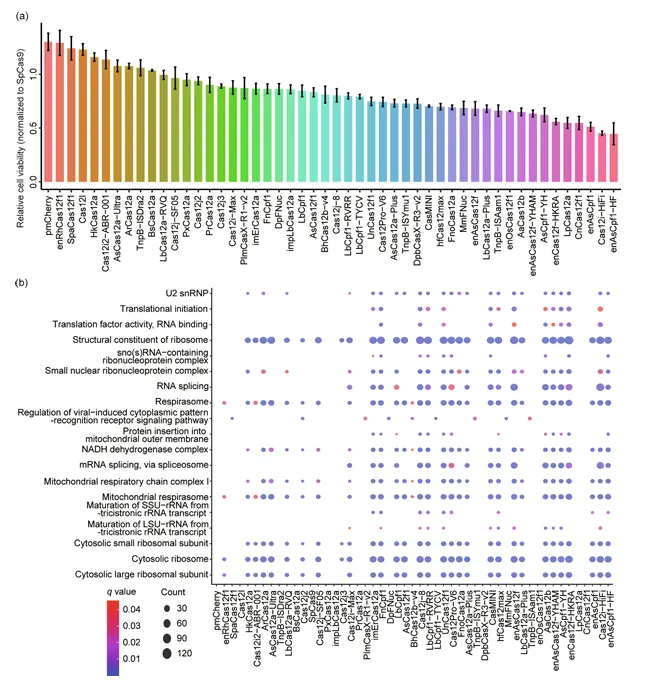
图5. 50种RGNs的细胞毒性及转录组影响
RNA-seq结合GO分析表明,高细胞毒性RGNs显著下调了核糖体亚基基因和线粒体呼吸链基因的表达,提示其可能通过干扰核糖体生物发生和ATP产生来抑制细胞增殖。

研究建立了包含细胞毒性、基因毒性和编辑活性的三维评估框架。AsCas12a-Ultra实现了最高编辑活性和极低细胞毒性,是敏感细胞类型编辑的理想选择。enOsCas12f1兼顾高效率、紧凑尺寸和低基因毒性,适合AAV递送的体内治疗应用(图6)。
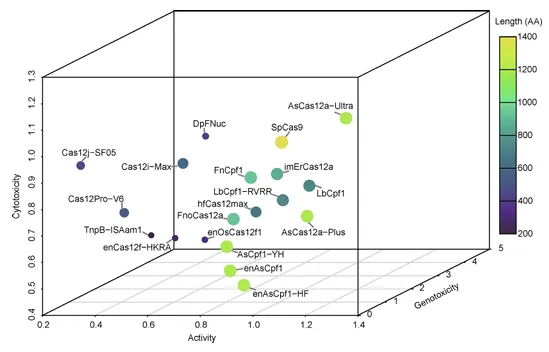
图6. 50种RGNs的多维性能图谱
AsCpf1-YH和FnCpf1具有较低的sgRNA依赖性脱靶风险,适用于高精度编辑场景。DpFNuc虽然脱靶位点最多但易位率较低,可能与其总体切割活性较低有关。
本研究首次对50种RNA引导核酸酶进行了大规模平行系统评估,涵盖编辑效率、删除模式、脱靶效应、染色体易位和细胞毒性五个维度。
AsCas12a-Ultra、LbCpf1等变体的编辑效率达到或超过SpCas9;紧凑型enOsCas12f1兼顾高效率与低基因毒性,适合AAV体内递送;AsCpf1-YH和FnCpf1脱靶风险最低,适用于高精度编辑;高细胞毒性RGNs通过下调核糖体和线粒体呼吸链基因抑制细胞增殖
本研究建立的三维评估框架为基因编辑工具的理性选择提供了数据驱动的决策支持。
如果你也想用“国自然+多组学”进行发文,思路复现,那就快来联系我们吧~




IF48.5!华中科技大学&武汉大学联手用“国自然”荣登《Nature》!揭示饮食脂质通过调控T细胞铁死亡影响免疫应答!




