《食品科学》:仲恺农业工程学院杨文华副教授等:蛋清卵转铁蛋白结构及其生物活性研究进展
- 2026-05-20 04:13:22


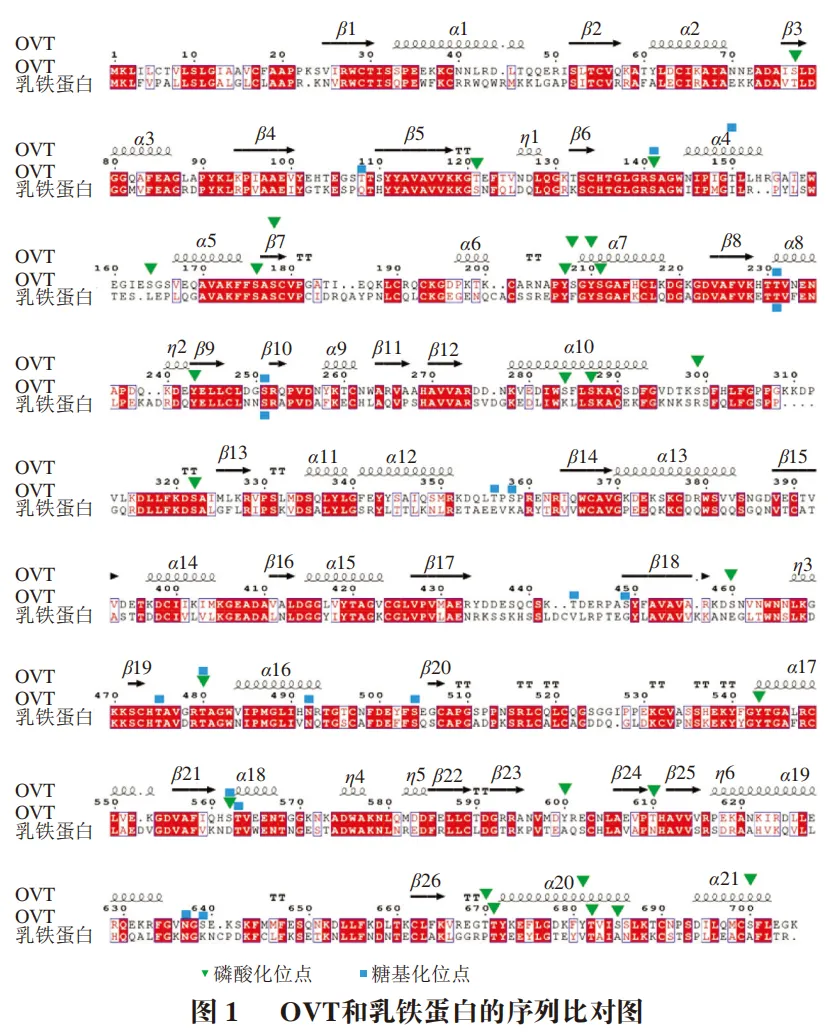
卵转铁蛋白(OVT)约占鸡蛋蛋清总蛋白质含量的12%~13%,仅次于卵清蛋白。它与人源乳铁蛋白(HLF)、牛源乳铁蛋白(BLF)、血清转铁蛋白、黑色素转铁蛋白同属转铁蛋白家族成员,且与BLF、HLF有着较高的同源性(达到50%)(图1)。此外,OVT与乳铁蛋白还具有相似的三维结构,这也使得它们具有许多类似的功能特性,如增强铁吸附、抗氧化活性、免疫调节和抗菌作用等。与乳铁蛋白相比,OVT的优势在于其在蛋清中的含量大约比牛奶中的乳铁蛋白高出140 倍,因此,从鸡蛋中提取OVT更容易。目前,OVT常用的分离纯化方法有硫酸盐沉淀法、有机溶剂沉淀法、色谱法等。
两种不同形式的OVT(不含铁的和与铁结合的)结构及理化性质有所不同,直接影响其在食品体系中加工、贮藏和食用过程中的性能,因此,对OVT结构和理化性质的研究不仅有助于OVT的广泛应用,而且有助于更好地理解蛋清在食品系统中的功能。
仲恺农业工程学院轻工食品学院的范雁、杨文华*、梁灿欢等综述OVT的纯化和分离方法,阐述OVT的两种形式及结构,系统介绍OVT的生物活性及其应用。同时,提出当前OVT研究中面临的挑战和仍需努力的方向,为OVT在食品加工、营养品开发等领域提供新思路和方向。
01
OVT的分离和纯化

目前,从鸡蛋清中分离纯化OVT的方法有多种,主要包括沉淀法和色谱法等。

1.1 沉淀法
沉淀法是一种基于溶解度或等电点差异分离蛋白质的方法。最早在1950年,Fraenkel-Conrat首次使用硫酸铵在pH值为3的条件下沉淀蛋白质,从蛋清中分离获得了OVT,但其纯度很低,仅40%。Warner等使用50%乙醇溶液在0.02 mol/L氯化钠溶液(pH 6~9)中分离获得OVT,包括不含铁的和含铁的两种形式,然而使用该方法提取出的蛋白纯度只有44%。随后,Ahn团队采用2.5%硫酸铵和2.5%柠檬酸的酸性盐组合从蛋清中分离获得的OVT纯度能够达到88%以上,而且该方法操作简单、快速且易于放大。同年,该团队又采用阳离子交换色谱、等电沉淀、硫酸铵和柠檬酸沉淀以及热处理的组合依次分离蛋清中的溶菌酶、卵黏蛋白、卵清蛋白和OVT,OVT的产量超过82%,纯度达到90%以上。此外,华中农业大学的鸡蛋研究团队也对蛋白质共纯化进行了深入研究,Ji Shengnan等首先用蒸馏水和甘氨酸-氢氧化钠缓冲液(0.1 mol/L、pH 9.3)依次洗涤树脂,将溶菌酶与其他不溶性和未吸附的蛋白质分离。然后,通过盐析、等电点沉淀和乙醇沉淀分离卵黏蛋白、OVT、卵类黏蛋白和卵清蛋白,其中OVT的纯度达到90%以上,产量为82%。Geng Fang等使用聚乙二醇沉淀法和阴离子交换层析共纯化鸡蛋清蛋白,与盐沉淀不同,阴离子交换层析前不需要脱盐,聚乙二醇有利于维持蛋白质的生物活性,最终在15%聚乙二醇8000的条件下获得了纯度为95%的OVT,回收率达到78%,该方法操作简单,且纯度高。从以上研究中发现,目前大多数共纯化方法都使用了离子交换树脂或层析法,并辅以沉淀法。这些组合方法具有操作简便、节省原材料和纯化周期短等优点。

1.2 色谱法
为了进一步提高OVT的纯度和产量,减少蛋白在纯化过程中发生的结构变化,人们将色谱法应用于OVT的分离过程,其中离子交换色谱应用最广泛。Rhodes等在羧甲基纤维素色谱柱上利用pH 8.5 0.1 mol/L乙酸铵分离得到OVT,该方法不需要蛋白质结晶和硫酸铵的进一步分离就可以直接提取得到OVT,然而,该方法获得的蛋白容易被球蛋白污染。随后,Al-Mashikiii和Chung等分别将固定化金属亲和层析和DEAE亲和凝胶蓝色层析应用于OVT的分离纯化中,显著提高了OVT的纯度,根据聚丙烯酰胺凝胶电泳显示纯度能够达到94%~98%,然而,这个过程可能会发生蛋白质变性,因为需要剧烈的洗脱条件打破蛋白质与柱子之间的强相互作用,而且固定化金属亲和色谱也相对昂贵,限制了其在工艺规模上的应用。随后,有报道发现阳离子交换色谱和阴离子交换色谱也可以用于OVT纯化。Guérin-Dubiard等通过S Ceramin Hyper-DF阳离子交换色谱从蛋清中分离纯化的OVT纯度为89%。Tankrathok等先在Q-Sepharose Fast Flow柱上进行阴离子交换层析,然后再通过CM Toyopearl 650 M阳离子交换层析获得的OVT纯度为80%,然而,该方法获得的OVT回收率较低(21%)。与离子交换色谱相比,凝胶渗透色谱在工艺层面的适用性较低,因为它需要在将鸡蛋蛋白样品上柱之前去除脂质,而离子交换柱则不需要。然而,通过凝胶渗透色谱分离后,蛋白质结构不会发生构象变化,仍能保持初始活性。Wang Jianshan等还利用在线单柱二维液相色谱法对蛋清中的3 种活性蛋白进行了快速分离纯化,该技术可在70 min内完成对鸡蛋清中溶菌酶、卵清蛋白和OVT 3 种活性蛋白的快速分离纯化,其纯度分别为95%、93%和97%。该方法减少了样品的处理步骤,对样品的污染小,纯化速度快,操作简单,易于实现自动化和放大,在活性蛋白的快速分离制备和工业化生产方面具有广阔的应用前景。

1.3 电泳法
电泳法是一种将目标蛋白与其他杂质分离的方法,其原理是带电分子在电场中向与其电特性相反的电极移动。分离蛋清中蛋白质的主要电泳方法是等电聚焦电泳和自由流动电泳。Wang Shuai等基于电极溶液中H+和OH—的定向迁移构建了自制的两性电解质自由流动等电聚焦系统,并用其成功分离OVT、卵黏蛋白和卵清蛋白。Shimazaki等使用非变性二维电泳分离由OVT、卵清蛋白和溶菌酶组成的混合体系,但该技术目前仅适用于实验室使用,不能广泛用于工业生产。因此,开发简单、高效、可扩大规模的OVT分离方法是其在营养保健品和制药行业实际应用中非常重要的一步(表1)。

02
OVT的结构和铁递送机制


2.1 结构
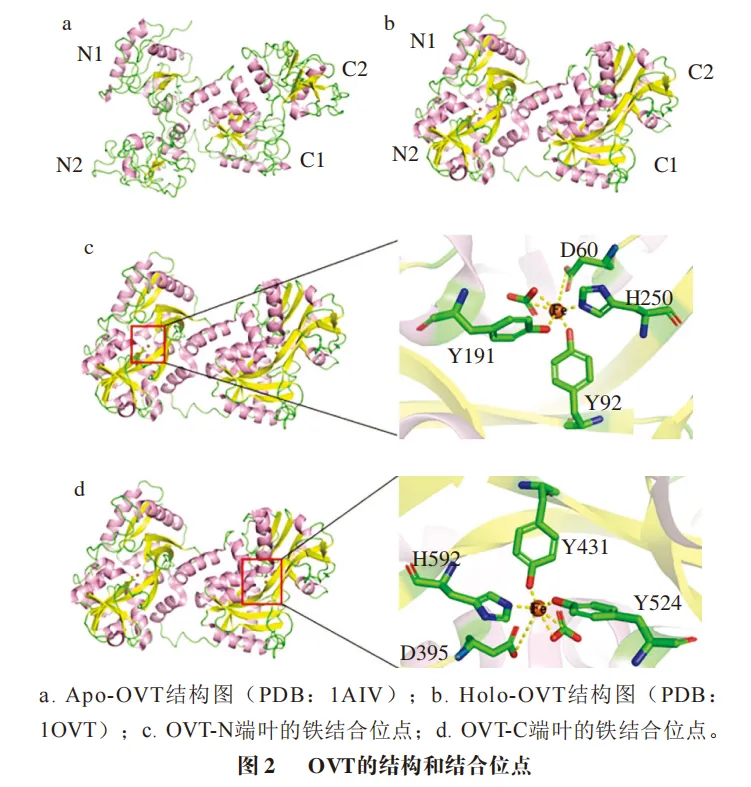
OVT是一种由686 个氨基酸和15 个二硫键组成的单链铁结合糖蛋白,糖基约占2%~6%,分子质量为77~80 kDa,不含游离疏基。在整体结构上,OVT由两个球状叶瓣组成,称为N端叶(残基1~332)和C端叶(残基342~686),它们通过9 个氨基酸残基(残基333~341)的α-螺旋连接,这些残基可以通过胰蛋白酶消化释放。15 个二硫键中有9 个位于C端叶,6 个位于N端叶。N端叶和C端叶通过非共价键和疏水相互作用结合,研究证明分离的N端叶和C端叶可以在溶液中重新结合。与其他同属于转铁家族的成员一样,每个叶可以进一步分为大小相似的α/β亚结构域(N1、N2和C1、C2),每个结构域有160 个残基;亚结构域由两条反向平行的β链连接,使得它们能够以铰链样机制打开和关闭。N端叶和C端叶的氨基酸序列具有37.4%的同源性,两个叶瓣的主要差异在于环状区域。天然的OVT分为两种形式:不含铁的(Apo-OVT)和与铁结合的(Holo-OVT),它们的三维结构由PubChem数据库(https://pubchem.ncbi.nlm.nih.gov/)查得,如图2a、b所示。
蛋白质翻译后修饰是指蛋白质在翻译完成后,通过在一个或多个氨基酸上添加修饰基团(如磷酸基、糖基和乙酰基等)改变其结构和功能的过程。确定OVT的修饰位点对于深入、全面地研究OVT在生理功能、结构、细胞活动以及疾病等诸多方面的作用都有着极为重要的意义。目前,除了在天然OVT中鉴定出2 个磷酸化肽中的两个磷酸化位点(Ser141和Ser211),Liu Yaping等在磷酸化OVT的样品中发现了更多的磷酸化位点(图1),其中大多数连接在丝氨酸残基上(Ser77、Ser141、Ser164、Ser176、Ser178、Ser208、Ser284、Ser287、Ser299、Ser322、Ser460、Ser562、Ser685和Ser700),其余位点则在苏氨酸残基(Thr121、Thr480、Thr610、Thr670、Thr671、Thr681和Thr682)和酪氨酸残基(Tyr207、Tyr210、Tyr243、Tyr543、Tyr600和Tyr681)上,这些位点主要是在α-螺旋和β-片层中。此外,曾齐对OVT糖基化位点进行了鉴定,确定了17 个糖基化位点(Ser141、Ser251、Ser358、Ser449、Ser504、Ser562、Ser639、Thr108、Thr150、Thr231、Thr356、Thr443、Thr475、Thr480、Thr563、Asn492和Asn637)。这些位点的鉴定为研究OVT的结构与功能间的关系提供了依据。

2.2 OVT的铁结合位点和铁释放机制
OVT的N端叶和C端叶都含有一个铁结合位点,位于每个叶瓣的裂隙内,每个Fe3+的配体由4 个氨基酸残基和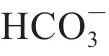 组成,在N端叶结构域中,4 个氨基酸残基包括存在于N1子结构域的Asp60、N2子结构域的Tyr 191和两种子结构域之间的铰链区处的Tyr92和His250,在C端叶结构域中,包括Asp395、Tyr524、Tyr431和His592(图2c、d)。
组成,在N端叶结构域中,4 个氨基酸残基包括存在于N1子结构域的Asp60、N2子结构域的Tyr 191和两种子结构域之间的铰链区处的Tyr92和His250,在C端叶结构域中,包括Asp395、Tyr524、Tyr431和His592(图2c、d)。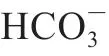 通过Arg121锚定在N端叶结构域中或者通过Arg 460锚定在C端结构域中参与铁离子的结合。两个叶瓣的铁结合能力不同(C端叶的铁结合常数:1.5×1018 L/mol;N端叶的铁结合常数:1.5×1014 L/mol),这可能是两个叶中结构域间相互作用的差异导致。因此,OVT能够以较高的亲和力结合铁离子,在生物体的铁代谢等过程发挥关键作用。除了铁,OVT还可与铬、铜、锰、锌、镍、钴和镉等二价阳离子结合,但其他二价阳离子与OVT的亲和力都低于铁(亲和力Fe3+>Cr3+,Cu2+>Mn2+、Co2+和Cd2+>Zn2+>Ni2+)。
通过Arg121锚定在N端叶结构域中或者通过Arg 460锚定在C端结构域中参与铁离子的结合。两个叶瓣的铁结合能力不同(C端叶的铁结合常数:1.5×1018 L/mol;N端叶的铁结合常数:1.5×1014 L/mol),这可能是两个叶中结构域间相互作用的差异导致。因此,OVT能够以较高的亲和力结合铁离子,在生物体的铁代谢等过程发挥关键作用。除了铁,OVT还可与铬、铜、锰、锌、镍、钴和镉等二价阳离子结合,但其他二价阳离子与OVT的亲和力都低于铁(亲和力Fe3+>Cr3+,Cu2+>Mn2+、Co2+和Cd2+>Zn2+>Ni2+)。
OVT在铁结合和释放后,每个叶都会发生大规模的构象变化:两个结构域间裂隙(在亚结构域N1和N2之间或亚结构域C1和C2之间)在铁吸收之前打开,在铁掺入铁结合位点时关闭。目前的证据表明,人类乳铁蛋白、转铁蛋白和OVT都具有相同的铁结合或释放机制。然而,对于OVT释放铁离子的机制目前尚不完全清楚。据报道,在没有阴离子螯合剂和酸性条件下,OVT的铁结合残基的质子化缓慢。OVT中铁离子的释放需要简单阴离子存在,例如焦磷酸盐、硫酸盐或氯化物,然而,C端叶的阴离子介导的铁释放速率比N端叶慢得多,因为N端叶中有两个阴离子结合位点,但在C端叶中只有一个阴离子结合位点。此外,在C端叶中,有一个子结构域间存在二硫键,即Cys478-Cys671,它可能限制铁结合裂隙的开放,Cys478和Cys671的选择性还原和烷基化导致对铁的亲和力降低。Dewan等根据Lys209-Lys301介导的亚结构域间相互作用解释了OVT在酸性pH值条件下的这种双相铁释放机制,即由于两个赖氨酸残基的质子化降低了pH值,促进了铁从N端叶释放,产生的两个正电荷非常接近,并且它们位于N端叶的结构域上,这很可能是打开蛋白质N端叶的两个子结构域(N1和N2)的驱动力,暴露出Fe3+并促进其释放。

2.3 OVT的铁递送过程
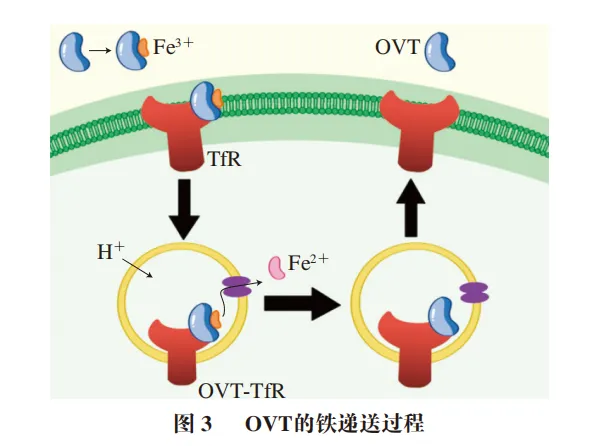
转铁蛋白家族的结构是为运输Fe3+而自然形成的,在结合和释放Fe3+前后,它们的结构会发生相应变化以适配Fe3+。基于转铁蛋白家族的铁递送过程,推测了机体中OVT运输铁离子的过程如下:OVT首先与Fe3+发生结合,随后,含铁的OVT与活性分裂细胞表面的OVT受体(TfR)相结合。此后,OVT-TfR复合物被细胞摄取并转运至内涵体。在此过程中,依赖ATP供能,H+被主动转运至内涵体。当内涵体内部的pH值降至5.5时,Fe3+从OVT中解离释放。与此同时,TfR在酸性环境下发生构象改变,但仍与Apo-OVT保持结合状态,直至该复合物重新回到细胞表面才发生脱离。Apo-OVT进入体液后,在肠道及血红蛋白分解部位再次与游离铁结合,从而开启下一轮铁离子运输循环(图3)。
03
OVT的理化性质


Apo-OVT与Holo-OVT的物理化学性质大有不同(表2)。Apo-OVT呈无色,在物理和化学条件下容易变性,结构更为松弛;而Holo-OVT则呈橙红色,对物理和化学处理不敏感,构象相对紧密且稳定。Apo-OVT的等电点为6.73,而Holo-OVT的等电点为5.78。此外,OVT在与铁结合时表现出3 种同型:未结合、与一个铁原子结合以及与两个铁原子结合,而铁有两种主要形式,氧化的三价铁形式或还原的亚铁形式。在有氧条件下,铁的三价形式最丰富。然而,三价铁的溶解度远低于亚铁形式的溶解度。另一方面,在缺氧条件下,亚铁形式占主导地位,在厌氧和酸性条件下,亚铁形式比三价铁形式更稳定。OVT在与其他金属离子结合时表现出不同的物理化学性质。例如,当OVT与Cu2+结合时,OVT呈黄色,在440 nm波长处出现最大吸收峰;然而,当与Zn2+络合时,热变性温度升高,并且对蛋白酶和各种变性处理的耐受性也有所提高。此外,Apo-OVT和Holo-OVT的功能性质也有不同,Apo-OVT具有清除过氧离子、螯合铁离子、促进脂质过氧化等功能,而Holo-OVT具有运输铁离子、抗氧化、抗菌活性、免疫调节等功能作用。

3.1 热稳定性
OVT是蛋清中最热敏的蛋白质,它在50 ℃时开始变性并聚集,并在55 ℃时完全聚集,这远低于巴氏杀菌温度。此外,热变性的OVT可能会导致其他蛋清蛋白的热聚集。因此,它被认为是蛋清初始热聚集的原因,提高其热稳定性,尤其是巴氏杀菌过程中的耐热性,是增强蛋清加工适宜性的最有效方法之一。据研究表明,多元醇(甘油和乙二醇)能通过竞争蛋白质上的疏水相互作用抑制温度介导的OVT聚集,并且甘油在抑制OVT聚集体的形成方面比乙二醇更有效。此外,也可以通过添加无机盐提高OVT的热稳定性,如硫酸盐、硫酸盐、氯化物和碳酸氢盐等能够提升OVT的初始聚集温度,硫酸盐和磷酸盐对OVT聚集的抑制能力相对较好。然而,由于无机盐对人体具有毒性,因此无法大量使用。而精氨酸作为一种天然存在的氨基酸,已经显现出其抑制OVT聚集的潜力,能够较好地解决无机盐不安全的问题。在精氨酸存在的情况下,将蛋清在90 ℃条件下热处理30 min,也没有观察到OVT聚集体,这可能归因于精氨酸对OVT的化学修饰以及精氨酸和OVT之间的特定相互作用。同时,甘氨酸、赖氨酸也可以通过提高OVT聚集的起始温度抑制OVT的热聚集,但它们在抑制OVT聚集方面不如精氨酸有效。还有来自蛋黄的天然卵黄高磷蛋白可以与热变性的OVT发生非共价相互作用,产生可溶性复合物阻碍OVT的热聚集。此外,糖基化反应和磷酸化反应在一定程度上也可以抑制OVT的热聚集。Liu Yaping等研究了不同pH值条件下磷酸化修饰OVT的耐热性,结果显示pH 8.0条件下OVT在巴氏杀菌过程中的耐热性最好,磷酸化修饰后的OVT二级结构中,β-折叠和展开结构向α-螺旋转变,使更多的疏水性氨基酸移动到OVT分子的表面,从而提高了热稳定性。

3.2 表面疏水性
表面疏水性代表蛋白质表面疏水基团的数量,可以反映蛋白质的构象变化。加热是提高OVT表面疏水性的有效手段,这归因于蛋白质的去折叠和更多暴露的疏水区域。高压处理也可以提高OVT的表面疏水性,这与处理样品的pH值有关。在pH值为8.0时,OVT的表面疏水性在400 MPa时开始增加,但在pH值为3.0时,OVT的表面疏水性在200 MPa时开始增加。同时,OVT的构象从最初的螺旋、折叠和聚集链转变为分子间双折叠形式。然而,该结构可以在大于500 MPa的压力下恢复到其原始构象。以冷冻形式运输和储存的蛋清在加工前不可避免地要经过解冻处理,而冻融处理也会影响蛋清蛋白的表面疏水性。研究人员发现,OVT的表面疏水性随着冻融周期的增加而波动很大,这归因于OVT在多次冻融过程中的大规模构象变化。此外,糖基化反应已被证明是降低OVT表面疏水性的可行方法。当亲水性糖(葡萄糖或乳糖)引入蛋白质表面,糖基化可以降低OVT的表面疏水性。Zhang Xianli等也发现了类似的现象,即OVT与葡萄糖结合后表面疏水性降低,而超声波辅助糖基化会导致表面疏水性进一步降低。超声处理后蛋白质结构展开,显示出更大的柔性,疏水基团暴露于分子的表面并与磷酸基团反应,导致表面疏水性的增加。

3.3 乳化性
蛋白质的乳化特性受许多因素的影响,例如蛋白质在空气-水(油-水)界面的吸附、吸附蛋白质的含量、界面处的构象重排和黏弹性界面膜的形成。良好的乳化性能使蛋白质在食品(蛋糕、冰淇淋、巧克力等)中发挥广泛的应用,因此改善OVT的乳化性能非常有前景。研究表明,磷酸化可以有效提升OVT的乳化性能。与天然OVT及干式加热后的OVT相比,在焦磷酸盐存在的情况下,OVT的乳化活性和稳定性更高,这是由于引入了大量带负电荷的磷酸基团使得蛋白溶液具有较高的电负性,在乳液体系中液滴之间具有足够强的静电排斥力,可以改善液滴表面的电荷强度,从而实现更好的空间稳定性并防止分子聚集。交联也被证明是制备具有强乳化能力的OVT基乳化剂的可行方法,由京尼平交联的OVT颗粒稳定的Pickering乳液能够保持长期的储存稳定性,并且可以抵抗包括不同离子强度和pH值的环境条件。OVT的组装产品已被用作稳定乳液的优质乳化剂。相比于单个OVT稳定的乳液,可溶性OVT-甜菜果胶复合物稳定的乳液液滴尺寸更小,这表明可溶性OVT-甜菜果胶复合物作为乳化剂比OVT具有更出色的乳化能力。这可能是由于OVT和甜菜果胶的协同吸附。而且,由可溶性OVT-甜菜果胶复合物稳定的乳液显示出更好的物理稳定性,这可能与乳液的液滴尺寸较小、乳液液滴之间有足够的静电排斥以及油滴表面周围界面层较厚有关。此外,OVT与自身或其他生物聚合物的不溶性组装产物被证明是有效的Pickering乳化剂。OVT的不溶性组装产物与自身或其他生物聚合物稳定的Pickering乳液表现出优异的乳化相体积分数和长期储存稳定性,这可能是由于乳化剂在油水界面的结构完整性、乳化剂的强界面吸附和凝胶状结构以及这些乳液的高黏度。

3.4 起泡性
起泡性是指气体相在液体基质中形成稳定分散体系的多相系统,出色的发泡性能够使蛋白质在食品中具有广泛的应用。Duan Xiang等研究了增强OVT发泡特性的方法,发现冻融处理可以改善OVT的发泡性能,并且随着冻融循环次数的增加,发泡容量和发泡稳定性逐渐提高。这是由于OVT的展开和重排构象导致其在冻融处理过程中在空气-水界面的吸附能力增强。Yu Yali等利用超声-辐照联合处理OVT增强了其起泡性,光谱结果显示OVT发生解折叠,α-螺旋和β-折叠的含量减少,促进了起泡性能的改善。
04
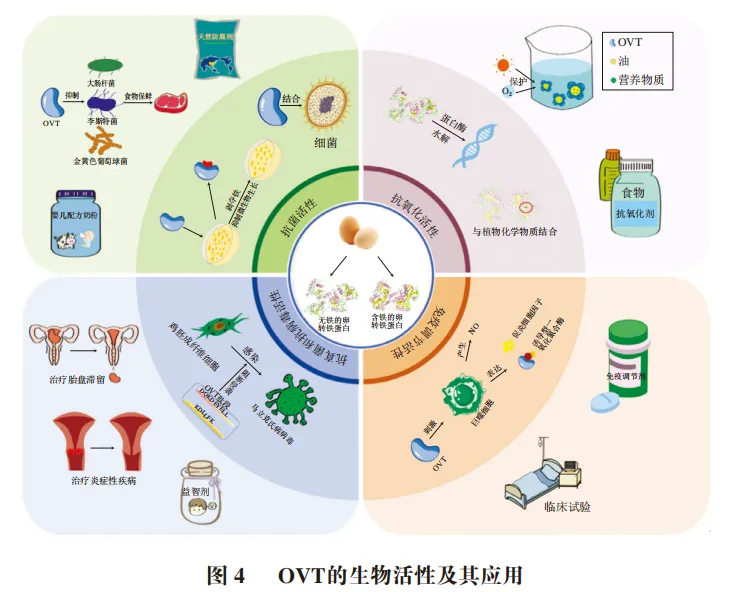
OVT的生物活性


4.1 抗细菌活性
OVT的抑菌活性来源于它能够结合微生物生长所必需的Fe3+。它的抗菌结构域存在于N端叶(残基1~332)中,对细菌、真菌、酵母和寄生虫表现出广谱的抗菌活性。OVT能够抑制常见的食源性病原体,如金黄色葡萄球菌、蜡样芽孢杆菌、单核细胞增生李斯特菌、大肠杆菌和幽门螺杆菌,而且其抗菌活性具有剂量依赖性。然而,OVT抗菌活性的敏感性在细菌种类之间差异很大:最敏感的物种是假单胞菌属、大肠杆菌和变形链球菌;最具抵抗力的是金黄色葡萄球菌、变形杆菌属和克雷伯氏菌。有研究表明,碳酸氢盐能够增加OVT对转铁蛋白敏感菌株(如表皮葡萄球菌和腐生葡萄球菌)的抗菌作用,但对金黄色葡萄球菌等耐药菌株的抗菌作用不强。在碳酸氢盐存在下将柠檬酸盐添加到OVT中时,观察到拮抗作用。然而,添加乙二胺四乙酸(EDTA)增强了OVT对大肠杆菌O157:H7和单核细胞增生李斯特菌的抗菌活性。Valenti等发现螯合Zn2+的饱和OVT比Apo-OVT或其他OVT金属络合物表现出更强的抗菌活性,这是Zn-OVT复合物的特性;此外,Zn-OVT复合物与细菌表面需要直接接触才能达到杀菌效果。因此,OVT的部分抗菌活性不仅仅是由于从培养基中剥夺了微生物生长所必需的铁,还涉及OVT与细菌表面直接结合相关的更复杂的机制。OVT能够渗透大肠杆菌外膜到达内膜,使得细菌内部的离子选择性渗透,导致电位变化和呼吸依赖性能量产生解偶联,从而发挥抗菌活性。Superti等也证明了OVT对肠道沙门氏菌(霍乱血清型)的抗菌作用取决于培养条件是否有利于OVT与细菌表面结合。此外,OVT抗菌活性机制增强与其蛋白结构变化紧密相关,Zhang Xianli等发现超声辅助糖基化后OVT中β-折叠和β-转角的比例显著增加,导致蛋白质结构更加稳定。改性OVT增强了其结构稳定性和溶解度,使其在破坏微生物的细胞膜方面更强大。
OVT具有的抗菌活性使得其可以作为婴儿配方奶粉成分治疗急性腹泻。此外,OVT还可以作为一种包装成分进行食品保鲜,以延长食品的保质期(图4)。Seol等开发了一种与EDTA结合的OVT抗菌膜,并将其用作具有抗菌特性的包装材料,通过抑制大肠杆菌来延长新鲜鸡胸肉的保质期。OVT还可以运输抗生素以形成OVT-抗生素复合物的载体。研究表明,由转铁蛋白受体介导的OVT内吞作用可用于将药物直接递送给病原体或细胞内感染细胞。OVT作为抗生素和天然防腐剂的新型安全替代品,其优异的抗菌活性能够广泛用于医药、包装材料和食品工业。

4.2 抗真菌和抗病毒活性
OVT对属于念珠菌属的物种具有抗真菌活性。Valenti等发现在测试的100多种念珠菌中,只有克鲁塞氏梭菌对OVT表现出抗性。碳酸氢盐增加并不能改变OVT对念珠菌属的抗真菌活性。在柠檬酸盐存在下,念珠菌属的抑菌效果与在没有柠檬酸盐介导的铁转运系统的细菌中观察到的结果相似。Giansanti等发现了OVT的抗马立克氏病病毒(MDV)活性,在抑制MDV感染方面,OVT比人转铁蛋白和牛乳铁蛋白更有效。然而,抗病毒活性与OVT的铁饱和度之间没有相关性。OVT的抗病毒活性是由于其肽段DQKDEYELL和KDLLFK能够阻断鸡胚成纤维细胞对马立克氏病病毒的感染,但多肽的感染阻断效率低于完整蛋白。Van Droogenbroeck等还在临床上使用OVT治疗养殖火鸡,成功地减少了鹦鹉热衣原体和禽细小病毒的数量。
目前,OVT已被测试可以作为治疗胎盘滞留、生殖道感染和子宫炎等炎症性疾病的治疗剂,以改善生殖道健康和生育能力。此外,由于OVT和乳铁蛋白之间高度的序列和结构同源性,推测OVT可能能够干扰假病毒的进入,并以与乳铁蛋白相同的方式调节相关的铁失调。

4.3 抗氧化活性
OVT是一种超氧化物歧化酶模拟蛋白,具有抗氧化活性,其抗氧化机制源于其清除超氧化物自由基(一种活性氧)的能力。然而,天然OVT的抗氧化活性相对较弱。近年来,一些研究人员将重点聚焦在提高OVT的抗氧化活性上,这对OVT作为功能性食品配料在食品工业中的应用具有极其重要的意义。当OVT与铁、镁和铜等金属离子,或与VC、咖啡酸、槲皮素和表没食子儿茶素-3-没食子酸盐等植物化学物质结合时,它可以表现出更高的抗氧化活性。You Juan等报道,当OVT中的赖氨酸(残基327)和谷氨酸(残基186)与绿茶中的儿茶素结合时,OVT复合物的氧自由基清除能力比天然OVT高4~5 倍。这些结果表明,对OVT进行修饰是改善其功能特性的有效策略。此外,OVT经过嗜热菌蛋白酶和胃蛋白酶消化后,所得OVT水解产物比天然OVT具有更高的氧自由基吸收能力。OVT水解物的抗氧化活性高低与酶的类型有关。Wickramasinghe等证明,用木瓜蛋白酶和蛋白酶组合、α-胰凝乳蛋白酶和木瓜蛋白酶组合以及弹性蛋白酶和α-胰凝乳蛋白酶组合水解OVT的水解物显示出更优异的抗氧化活性和Fe2+螯合活性。因此,选择合适的酶水解OVT对提高其抗氧化活性至关重要。
许多天然抗氧化成分已从植物中分离并生产出来以取代合成抗氧化剂,从而改善食品的味道和质量,并延长食品的保质期。OVT及其水解产物的高抗氧化性具备代替人工抗氧化剂的潜力,不仅可以控制食品中的脂质氧化,还可以为消费者提供额外的必需氨基酸。此外,OVT还可以用于制备食品级载体以提高营养活性成分的生物利用度,例如纳米颗粒载体和微胶囊化,凸显了其作为营养保健载体的巨大潜力。

4.4 免疫调节活性
免疫调节是指生物体识别和排除抗原性外来物质并维持其生理动态平衡和相对稳定的生理功能的过程,主要通过免疫系统达到生物体的平衡和稳定。与转铁蛋白家族的其他成员一样,OVT是先天免疫的一个组成部分。在鸡的体内,OVT被表征为急性期蛋白,其水平在炎症和疾病期间会有所升高。Xie Hang等报道了OVT对巨噬细胞和嗜异性粒细胞具有免疫调节作用。Ru Zhiying等发现OVT能够刺激RAW264.7巨噬细胞中一氧化氮的产生、诱导型一氧化氮合酶和促炎细胞因子的表达,并增加与巨噬细胞活化相关的丝裂原活化蛋白激酶(MAPK)信号通路的磷酸化水平。Zhu Gaoxiang等发现OVT可促进细胞因子和TNF-α、干扰素-γ、白细胞介素-4和白细胞介素-10基因的表达,以及增加免疫球蛋白A和分泌型免疫球蛋白A的分泌,从而促进小鼠的肠道体液免疫反应。OVT可以通过抑制NF-κB和MAPK活化抑制RANKL介导的破骨细胞产生和吸收,从而通过调节破骨细胞的产生和破骨细胞寿命来预防骨质疏松症。此外,OVT还可以改善环磷酰胺诱导的免疫功能障碍。
因此,OVT可用作天然免疫调节剂,以增强先天性和适应性免疫系统的免疫反应,从而预防疾病。而且,OVT于2020年11月用于临床试验,以评估OVT作为COVID-19患者免疫调节剂的疗效和安全性,并被纳入临床试验注册研究。
05
结 语

本文对OVT的分离和纯化方法、结构和理化性质及其功能特性进行了系统综述。虽然目前已经研究了各种简单、经济的OVT分离方法,但OVT及其衍生肽的规模化工业生产和应用尚未完全实现。其次,OVT的物理化学性质会影响其在食品系统中的应用潜力,良好的热稳定性和乳化性是决定OVT在食品加工和营养品开发中应用的关键因素。此外,关于OVT的多种功能特性,许多研究仍处于实验室和动物试验阶段,其生物利用度和安全性评估仍需进一步验证,特别是在长期摄入和特殊人群中的应用效果和潜在风险。未来研究应聚焦于通过基因工程和酶工程技术优化OVT的功能特性,开发高效、低成本的制备工艺,并结合多组学技术深入解析其作用机制,为OVT在功能性食品、营养补充剂及医药领域的创新应用提供理论支持和技术保障。
引文格式:
范雁, 杨文华, 梁灿欢, 等. 蛋清卵转铁蛋白结构及其生物活性研究进展[J]. 食品科学, 2025, 46(17): 424-434. DOI:10.7506/spkx1002-6630-20250301-003.
FAN Yan, YANG Wenhua, LIANG Canhuan, et al. Research progress on the structure and biological activity of egg white ovotransferrin[J]. Food Science, 2025, 46(17): 424-434. (in Chinese with English abstract) DOI:10.7506/spkx1002-6630-20250301-003.
点击下方阅读原文即可查看文章相关信息。
实习编辑:李雄;责任编辑:张睿梅。点击下方阅读原文即可查看全文。图片来源于文章原文及摄图网
近期研究热点



长按或微信扫码进行注册
为系统提升我国食品营养与安全的科技创新策源能力,加速科技成果向现实生产力转化,推动食品产业向绿色化、智能化、高端化转型升级,由北京食品科学研究院、中国食品杂志社《食品科学》杂志(EI收录)、中国食品杂志社《Food Science and Human Wellness》杂志(SCI收录)、中国食品杂志社《Journal of Future Foods》杂志(ESCI收录)主办,合肥工业大学、安徽农业大学、安徽省食品行业协会、安徽大学、合肥大学、合肥师范学院、北京工商大学、中国科技大学附属第一医院临床营养科、安徽粮食工程职业学院、安徽省农科院农产品加工研究所、安徽科技学院、皖西学院、黄山学院、滁州学院、蚌埠学院共同主办的“第六届食品科学与人类健康国际研讨会”,将于 2026年8月15-16日(8月14日全天报到)在中国 安徽 合肥召开。

长按或微信扫码进行注册
会议招商招展
联系人:杨红;电话:010-83152138;手机:13522179918(微信同号)

